キノホルムの神経毒性、半世紀以上経ってもメカニズムは完全には解明されていない
京都府立医科大学は3月28日、薬害スモン(亜急性脊髄視束神経症)を引き起こしたキノホルム(クリオキノール)がミトコンドリア毒性を誘発することを明らかにしたと発表した。この研究は、同大大学院医学研究科中央研究室・RI部門の勝山真人研究教授、分子病態病理学の矢追毅助教、病態分子薬理学の楳村敦詩教授、国立医薬品食品衛生研究所・医薬安全科学部の荒川憲昭室長、国立病院機構・鈴鹿病院の木村円研究員ら研究グループによるもの。研究成果は、「FEBS Letters」にオンライン掲載されている。
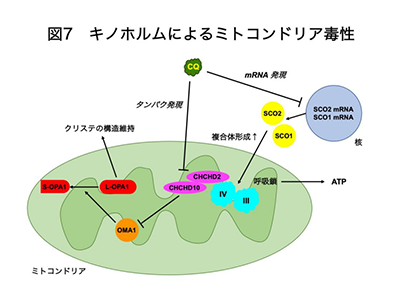
画像はリリースより
(詳細は▼関連リンクからご確認ください)
亜急性脊髄視束神経症(スモン)は、猛烈な腹痛に続き、特有の痺れ感が足先から下肢全体、あるいは腹部・胸部にまで上行する神経疾患。下肢の痙縮や脱力をきたし、重症例では視力障害や失明、さらには脳幹障害による死亡例まで存在する。1960年代に日本で多発し、同時に各地で集団発生したことから新たな感染症が疑われ、大きな社会問題となった。
1970年にスモン患者の多くで緑色の舌苔、緑便、緑尿が認められることが注目され、緑尿の成分分析の結果、緑色物質の本体は当時整腸剤として多用されたキノホルム(一般名:クリオキノール)と鉄イオンのキレート化合物であることが判明した。キノホルム製剤の使用禁止以降、新たな患者の発生が止まったことから、スモンはキノホルムによる薬害と確定した。しかし、それから半世紀以上が経過したにもかかわらず、キノホルムによるスモン発症のメカニズムは未解明のままだ。
一方、キノホルムは金属イオンを介するタンパク質の凝集を抑えることから、近年海外において神経変性疾患に対する改善効果が注目され、その類縁化合物として開発されたATH434が多系統萎縮症の希少疾病用医薬品として承認されている。こうした化合物による新たな薬害の阻止と、より安全な薬剤開発のためには、キノホルムの神経毒性の分子基盤の解明は必須だ。
キノホルムはスモン症状と関連する遺伝子発現変化を引き起こす
研究グループは、これまでにDNAチップを用いて培養神経芽細胞腫においてキノホルムにより発現が変動する遺伝子を網羅的に解析し、以下の発見を報告してきた。1)キノホルムの細胞毒性にはDNA二本鎖切断によるATMの活性化、およびそれに伴うがん抑制性転写因子p53の活性化が関与すること、2)キノホルムが転写因子c-Fosの発現誘導を介して、痛み反応に関与する神経ペプチド前駆体VGFの発現を誘導すること、3)キノホルムが転写因子GATA-2およびGATA-3の発現抑制を介して、腸炎、視神経炎、神経因性疼痛への関与が報告されているインターロイキン-8(IL-8)の発現誘導を引き起こすこと、4)キノホルムは細胞内に亜鉛を流入させるとともに銅シャペロンATOX1の酸化型への変換により銅の代謝障害を引き起こし、ドパミンβ水酸化酵素の成熟阻害を介して神経伝達物質ノルアドレナリンの生合成を阻害すること。
これらの知見から、VGF由来神経ペプチドやIL-8が、腹痛などのスモンの初期症状のみならず、引き続いて起こる感覚異常や視神経炎にも関与している可能性が考えられる。また、ノルアドレナリン合成の阻害は、交感神経系や青斑核から脊髄後角への下行性疼痛抑制系の機能障害につながる可能性がある。さらに、スモンの初期症状である猛烈な腹痛は副交感神経系の過剰亢進による腸管収縮に由来する可能性や、下行性疼痛抑制系の機能障害がスモンにおける感覚異常の一因である可能性も考えられる。
キノホルムは呼吸鎖複合体IVの形成を阻害し、ミトコンドリア毒性を示す
今回の研究では、ATOX1以外の銅関連タンパク質群についてもキノホルムによる影響があるのではないかと考え、その発現変化について培養神経芽細胞腫を用いて解析した。
網羅的解析および定量PCRの結果、キノホルムは20μM以上の濃度で、ミトコンドリア呼吸鎖複合体IV(シトクロムcオキシダーゼ)への銅輸送に関わるタンパク質SCO1とSCO2の発現をmRNAレベルで抑制することがわかった。これらのタンパク質は複合体IVの形成に必須である。
次に、非変性条件下でタンパク質を複合体として検出できるHigh resolution clear native PAGEを行った。抗COX4抗体で検出される複合体IVのスメア状のバンドは、キノホルム刺激したサンプルでは強度が低下した。抗UQCRC2抗体でも、高分子側の同じ位置に検出される複合体IIIと複合体IVの超複合体と考えられるバンドがキノホルム刺激により強度が低下した。また、複合体IVの酵素活性を測定したところ、キノホルムは20μM以上の濃度でその活性を低下させた。
グルコース不含培地下で、ミトコンドリアによる酸化的リン酸化に依存したATP産生を測定したところ、キノホルムは10μM以上の濃度でATP産生を有意に抑制した。しかし、同じ2時間の刺激では有意な細胞毒性(細胞膜の完全性の破綻)は認められなかったことから、キノホルムがミトコンドリア毒性を示すことが明らかとなった。
キノホルムはOMA1を介してOPA1を切断し、ミトコンドリア構造を破綻させる
OPA1は、ミトコンドリア内膜の融合とクリステの構造維持に関わるダイナミン様GTPアーゼであり、L-OPA1からS-OPA1への切断によりその活性を失う。研究グループは、キノホルムがOPA1の切断を引き起こすのではないかと考え、ウエスタンブロット法による解析を行った。その結果、キノホルムは10μM以上の濃度でL-OPA1からS-OPA1への切断を引き起こした。経時変化を観察したところ、刺激8時間以降でS-OPA1への切断が観察された。
OPA1の切断には、ミトコンドリア膜間腔に局在し、刺激によって活性化されるプロテアーゼOMA1の関与が知られている。そこで、ゲノム編集によりOMA1をノックダウンした細胞を作製したところ、キノホルムによるS-OPA1への切断が抑制された。
キノホルムは神経変性疾患に関わるミトコンドリアタンパク質の発現を抑制する
キノホルムによるOPA1の切断にOMA1が関与していたので、次に2つのミトコンドリアタンパク質CHCHD10とCHCHD2に着目した。両者は複合体IVの活性を増強することが知られている。また、CHCHD10の変異は筋萎縮性側索硬化症ならびに前頭側頭型認知症、CHCHD2の変異はパーキンソン病と連関することが報告されている。さらに、両遺伝子を欠損させたマウスではOMA1が活性化され、OPA1が切断されるとの報告がある。
そこで、キノホルムによるCHCHD10とCHCHD2の発現変化をウエスタンブロット法により解析したところ、両者とも10μM以上の濃度のキノホルムで発現が抑制された。経時変化を調べると、キノホルム刺激4時間で両者の発現は抑制された。
以上の結果から、キノホルムは1)SCO1、SCO2の発現をmRNAレベルで抑制し、呼吸鎖複合体IVの形成と酵素活性を抑制すること、2)CHCHD10、CHCHD2の発現をタンパク質レベルで抑制し、OMA1の活性化を介してクリステの構造維持に関わるOPA1の切断を引き起こすことにより、ミトコンドリア毒性を誘発することが明らかとなった。
スモン発症メカニズムの解明、他の神経変性疾患へも応用の可能性
今回の研究で、キノホルムがエネルギー(ATP)産生に重要な呼吸鎖複合体IVの形成を阻害すること、またクリステの構造維持に関わるタンパクの発現を抑えることにより、ミトコンドリア毒性を誘発することが初めて解明された。この研究成果は、キノホルムの神経毒性の一端を細胞レベルで証明したもので、キノホルムによるスモン発症メカニズムの全容解明に、さらに一歩近づいたものと考えられる。
「本研究が、今も後遺症に苦しんでいるスモン患者の治療に、すぐさま結びつくわけではない。しかし、キノホルム誘導体が多系統萎縮症などの神経変性疾患に対して臨床応用されつつあることから、今回発見したキノホルムによるミトコンドリア毒性発現機序は、より安全な神経変性疾患治療薬の開発に有益な情報を提供するものだ。スモン発症メカニズムの解明は、スモンが多発した我が国の研究者の責務であり、科学立国・日本の研究者として、何としても成し遂げなければならないことだと考えている。今後もキノホルムによるスモン発症メカニズムの全容解明のため、研究を続けていく」と、研究グループは述べている。
▼関連リンク
・京都府立医科大学 プレスリリース




