特発性肺線維症の治療法は確立されていない
大阪大学は3月11日、指定難病「特発性肺線維症」において、長鎖非コードRNAであるMIR205HGが基底細胞において高発現し、炎症性サイトカインIL33をRNAレベルで発現制御することを明らかにしたと発表した。この研究は、同大大学院医学系研究科の髙島剛志氏(博士後期課程)、病態病理学の森井英一教授、産業科学研究所の中谷和彦教授、大学院生命機能研究科の廣瀬哲郎教授、早稲田大学理工学術院の浜田道昭教授、千葉工業大学先進工学研究科の河合剛太教授らの研究グループによるもの。研究成果は、「JCI Insight」にオンライン掲載されている。
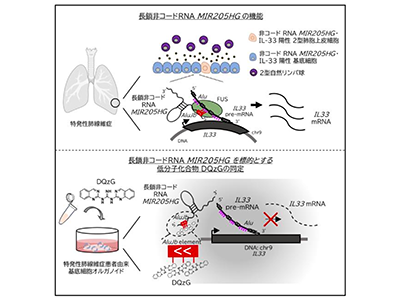
画像はリリースより
(詳細は▼関連リンクからご確認ください)
特発性肺線維症は、肺の奥深くで組織が固くなること(線維化)を特徴とする難治性の進行性肺疾患。この病気の進行を完全に止める治療薬はまだ開発されておらず、病態メカニズムの解明とそれに基づいた治療法の開発が望まれている。
これまでに、特発性肺線維症では本来ないはずの場所に基底細胞が出現し、その基底細胞の増加は予後不良を示すことが分かっていた。2022年には、基底細胞が細胞外マトリックスを増やし、筋線維芽細胞を活性化させることが初めて報告された。しかし、病態メカニズムの解明につながる基底細胞の機能については不明な点が多く残されていた。
長鎖非コードRNA「MIR205HG」を高発現する患者は予後不良
今回の研究では、正常および特発性肺線維症患者の肺におけるscRNA-seqデータを再解析することで、基底細胞に特異的かつ高発現している遺伝子として長鎖非コードRNA「MIR205HG」を同定した。同大医学部附属病院の患者サンプルを用いた予後解析では、MIR205HGの高発現群は予後不良を示した。特発性肺線維症において、MIR205HGの関与については、これまで報告がなかったことから、研究グループは新たな病態関与遺伝子として着目した。
MIR205HGは炎症性サイトカインIL33の遺伝子発現を制御する
長鎖非コードRNAは、さまざまな遺伝子の発現制御に関与するとの報告から、正常肺の肺胞上皮細胞あるいは特発性肺線維症患者由来の基底細胞からオルガノイドを樹立し、MIR205HGの過剰発現やノックダウンの実験を行うことで下流の発現変動遺伝子を探索した。さまざまなデータベースを用いて発現制御遺伝子を絞り込んだところ、MIR205HGが炎症性サイトカインIL33の遺伝子発現を制御していることが明らかとなった。
そのメカニズムとして、MIR205HGの遺伝子領域内(エクソン領域)に存在するAlujbエレメントがIL33のDNA/pre-mRNA(イントロン領域)と9か所で配列相同性があることが予測された。そこで、MIR205HG AlujbエレメントがIL33の発現制御において機能的であるのか検討した。実際にMIR205HGの全長ベクターとMIR205HG Alujbエレメントを欠失させたベクターを細胞へ導入すると、Alujbエレメントを欠失させたベクターを用いた細胞においてIL33の発現の上昇の程度が低いことが明らかとなった。
患者由来オルガノイドでIL33発現を抑制する低分子化合物を同定
そこで、低分子化合物の処理によって、MIR205HGのAlujbエレメントを標的としたIL33の発現抑制が可能か試みた。MIR205HGのAluJbエレメントに結合しうる低分子化合物をスクリーニングしたところ、新規の低分子化合物「DQzG」を同定した。特発性肺線維症患者由来オルガノイドにDQzGを処理したところIL33のRNAとタンパク質の発現減少を確認した。
MIR205HGが特発性肺線維症の病態にも関与する可能性を示唆
近年、肺線維化マウスモデルにおいてIL33が2型自然リンパ球(ILC2)を誘導することで線維化を促進することが報告されている。研究グループは、特発性肺線維症サンプルにおいて、MIR205HGとILC2との関連について調べることで病態関与の傍証となり得ると考えた。
いくつかの検討を重ねた結果、特発性肺線維症患者サンプルにおいて上皮細胞に発現するIL33は、MIR205HGの発現と正の相関関係があり、上皮細胞におけるIL33の高発現は予後不良を示すという結果を得た。MIR205HGの高発現例ではILC2の数の増加を認め、線維化領域内のMIR205HGとIL33を高発現する細胞の近傍にILC2が存在することも明らかにした。
特発性肺線維症の病態の一端が明らかに、治療薬開発にも期待
今回の研究により、特発性肺線維症において基底細胞がもたらす病態機構の一端が明らかになった。「基底細胞に高発現するMIR205HGのAlujbエレメントを標的とし、IL33の発現を抑制する低分子化合物DQzGは特発性肺線維症の新たな治療薬候補となりうる」と、研究グループは述べている。
▼関連リンク
・大阪大学 ResOU




