末梢感覚神経の損傷により発症する神経障害性疼痛、治療法や創薬に関する情報は乏しい
京都大学は3月14日、神経障害性疼痛の病態に関わる可能性のある分子として、transient receptor potential(TRP)スーパーファミリーの一種であり脊髄や一次感覚ニューロンなどに広く発現するTRP canonical 3(TRPC3)に着目し、脊髄後角ニューロンに発現するTRPC3が神経障害性疼痛の病態に重要な役割を果たしていることを明らかにしたと発表した。この研究は、同大大学院薬学研究科の白川久志准教授、大学院薬学専攻博士課程の戸堀翔太氏らの研究グループによるもの。研究成果は、「PNAS」に掲載されている。
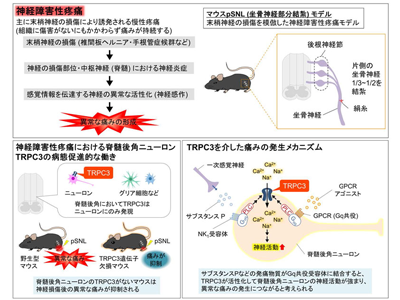
画像はリリースより
(詳細は▼関連リンクからご確認ください)
「痛み」という感覚は生体が組織の損傷を防ぐための警告システムとしての役割を担っている。しかしながら慢性疼痛の病態下では組織の傷害がほとんどないにもかかわらず、耐え難いほどの異常な疼痛が長期的に持続するため、患者のQOL(生活の質)が著しく損なわれる。神経障害性疼痛はそのような耐え難い慢性疼痛の一つであり、主に末梢感覚神経の損傷により発症する。神経障害性疼痛の病態形成においては、末梢および中枢における体性感覚神経系の感作、すなわち特定の神経刺激に対して反応が大きくなったり過敏状態になったりすることで、通常であれば痛みを惹起しないような弱い刺激(例:触覚刺激)に対しても痛みを感じてしまうようになることが、これまでの研究で明らかにされてきた。しかしながら、その治療的介入や創薬標的に関する情報は非常に乏しいものだった。
TRPC3に着目、Gq共役型受容体を介して疼痛制御に関与する可能性を検証
2021年のノーベル生理学・医学賞ではカプサイシンおよび熱刺激の受容体であるTRPV1や、メントールおよび冷刺激の受容体であるTRPM8が受賞対象分子となった。今回の研究では、同じTRPスーパーファミリーに属するTRPC3に着目した。TRPC3は元々、一次感覚ニューロンに機能的に発現することが報告されていた。さらに近年、ヒトを対象とした臨床研究において、TRPC3遺伝子座のイントロン部分に存在する一塩基多型(SNP)が慢性疼痛の発症と相関していることが報告された。したがって、TRPC3が関与する経路が神経障害性疼痛の病態に重要である可能性が考えられたが、そのような分子機構は検証されていなかった。
Gタンパク質共役受容体(GPCR)のうちGq共役型受容体は一次感覚ニューロンの侵害受容線維および脊髄における痛み情報の伝達に重要な役割を果たしている。TRPC3は、Gqタンパクの下流でホスホリパーゼC(PLC)の活性化によって産生されるジアシルグリセロール(DAG)により直接活性化される。TRPC3はサブスタンスP・アデノシン三リン酸(ATP)・プロテアーゼ・エンドセリン-1・ブラジキニンといったGq共役型受容体を介して痛みを惹起する物質のシグナリングに関与していることから、TRPC3がGq共役型受容体を介して疼痛制御に関与する可能性が考えられたが、そのような検証も全く行われていなかった。
骨髄系細胞以外でTRPC3を欠損するマウス、pSNL処置後の機械痛覚過敏が抑制される
そこで今回の研究では坐骨神経部分結紮(pSNL)を施したマウス神経障害性疼痛モデルを作成し、遺伝子改変マウスやmiRNAを用いた細胞特異的ノックダウン手法を駆使して、TRPC3の病態生理学的役割を検討した。その結果、pSNL処置による機械痛覚過敏および熱痛覚過敏がTRPC3欠損マウスでは顕著に抑制されることが明らかになった。骨髄系細胞でのみTRPC3を欠損する骨髄キメラマウスはpSNL処置により対照群と同程度に機械痛覚過敏を発症したが、骨髄系細胞以外でTRPC3を欠損する骨髄キメラマウスではpSNL処置後の機械痛覚過敏が抑制されることがわかった。
脊髄後角ニューロン特異的TRPC3ノックダウンで抑制、一次感覚ノックダウンは抑制されない
In situハイブリダイゼーションの結果も踏まえニューロンに発現するTRPC3にさらに着目して検討したところ、脊髄後角ニューロン特異的にTRPC3をノックダウンしたマウスではpSNL処置後の機械痛覚過敏が抑制されるが、一次感覚ニューロンでTRPC3をノックダウンしたマウスでは機械痛覚過敏は抑制されないことが明らかとなった。また、脊髄TRPC3の直接的な刺激により急性の機械痛覚過敏が形成されたが、一次感覚ニューロンTRPC3の直接的な刺激では疼痛様行動が惹起されなかった。
TRPC3の活性化、脊髄後角ニューロン発現のNK1受容体などの下流でCa2+流入を促進し疼痛シグナル増強と示唆
さらに脊髄NK1受容体やPLCの活性化により誘発される機械痛覚過敏はTRPC3欠損により抑制された。神経障害性疼痛の発症メカニズムにおいて、中枢における神経感作は侵害刺激に対する応答の増強または非侵害刺激に対する異常な疼痛反応の形成の原因となることや、TRPC3がCa2+透過性カチオンチャネルであることを踏まえると、脊髄後角ニューロンに発現するNK1受容体などのGq共役型受容体の下流におけるTRPC3の活性化は、神経障害性疼痛の病態形成においてCa2+流入を促進し、脊髄後角ニューロンの神経活動および疼痛シグナルを増強していると考えられる。
TRPC3阻害薬開発、神経障害性疼痛に対する有望な創薬戦略になると期待
研究成果は、末梢神経損傷後の神経障害性疼痛およびPLCの活性化により誘発される機械痛覚過敏の形成に対する脊髄TRPC3の関与を初めて明らかにしたものである。「今回の発見により、神経障害性疼痛の病態メカニズムとして痛みの伝導路である中枢のニューロンの活動を抑制するという戦略の重要性が明らかとなったことから、サブスタンスP・ATP・プロテアーゼ・エンドセリン-1・ブラジキニンなどの発痛物質を個別に阻害するよりも、神経活動の抑制という創薬戦略に注目が再び集まると考えられ、中枢神経系に到達するTRPC3阻害薬の開発が、いまだに著効薬が乏しい神経障害性疼痛に対する有望な創薬戦略になると期待される」と、研究グループは述べている。
▼関連リンク
・京都大学 最新の研究成果を知る




