第5のがん治療として期待のNIR-PIT、細胞死メカニズム解明が臨床承認へのハードル
名古屋大学は2月19日、新開発の顕微鏡である走査型電子線誘電顕微鏡(SE-ADM)を用いることで近赤外光線免疫療法(Near Infrared Photoimmunotherapy:NIR-PIT)の細胞死メカニズムを解析し、その細胞死を「Photochemosis」と名付け新規細胞死としての詳細機序を明らかにしたと発表した。この研究は、同大大学院医学系研究科・高等研究院・医工連携ユニット(JST創発的研究支援事業1期生)の佐藤和秀特任講師、総合保健学専攻オミックス医療科学の佐藤光夫教授、国立研究開発法人産業技術総合研究所(産総研)の小椋俊彦上級主任研究員、岡田知子テクニカルスタッフらの研究グループによるもの。研究成果は、「ACS nano」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
近年、光を用いた医療技術開発が次世代の新規治療方法として脚光を浴びている。その中でも、2011年に米国立がんセンターの小林久隆博士らにより報告された新しいがん治療法であるNIR-PITは新規のがん治療技術として注目されている。この治療法は、これまでと異なる方法でがん細胞を標的破壊できることから、手術・放射線・化学療法・がん免疫療法に続く、「第5のがん治療」として期待されており、世界に先駆けて日本で2020年9月にEGFRを高発現する再発既治療頭頸部がんに対して、限定承認を受けて保険適用されている。しかし、第3相試験開始時点では、NIR-PITによる細胞死のメカニズムは解明されておらず、これがNIR-PITの臨床承認に向けた大きなハードルとなっていた。
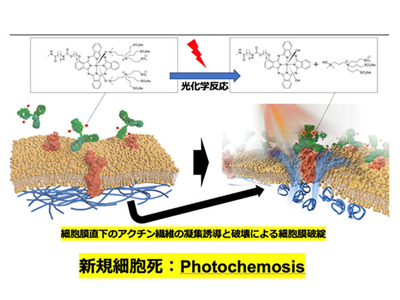
研究グループは2018年、NIR-PITによる細胞死のメカニズムの起点として、この治療法による細胞死の引き金となる物質を特定した。具体的には、複合体を近赤外光で照射すると、IR700(シリカフタロシアニン:SiPc)の親水性側鎖軸配位子(C14H34NO10S3Si:シラノール)が光化学的配位子反応により複合体から解離し、抗体を含む残りの構造は急速に疎水性となり、凝集した。この光化学反応によって、がん細胞膜上の表面抗原に対する抗体が凝集し、細胞破壊が誘発され、光化学反応がNIR-PITによる細胞死の開始の起点となっていることを明らかにしていた。しかし、この反応が標的細胞にどのような影響を与え、細胞破裂を引き起こすのかについては、解明されておらず、NIR-PITの細胞死の詳細はいまだに不明だった。
最近、新しい画像化技術である走査電子誘電率顕微鏡(SE-ADM)が産総研の小椋俊彦上級主任研究員によって開発された。この技術では、放射線損傷なしに、8nmの空間分解能で水溶液中のさまざまな生物学的サンプルを観察することができる。この分析では生きた細胞のナノスケールでの画像化が可能になり、これまで報告されていない新たな変化の検出が可能になる。今回、SE-ADMを用いてNIR-PIT治療細胞の詳細観察を行った。
アクチン重合阻害薬や細胞外液の高張条件でNIR-PITの細胞死は減少
まず、20%スクロース液で細胞外液を高張条件にした場合では、NIR-PITの細胞死は減少した。また、4℃で細胞機能を停止しても室温の場合とNIR-PIT細胞死の効果に変化はなかった。このことから、細胞膜の物理的破綻と細胞外からの水の流入が細胞死に係ることがわかった。
アクチン重合阻害薬を用いると、NIR-PITの細胞死は抑制された。SE-ADMを用いた解析で細胞膜直下に黒色の凝集粒子が生成されていることがわかり、さらにアクチン重合阻害剤でこの粒子は減少した。
アクチンタンパク質、NIR-PITにより凝集し構造変化
アクチンタンパク質の生化学的な解析で、NIR-PITによってアクチンタンパク質が凝集していることがわかった。また、アクチンGFP恒常発現細胞の細胞膜上のアクチンが、NIR-PITの近赤外照射直後に蛍光を喪失する(凝集による構造変化)ことがリアルタイムに観察され、この反応は生体内の腫瘍でも同様に起きていた。
チューブ内のタンパク質化学解析では、抗体・IR700複合体(trastzumab-IR700)、標的とする抗原(HER2)、アクチンはすべて近赤外光照射で凝集した。一方、他の水溶性の光吸収薬剤を用いた比較検討ではこのような変化は生じなかったため、アクチンに対しての反応はNIR-PITに特異的な変化であると考えられた。
IR700の光化学反応による疎水性への変化、アクチン構造の凝集引き起こし細胞破裂
以上の実験結果から、近赤外光の照射により、IR700の2つのシラノール基が光解離し、残りのシリコンフタロシアニン構造が凝集する反応がまず起こる。この親水性から疎水性への急激な変化は、受容体結合だけでなく、細胞膜と受容体タンパク質を支える皮質アクチン網目構造の凝集も引き起こす。この細胞膜直下の細胞骨格アクチンの破壊により、細胞膜を維持する機能が失われ、浸透圧の関係で細胞内に水が入り込み、細胞が破裂する。この一連の現象がNIR-PITの細胞死のメカニズムであり、従来の細胞死のメカニズム(アポトーシスやネクローシスなど)とは全く異なる。つまり、NIR-PITによる細胞死機序として、細胞膜直下のアクチン繊維(皮質アクチン網)が破綻することで細胞膜構造の維持ができなくなり、細胞内外の浸透圧較差で水分が流入し細胞死が破裂する「Photochemosis」機序を解明した。
NIR-PITによる「Photochemosis」、これまでとは異なる機序の細胞死を提唱
これまでのがん治療技術である手術、化学療法、放射線治療、がん免疫療法や既存の光治療である光線力学療法はアポートーシスないしはネクローシスが細胞死のメカニズムとして知られていたが、NIR-PITは機序の全く異なる新概念の「Photochemosis」が細胞死のメカニズムであり、NIR-PITの第5のがん治療技術としての地位が証明・樹立できた。
このユニークな細胞死「Photochemosis」により、NIR-PITは既存の抗がん剤や放射線治療、手術などとは全く異なる「第5のがん治療技術」として注目され、その治療効果とともに既存の標準治療への組み込みが期待できる。本機序解明を科学的な裏付けとしてNIR-PITは他のさまざまながん治療法との併用が期待でき、集学的ながん治療への応用が期待される。特に、NIR-PITとがん免疫療法(免疫チェックポイント阻害剤など)の併用療法は、大きな効果が期待でき、将来的には多くの患者の治療選択肢となる可能性がある。
「引き続き、人類が手にしたこの新規のがん治療技術によるがん細胞の変化の詳細解明や、治療の手立てが少ないがんへの適応を目指した新規治療を目的とした研究を行っていく」と、研究グループは述べている。
▼関連リンク
・名古屋大学 研究成果発信サイト



