肝臓の代謝情報から全身代謝を協調的に調節する機構、肥満背景の病態解明にも重要
帝京大学は1月27日、動物モデル(遺伝子改変モデルマウス)を用いて、肝臓に端を発した、全身糖代謝と体組成を制御する新しい臓器間ネットワーク機構の存在とその仕組みを明らかにしたと発表した。この研究は、同大医学部内科学講座の宇野健司准教授、東北大学大学院医学系研究科糖尿病代謝・内分泌内科学分野の片桐秀樹教授、東京女子医科大学実験動物研究所の本田浩章教授らの研究グループによるもの。研究成果は、「PLOS Biology」にオンライン掲載されている。
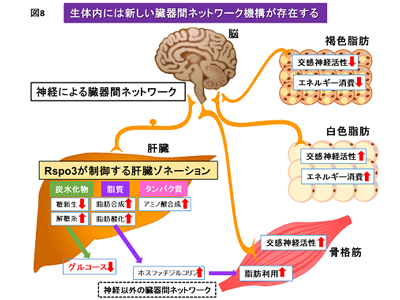
画像はリリースより
(詳細は▼関連リンクからご確認ください)
哺乳動物の生命機能、特に代謝恒常性は分泌生理活性物質、神経系や血管系ネットワークを介して体内各臓器が連携することで維持されている。飽食の現代、肥満を背景にこの恒常性維持機構が破綻し、糖尿病・メタボリックシンドロームの病態につながることが大きな問題となっている。
これまで、研究グループは、肝臓での脂肪やアミノ酸代謝に基づく情報が、自律神経ネットワークを介して各臓器、ひいては全身の代謝を協調的に調節するという、臓器間・栄養素間代謝連携機構が存在することを世界に先駆けて発見してきた。この機構は、肝臓を起点とし求心性(迷走)神経→脳→遠心性(交感)神経からなる神経ネットワークにより構築され、全身の代謝恒常性維持という生理機能を有する反面、過栄養が持続するとかえってメタボリックシンドロームの諸病態の進展につながる病態生理をも有することがわかってきた。これらはまさに、多様さ・複雑さを持って機能する生命原理が体内には存在していること、その一端を示していると言える。これらの知見を踏まえると、体内にはいまだ未知の臓器間ネットワーク機構が数多く存在していることが想定され、新たな臓器連携の仕組みを解き明かすことは非常に大切である。
肝臓は、肝細胞や動静脈、門脈、胆管などによって構築される無数の肝小葉構造が集まってできている。さまざまな栄養素の代謝は、肝小葉内の領域ごと(門脈域、中心静脈域、中間域)に分かれて(zonation)調節されており、このことは代謝の肝臓ゾネーション(metabolic liver zonation)と呼ばれている。しかし、これまで肝臓ゾネーションの詳細なメカニズムは明らかではなかった。
やせ型では食事摂食後に中心静脈域に収束するRspo3、肥満型では発現が減少
そこで、今回の研究では、この肝臓ゾネーションが生体内で時空間的にどのように調節され、全身の代謝や脂肪組織・骨格筋などの他臓器へいかなる影響を及ぼすのか、その機序を解明した。まず、肝臓において、肝臓ゾネーションに関与するR-spondin3(Rspo3)の生理的な発現様式をmRNAレベル、タンパク質レベルで検討した。Rspo3は、やせ型では食事摂食後に中心静脈域に収束する特徴を持つのに対し、肥満型ではこうした発現様式が減弱しているとともに、Rspo3の発現自体が減少していることがわかった。すなわち、肝臓においてRspo3の時空間的な調節は、肥満の病態では変調を来してしまい、肝臓の代謝に大きな影響をもたらすことが考えられた。
肝臓にRspo3導入の肥満モデルマウス、脂肪肝・糖尿病など改善し白色・褐色脂肪組織にも影響
そこで、肥満モデルマウスの肝臓にウイルスを用いてRspo3を導入すると、脂肪肝の改善のみならず、糖尿病の改善と肝臓・脂肪組織・骨格筋インスリン抵抗性の改善が見られた。また、遠隔臓器への特徴的な影響として、白色脂肪組織では脂肪細胞の縮小化とエネルギー消費に関わるUcp1の発現増加を認めたが、逆に褐色脂肪組織では脂肪細胞の増大化とUcp1の発現低下を認めた。
迷走神経肝臓枝の切断により、肝臓から白色脂肪組織への遠隔作用途絶
肥満の状態では、褐色脂肪組織でのエネルギー消費が亢進することで、さらなる肥満が進行しないようにする防御機構が働く。今回の結果は、過剰な刺激を受ける褐色脂肪組織を休ませ、新たに白色・褐色脂肪組織でのエネルギー消費の配分を再調節することで、体内の恒常性を保つように働いていることを示していると考えられる。そして、この肝臓から白色脂肪組織の縮小化という臓器をまたいだ遠隔作用は、肝臓と脳をつなぐ迷走神経肝臓枝を切断(Hepatic vagotomy:HV)することで見られなくなり、これはまさに肝臓由来の迷走神経を介した新しい臓器間神経ネットワーク機構が体内に存在していることを示している。
Rspo3欠損のモデルマウスは糖尿病・メタボリックシンドロームへ進展
次に、肝臓特異的にRspo3を欠損したモデルマウスでは、過剰発現モデルとは逆に、脂肪肝の進展と糖代謝の増悪、肝臓・脂肪組織・骨格筋インスリンシグナル減弱など、いわゆる糖尿病・メタボリックシンドロームの病態へ進展していることが認められた。
肝臓ゾネーションの調節と臓器間ネットワーク機構、治療応用への可能性に期待
Rspo3を介した肝臓ゾネーションの調節は、新しい臓器間ネットワークを構築し、全身の糖代謝と脂肪組織・骨格筋の質の制御を行うという生命現象が明らかになった。そして、Rspo3を用いて、肥満で変調した肝臓ゾネーションに再構築のスイッチを入れることが、臓器連携を介して糖尿病の改善、白色・褐色脂肪組織のエネルギー消費の再配分や、骨格筋の質向上という、全身の代謝恒常性の回復につながる可能性を示唆していた。
「糖尿病やメタボリックシンドローム、サルコペニアの患者が増加する高齢化の日本において、今回の研究で解明した肝臓ゾネーション由来の臓器間ネットワーク機構を選択的に制御することができれば、こうした疾患に対して有意義な治療応用への可能性を秘めていると期待される」と、研究グループは述べている。
▼関連リンク
・帝京大学 トピックス



