遺伝性がん病的バリアント、保有の判明でサーベイランス検査・予防的切除などの対策可能
東北大学は1月22日、東北メディカル・メガバンク(TMM)計画で取得した5万人のゲノム情報をもとに、遺伝性がん(遺伝性乳がん卵巣がん症候群:HBOC、リンチ症候群:LS)のリスク保有者97人にゲノム解析結果を返却したと発表した。この研究は、同大メディカル・メガバンク機構ゲノム予防医学分野の大根田絹子教授らの研究グループによるもの。研究成果は、「Journal of Human Genetics」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
遺伝性がんは、生まれたときから特定の遺伝子に特徴(病的バリアント)があることにより発症するがんの総称で、がん全体の約5~10%を占めると言われている。遺伝性がんの病的バリアント保有者は、非保有者に比べて若年から高い確率でがんを発症することが知られている。早期発見や予防のためのエビデンスが確立している病的バリアントを保有することがわかった場合には、定期的に詳しいがんの検査(サーベイランス検査)を行ったり、がんに罹りやすい器官を予防的に切除したりする診療が行われることがある。また、病的バリアントは親から子へ2分の1の確率で受け継がれるため、血縁者も遺伝カウンセリングを受けて、病的バリアントを持っているかどうか検査することができる。このような医療上の対策があるものについては、医療機関で実施する網羅的なゲノム検査において、診断・治療の対象以外の遺伝性がんの病的バリアントについても保有していることがわかった場合には、患者に結果を返却することが推奨されるようになってきた。
バイオバンクの参加者、遺伝性がんの病的バリアントを持つ場合も結果は知らされない
個人による遺伝子の特徴がどの程度病気の発症と関連しているかを正しく評価するためには、大規模な一般住民のゲノム情報が極めて重要であり、世界各国でその解析が進められている。また、そのために生体試料を集積するバイオバンクがゲノム医療の基盤として構築されている。日本では、TMM計画の参加者約15万人からなるバイオバンクがある。一般住民の全ゲノム解析情報をもとにした、DNA塩基配列の個人による相違の頻度の公開情報は、研究や医療に広く活用されている。
遺伝性がんの病的バリアントを持っていると、必ずがんに罹るわけではない。バイオバンクに協力しゲノム解析が行われた一般住民の中にも、遺伝性がんの病的バリアントを持っている人がいる。医療機関で行われるゲノム検査は、その患者の診断や治療を目的に実施され、対象としていた以外の遺伝子に病的バリアントが見つかった場合も、その病的バリアントに応じた医療上の対策が可能であることから、返却が推奨されている。一般住民の場合は状況が大きく異なり、バイオバンクに協力しゲノム解析が行われた人の多くは、自身が遺伝的にがんに罹りやすい体質であることを知らずに生活している。
バイオバンクに協力したことは、医療における措置を希望することとは異なるため、もし医療機関で返却が推奨されているのと同じ病的バリアントが見つかっても、その結果を直ちに返却するのではなく、その人が自身のゲノム情報を知りたいと考えているかどうかを確認する必要がある。また、予防や早期発見の機会が得られるという良い面ばかりではなく、医療費や通院の負担が生じることや、心理的・社会的にストレスを受ける可能性があることなど、ゲノム情報を知ることのネガティブな面も丁寧に説明した上で結果を返却し、サポートしていく必要がある。そのため、大規模な一般住民のゲノム情報を解析している研究機関やバイオバンクで、個人への結果返却を実施している例は、世界的にみてもほとんどない。
TMM参加者のうちHBOC・LSの病的バリアント保有者/一部の非保有者に結果返却希望を調査
TMM計画ではまずパイロットとして小規模な研究を3回実施し、今回の研究で初めて大規模なゲノム解析結果の返却に取り組んだ。なお、TMM計画ではこのゲノム解析結果の返却を「遺伝情報回付」として定義している。
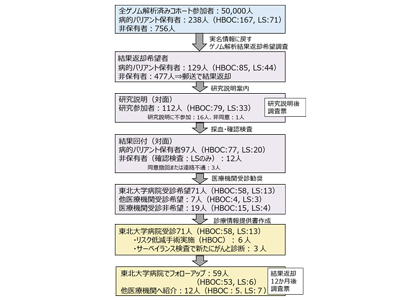
TMM計画のコホート調査に参加した一般住民約5万人の全ゲノム解析情報から、2つの遺伝性がん(HBOCとLS)の病的バリアント保有者238人(HBOC 167人、LS 71人)を抽出した。TMM計画では、コホート調査参加時に、将来健康にとって重要なゲノム情報を返却する予定があることを対面で説明している。そのため今回は、具体的な病名を明示せずに、病的バリアント保有者238人と非保有者の一部756人(ランダムに抽出)にゲノム情報の解析結果返却の希望調査を実施した。
病的バリアント保有者129人が返却を希望、研究参加の112人について確認検査を実施
病的バリアント保有者のみを調査の対象とすると、調査のお知らせ自体が病的バリアント保有を示唆する恐れがあったため、調査対象は非保有者を含めて幅広く設定した。その結果、病的バリアント保有者129人が返却を希望し、対面での研究説明を受けた112人(HBOC 79人、LS 33人)が研究に参加した。なお、非保有者のうち、結果返却を希望した477人には郵送で対象疾患の病的バリアントが見られなかったことを説明した。
研究参加者112人は対面で説明を受けた同日に採血し、病的バリアント保有部位の確認検査を実施した。確認検査の結果、全ゲノム解析情報から抽出したLSの病的バリアント保有者とされていた参加者のうち12人は病的バリアントを保有していないことがわかった。
6人でHBOCリスク低減手術実施、受診希望しない19人は通院や医療費負担など理由
後日対面で結果返却できた病的バリアント保有者97人(HBOC 77人、LS 20人)のうち、78人が医療機関の受診を希望した。このうち、71人が東北大学病院を受診し、サーベイランス検査を開始した。このうち、HBOCの病的バリアント保有者6人はリスク低減手術を受けた。また、HBOC 2人、LS 1人の病的バリアント保有者にはサーベイランス検査でがんが見つかった。
一方、受診しなかった19人は医療機関を受診する時間や労力、医療費の負担などを理由に、受診を希望しなかった。
ゲノム解析結果の返却が不安や心理的ストレスとなる人は限られることを示唆
研究参加時と結果返却1年後の2回(一部参加者には4回)、調査票による調査を実施し、99人から回答を得た。調査票では、これまでのパイロット研究で行っていた小規模な調査の結果を参考に、一般住民がゲノム解析結果返却を受けた後に生じる心理的ストレスや結果返却後の行動について、初めて統計学的に解析した。その結果、がんに対する不安の尺度(Cancer Worry Scale日本語版:CWS-J)は、がんに罹ったことがある人(28人)のほうが、未発症者(71人)に比べて高スコアであることがわかった。しかしながら、がんに罹ったことがあっても、非特異的な心理ストレス指標であるKessler 6(K6)スコアが低い人のCWS-Jスコアは、がんの既往のない人と同程度だった。このことから、一般住民集団において、がんの罹患経験が不安につながる程度には個人差があり、がんに対する不安の大きさは、より簡便で汎用されているK6スコアから推定できると考えられた。また、興味深いことに、研究説明後と結果返却1年後の2回の調査のスコアを比べたところ、CWS-J、K6ともに有意な変化は見られなかった。このことは、ゲノム解析結果の返却が不安やストレスの原因になる人は限られていることを示している。
HBOCバリアント保有者、女性・子の血縁者に対しゲノム解析結果伝える割合高いと判明
ゲノム解析結果返却のポジティブな点として、返却を受けた人だけでなく、その血縁者にも、医療上の対策を受ける機会が広がるという点がある。そこで、東北大学病院を受診したHBOCの病的バリアント保有者に、今回わかったゲノム解析の結果を血縁者に伝えているかどうか調査した。その結果、男性よりも女性、親より子の血縁者に対して、高い割合で伝えていることがわかった。このことは、返却を受けた人を介して、医療上の対策が同じリスクを有する血縁者にも広がる可能性を示している。
遺伝性がんリスクを一般住民へ伝える取り組み、個別化予防・医療に向け重要な先例
疾患の予防や医療をゲノム情報に基づき個別化して実施することが、今後予防および医療の標準になっていくことが予想される。2023年6月に成立されたゲノム医療推進法第13条では、ゲノム情報に係る試料提供者に対し、相談支援の適切な実施のための体制の整備を図るために必要な施策を講ずることが明記されている。
今回の研究は、研究のために取得したゲノム情報の提供者である一般住民に、個別に遺伝性がんのリスクがあることを伝えて、個別化予防・医療につなげた先駆的な取り組みである。今回の研究で実施したゲノム解析結果返却のプロトコルや、遺伝性がんについての理解度、がんに対する不安の尺度とその経時的変化、血縁者とのゲノム情報の共有について調査した結果は、研究や診療の場でゲノム解析結果を返却する体制を構築する上で貴重な先例となる。「今後は、遺伝性がん以外の遺伝性疾患や生活習慣病などの多因子疾患へと対象を広げることや、健康診断の一環として実施したゲノム情報の適切な返却方法の検討などを通じて、ゲノム情報に基づく個別化予防・医療を一般住民に広げる取り組みを継続していく」と、研究グループは述べている。
▼関連リンク
・東北大学 プレスリリース・研究成果



