さまざまな選択肢がある胃がん治療、患者の特性に応じた治療が求められている
理化学研究所(理研)は12月16日、胃がん患者一人ひとりのゲノム変異およびRNA発現データから腫瘍内の免疫活動の特徴を解析し、人工知能(AI)の一つの手法である機械学習を用いて、それぞれの化学療法の効果を予測することに成功したと発表した。この研究は、理研生命医科学研究センターがんゲノム研究チームの笹川翔太研究員、中川英刀チームリーダー、国立国際医療研究センターの山田康秀研究医療部長、国立がん研究センター中央病院頭頸部・食道内科の本間義崇医長、近畿大学医学部免疫学教室の垣見和宏主任教授らの研究グループによるもの。研究成果は、「Gastric Cancer」にオンライン掲載されている。
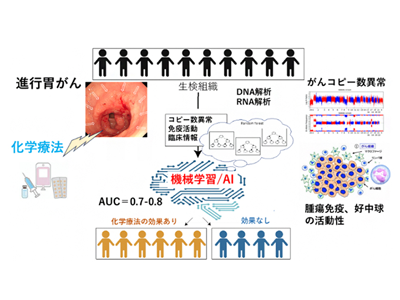
画像はリリースより
(詳細は▼関連リンクからご確認ください)
日本およびアジアでは、胃がんは依然として重要な健康課題だ。日本では胃がんの罹患率は、医療技術の向上やヘリコバクター・ピロリ菌の除菌治療の普及によって減少しつつあるが、いまだに国内のがんの中で罹患率が高く、2020年では10万9,679例が胃がんと診断され、2022年の胃がんによる死亡者数は4万711人だった。胃がん治療には、病期や患者の体調に応じてさまざまな選択肢が用意されている。早期発見された場合、内視鏡による低侵襲治療が有効だ。進行した胃がんに対しては、外科的切除が第一選択とされ、胃の一部または全摘出とリンパ節郭清(かくせい:切除)が行われる。また、手術後の再発予防や進行胃がんに対しては、薬物療法が治療の重要な柱となっている。
胃がんに対する薬物療法として、従来から使用されてきたプラチナ製剤(シスプラチンやオキサリプラチン)やフッ化ピリミジン系薬剤(S-1やカペシタビン)による化学療法に加えて、新たな分子標的薬や、免疫チェックポイント阻害剤(PD-1阻害薬)による免疫療法も導入されている。これにより、患者の特性に応じた個別化医療が進み、治療効果の向上が期待されている。特に進行胃がんの治療では、分子標的薬であるトラスツズマブが利用されており、トラスツズマブはがん細胞の増殖に関係するタンパク質HER2が陽性(HER2遺伝子が高発現またはコピー数増加)の胃がん患者に対して効果が期待できる。また、PD-1阻害薬であるニボルマブ(オプジーボ)やペムブロリズマブ(キイトルーダ)といった免疫チェックポイント阻害剤も、化学療法後の治療としての適応が拡大され、胃がんの薬物療法の新たな選択肢として期待を持たれている。術前や術後の補助化学療法も進歩しており、術後の再発リスクを抑えるためにプラチナ製剤とフッ化ピリミジン系薬剤の併用療法が標準治療とされている。
そこで今回の研究では、化学療法を受けた進行胃がんを対象として、ゲノム変異情報や、遺伝子発現から推測した免疫細胞の働きから、化学療法の効果を予測するアルゴリズムの開発を試みた。同様の研究手法は、以前に食道がんについて理研で行っている。
65例の進行胃がん組織を解析、実際の化学療法効果との関連を検討
研究グループは、国立がん研究センター中央病院において、プラチナ製剤とフッ化ピリミジン系薬剤の組み合わせを主とした化学療法の開始前に、内視鏡にて採取した65例の進行胃がん組織よりDNAとRNAを抽出した。そして、網羅的な全ゲノムシークエンス解析およびRNAシークエンス解析を行い、がん細胞やがん組織の遺伝子変異や遺伝子発現に関する情報を取得し、これらのデータと実際の化学療法の効果との関連を調べた。
driver遺伝子変異・薬剤代謝酵素の多型などは化学療法の効果と関連なし
胃がんのdriver遺伝子変異(発がんに関わる遺伝子変異)、薬剤代謝酵素の多型、MSI状態、EBVやピロリ菌感染をDNA情報より同定したが、実際の化学療法の効果とは関連が認められなかった。一方、全ゲノム解析の結果、がん細胞のコピー数異常における特定のパターンとの関連が認められた。
胃がん組織に浸潤する免疫細胞に着目、TANの多い群は化学療法の効果高いと判明
また、65例の胃がん組織のRNA発現解析の結果、492個の遺伝子発現が化学療法の効果と関連していることがわかった。そこで、遺伝子発現の傾向を調べるためにGSEAという解析を行ったところ、炎症関連のIFN-γやIL-6などのさまざまな遺伝子群の活性、つまりパスウェイ(遺伝子間の連続的な機能的連関)活性が、化学療法の効果が高い群で上昇していた。そして、がん細胞に対する免疫細胞の働きを遺伝子発現の程度から推測し、胃がん組織に浸潤している免疫細胞に着目することで、腫瘍内の好中球(TAN)、B細胞、CD8+T細胞、CD4+T細胞がそれぞれ多く発現する4つの群に分類できた。注目すべきことに、TANの多い群では他の群に比べて化学療法の効果が高く、TANの活動が化学療法の効果と機能的に関連していると考えられた。さらに興味深いことに、これは以前に報告した食道がんのTANの化学療法との相関とは逆の結果だった。
化学療法の効果予測アルゴリズムを機械学習で開発、診断の有用性示す精度を確認
次に、123項目のゲノム変異情報、コピー数異常、TANなどの腫瘍内の免疫情報、臨床情報を用いて、機械学習によって化学療法の効果を予測するアルゴリズムを開発した。内視鏡で組織を採取した65例のうち、45例(70%)のデータを学習セットに用いたところ、化学療法の効果に最も寄与する因子は、TANの活動とがん細胞のコピー数パターンであることがわかった。また、開発したアルゴリズムの予測精度を調べるために、残りの20例(30%)、および、中国にて行われた35例の臨床試験の公開データについても同様の解析を行った。その結果、診断法の有用性を示すAUC=0.7〜0.8(1に近いほど精度が高い)の値が得られ、高い予測精度の再現性が確認できた。
シングル細胞解析データから、抗腫瘍的もしくは親腫瘍的に働く種類のTANがあると判明
最後に、化学療法の効果と最も高い関連性が見られた腫瘍内に浸潤するTANに着目し、まず、胃がんと食道がん組織に浸潤している免疫細胞を抽出した。これらのシングル細胞解析を行い、5万9,584個の免疫細胞のRNA発現データから3,822個のTANのRNA発現データを抽出し、その特徴を調べた。これらTANを12個に分類することができ、そのうち、2つの分画は腫瘍の成長や転移を抑制して抗腫瘍的に働き、3つの分画は腫瘍の成長や転移を促進して親腫瘍的に働いていることがわかった。また、これら抗腫瘍的または親腫瘍的に働いているTANは、化学療法の反応性と胃がん患者の予後と関連していることも証明した。
他の腫瘍の化学療法効果予測・精密医療にも応用できる可能性
今回の研究により、胃がん組織のゲノム情報、免疫情報などのさまざまな情報を組み合わせることで、胃がんの化学療法の効果予測が可能であることが証明された。この研究手法は、胃がんのみならず他の腫瘍の化学療法の効果予測や精密医療にも応用できる可能性がある。
また、化学療法の効果に、腫瘍免疫、特にTANが密接に関連することがわかった。「胃がんに対する免疫細胞の活動についてさらに詳細な研究を進めることで、化学療法と免疫チェックポイント阻害剤の併用療法、または新しい複合免疫治療の開発が期待できる」と、研究グループは述べている。
▼関連リンク
・理化学研究所 プレスリリース



