交感神経の出力は全身性1種類の指令か、それとも個別の臓器ごとに制御されるのか
理化学研究所(理研)は12月10日、マウスを用いて、副腎と腸管の機能をそれぞれ制御する交感神経の異なるサブタイプが脊髄の中に存在することを発見したと発表した。この研究は、理研生命機能科学研究センター比較コネクトミクス研究チームの播磨有希子基礎科学特別研究員(研究当時)、宮道和成チームリーダーらの研究グループによるもの。研究成果は、「Nature Communications」にオンライン掲載されている。
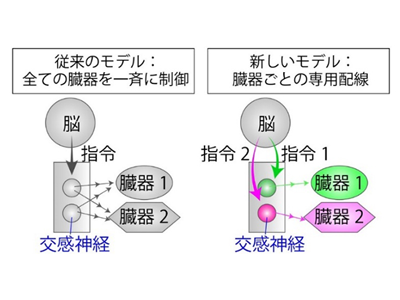
画像はリリースより
(詳細は▼関連リンクからご確認ください)
自律神経系は循環系、呼吸系、消化器系、生殖器系などさまざまな臓器を無意識に制御し、これらの機能を最適な状態に調節することで、外界の変化に適応し、生命を維持する重要な機能を担っている。
例えば、天敵に襲われた動物は、瞳孔が開き、全身の毛が逆立ち、心臓は激しく脈打ち、呼吸は浅く速くなるといった闘争・逃走反応と呼ばれる反応を示し、危機に対応する。米国の著名な生理学者ウォルター・キャノンは著書の中で、闘争・逃走反応とは交感神経を介して全身にエネルギーを供給する仕組みだと解説した。そして、「交感神経系は、体内環境の深刻な変化を防ぐために、迅速かつ直接的に作用し、身体のエネルギーを動員する役割を果たす。各種の交感神経の出力は一方向に同時に作用し、さまざまな臓器に及ぶように組織されている」と述べている。このようにキャノンは、交感神経の出力を1種類の全身性の指令として理解しており、この考え方は現在でも大きく修正されず受容されている。
一方で、交感神経の出力は個別の臓器あるいは臓器群ごとに、もっと細分化されているのではないかという考えも存在した。例えば、神経細胞同士の情報伝達に関与するさまざまな神経ペプチドや受容体遺伝子が交感神経に一様に発現するわけではなく、何らかのパターンがあることが見つかってきた。しかし、交感神経はどのように分類されるべきか、その分類がどのように臓器の制御と関連しているのか、という根本的な問題は未解決のままで現在に至っている。
1細胞RNA 解析による分類とウイルスベクターによる標識で交感神経を解析
研究グループは、交感神経の個別性と臓器制御の関連を解明するためには、遺伝学ツールの発達したマウスをモデルとする必要があると考えた。そこで、近年発表された遺伝子発現を網羅的に調べることのできる1細胞RNA sequence法による交感神経の分類を活用するとともに、ウイルスベクターを用いた神経細胞の標識技術を交感神経の研究に導入することにした。
腸管ぜん動運動を制御する腹腔神経節へはCartpt発現サブタイプの交感神経が軸索伸ばす
研究グループはまず、腸管のぜん動運動を制御する交感神経である腹腔・上腸間膜神経節(以下、腹腔神経節)に軸索の末端から細胞体へと逆行的に感染するウイルスベクターを導入することで、この神経節を制御している交感神経を特異的に標識する方法を確立した。標識された細胞は、脊髄の主に第8~13胸髄(下部胸髄)に存在した。組織化学的な手法を用いて、1細胞RNA sequence法による交感神経の分類結果と照合してみると、この神経節に軸索を伸ばす交感神経は、神経ペプチドを作るCartptという遺伝子マーカーを発現する特定のサブタイプに属することがわかった。
腹腔神経節のすぐ近くの副腎髄質へは別のOxtr遺伝子発現タイプが軸索を送ると判明
次に、ウイルスベクターを用いてCartptを発現する下部胸髄の交感神経を特異的に標識することができる実験系を確立した。軸索を標識して観察すると、Cartpt陽性の交感神経は予想通り腹腔神経節に軸索を接続したが、意外なことに、腹腔神経節のすぐ近くに存在する副腎髄質には全く軸索を送らなかった。
この結果を受けて、研究グループが副腎髄質に軸索を伸ばす交感神経を探索したところ、神経ホルモン・オキシトシンの受容体を作るOxtr遺伝子をマーカーとして発現する交感神経の一群が発見された。Oxtr陽性の交感神経を標識すると、その軸索は副腎髄質に存在し、腹腔神経節に全く存在しなかった。CartptあるいはOxtrを発現する交感神経は共に下部胸髄に存在するが、全く重なり合わない相異なる集団である。このように、下部胸髄の交感神経は、遺伝子発現により細分化が可能で、それぞれのサブタイプが互いに異なる軸索の接続先を持つことがわかった。
Cartpt発現交感神経の活性化でマウスの腸管通過時間を有意に延長
副腎髄質と腹腔神経節とが相異なる交感神経のサブタイプに支配されているという知見から、この両者を別々に制御することが可能だと考えられる。そこで研究グループは、OxtrあるいはCartptを発現する交感神経のいずれか一方だけを、薬理遺伝学と呼ばれる手法で任意の時期に活性化できるようにした。まず、腹腔神経節の支配を受ける腸管の機能に着目した。闘争・逃走反応では危機に対処するエネルギーを確保するため、緊急性の高くない消化機能は抑制されることが知られている。マウスに色素を食べさせてから着色便が排せつされるまでの時間を腸管通過時間と呼び、この時間が長いほど、腸通過に時間がかかることを示し、腸のぜん動運動が低下していることの指標となる。Oxtrを発現する交感神経を活性化させる前後で腸管通過時間に有意な違いはなかったが、Cartptを発現する交感神経を活性化させると、雌雄どちらのマウスも腸管通過時間が有意に延長した。この結果は、腹腔神経節を支配するCartpt陽性の交感神経が、実際に消化管のぜん動運動を抑制する機能を有することを示している。
Oxtr発現交感神経の活性化、雄マウスだけ顕著に血糖値上昇
闘争・逃走反応では危機に対応するエネルギー源として血糖値が上昇するが、副腎髄質はこの血糖値の上昇に寄与すると考えられている。そこで、交感神経のサブタイプを活性化させて血糖値を測定した。Cartptを発現する交感神経を活性化させても血糖値は変化しなかったが、Oxtrを発現する交感神経を活性化させると雄マウスだけ顕著な血糖値の上昇を示した。一方、雌マウスでは血糖値は変化しなかった。この雌雄差の生じる仕組みははっきりしていないが、先行研究では雄ラットの方がストレスによるアドレナリンの分泌量が多いことや、雌マウスの方がインスリンに対する感受性が高いことが知られている。これらのデータから、副腎髄質を支配するOxtr陽性の交感神経が血糖値の調整に関わるのに対して、腹腔神経節を支配するCartpt陽性の交感神経はこのプロセスに関与しない、という結論が得られた。
マウス糖質欠乏、Oxtr陽性交感神経は活動し副腎髄質を活性化するがCartpt陽性は不活性
研究グループは最後に、副腎髄質を支配するOxtr陽性交感神経と腸管機能を制御するCartpt陽性交感神経が実際に使い分けられるような状況があるのかを検討した。血糖値が急速に低下する状況は個体にとって深刻な危機で、交感神経は速やかに副腎髄質を活性化させて血糖値を回復させなくてはいけないが、その際に腸管の機能を低下させる必要性はなさそうである。むしろ、腸管機能を維持して消化・吸収を進めたほうが、長期的には血糖値の低下に抵抗できる可能性がある。
そこで、マウスに薬剤を注入して人為的に糖質の欠乏状態を誘導した。その結果、下部胸髄において、Oxtrを発現する交感神経には神経活動のマーカーであるc-Fos遺伝子の発現が誘導され、副腎髄質の活性化が起きていることがわかった。これに対して、Cartptを発現する交感神経はほとんどc-Fos遺伝子を発現せず、活性化されていないことがわかった。この結果は、糖質欠乏という危機に際して、副腎髄質を活性化しても交感神経が腸管機能を抑制しないことを示唆し、交感神経の出力はキャノンが考えたような1種類の全身性の指令ではなく、臓器レベルに細分化されている可能性を示している。そして、遺伝子発現によって個性を付けられた交感神経のサブタイプが、脳からの指令を特定の臓器に伝達する”専門家”として機能していると考えられる。
新しい概念を提案、臓器機能の不調を原因とする疾患の治療戦略にも貢献すると期待
今回の研究により、脊髄の交感神経を対象に、1細胞RNA sequenceデータを用いた神経細胞の分類やウイルスベクターによる精密な標識・神経活動の操作系が確立された。その結果、一方向に同時に作用すると考えられてきた交感神経に、分子レベルで規定される臓器ごとの専用配線の存在が見えてきた。ただし、Cartptを発現する交感神経の支配する腹腔神経節は、腸管以外にも肝臓、脾臓、膵臓などさまざまな臓器を制御しているといわれており、Cartpt陽性の交感神経がこれらをまとめて統括しているのか、さらなるサブタイプに分割されるのか、今後も研究が必要である。
基礎科学的には、交感神経による臓器ごとの専用配線があるという今回の発見が、眼や心臓も含めた全ての臓器・臓器群に対して一般に成り立つのか、それとも下部胸髄の担当する副腎髄質や腹腔神経節でのみ成立するのか、研究を進める必要がある。臓器ごとの専用配線がより一般的に成り立つのであれば、交感神経の出力を一種類の全身性の指令として理解してきたキャノン以来の神経生理学をメジャーアップデートする必要が出てくるだろう。その際、糖質欠乏に対する応答性がOxtrあるいはCartpt陽性の交感神経の間で大きく異なることは注目に値する。今後、さまざまなストレス条件においてどのような交感神経のサブタイプが活動するのかを網羅するような活動地図を作ることも必要だと思われる。
将来的には、さまざまな交感神経のサブタイプを特異的に操作することで、他の全身臓器に影響を与えずに特定の臓器機能だけを操作する技術が可能になるかもしれない。例えば、個別に脂肪を燃焼させたり代謝を高めたりといったことができれば、メタボリックシンドロームへの対策として有用性がある。「今回の研究で用いたサブタイプ特異的な交感神経の活性化手法は、遺伝子組換えを伴う薬理遺伝学の手法を用いているため直ちにヒトへと応用することはできない。しかし、交感神経サブタイプの機能やその遺伝子発現プロファイルの理解は、ヒトの臓器機能の不調を原因とする疾患の治療戦略に貢献するものである」と、研究グループは述べている。
▼関連リンク
・理化学研究所 プレスリリース




