CD30陽性PTCLに対するBVの効果は限定的で、治療抵抗性の克服が課題
北海道大学は12月9日、難治性の悪性リンパ腫「末梢性T細胞リンパ腫(peripheral T-cell lymphoma:PTCL)」の新規治療標的を解明したと発表した。この研究は、同大大学院医学院の須藤啓斗氏(博士課程4年)、中川雅夫助教らの研究グループによるもの。研究成果は、「Leukemia」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
PTCLは成熟T細胞に由来する悪性リンパ腫で、PTCL非特定型、ALK陽性未分化大細胞型リンパ腫(ALK+ ALCL)、成人T細胞性白血病/リンパ腫(ATLL)などの多様な病型を含む疾患である。PTCLはCD30を高率に発現することが知られており、CD30を標的とした抗体薬物複合体のブレンツキシマブベドチン(BV)は、初発ならびに再発・難治性のCD30陽性PTCLに対して広く用いられている。しかし、BVの奏功期間中央値(腫瘍奏効が最初に確認されてから、腫瘍進行が最初に確認されるまでの期間、または何らかの原因による死亡までの期間の中央値)は7~12か月とされており、治療抵抗性の克服が大きな課題となっている。これまで、どのような遺伝子がBVへの感受性に深く関与しているのかという点については、十分な検討がなされていなかった。
BV感受性規定する遺伝子、ゲノム編集用いてスクリーニング
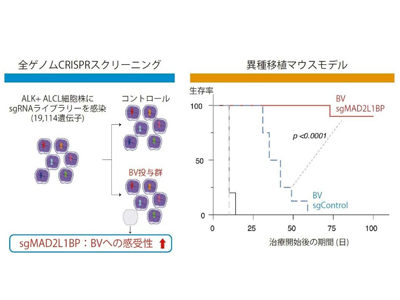
研究グループは、CD30陽性PTCLにおけるBVへの感受性を規定する遺伝子を同定するために、ゲノム編集技術であるCRISPR-Cas9をALK+ ALCL細胞株に用いることで、一度に約2万種類の遺伝子を網羅的にノックアウトさせ、ゲノムワイドなスクリーニングを施行した。
具体的な方法として、1万9,114種類の遺伝子に対する単鎖ガイドRNA(sgRNA)をALK+ ALCL細胞株に導入し、遺伝子ノックアウトを行った後、BV投与群とコントロール群に分けて培養を行った。次に、生存したALK+ ALCL細胞株のゲノムDNAを抽出し、ゲノムDNA上のsgRNA配列をPCRで増幅、次世代シークエンサーで検出した。そして、計測されたsgRNA数から、どの遺伝子がBVへの感受性亢進ならびに抵抗性に重要な役割を担っているのかを検討した。
有糸分裂チェックポイント複合体阻害因子の関与判明、APC/C阻害薬併用で相乗効果
スクリーニングの結果、有糸分裂チェックポイント複合体(MCC)の阻害因子であるMAD2L1 binding protein(MAD2L1BP)とanaphase promoting complex subunit 15(ANAPC15)がBVへの感受性亢進に関与していることを見出した。実際に、ALK+ ALCL細胞株ならびにATLL細胞株でこれらの分子をノックアウトさせることで、BVによる細胞毒性が増強することを確認した。さらに、ALK+ ALCL細胞株を用いた異種移植マウスモデルでも、MAD2L1BPをノックアウトすることでBVの抗腫瘍効果が増強することを明らかにした。また、BVとAPC/C阻害薬のproTAMEを併用することで細胞周期の停止を誘導し、相乗的な細胞傷害作用を示すことも見出した。
BV抵抗性に関与のSLC39A7発見、ノックアウトでCD30成熟障害され発現低下
一方、研究グループは今回のスクリーニングから、solute carrier family 39 member 7(SLC39A7)がBVへの抵抗性に関与していることも突き止めた。ALK+ ALCL細胞株ならびにATLL細胞株でSLC39A7をノックアウトさせると、CD30の成熟が障害され、CD30の細胞表面発現量が低下することで、BVへの抵抗性となることを示した。
今回の研究では、ゲノムワイドのCRISPR-Cas9ライブラリースクリーニングを用いて、CD30陽性PTCLにおけるBVへの感受性規定因子に関して、感受性亢進・抵抗性の両面について重要な遺伝子を同定した。「特に、APC/C阻害薬のproTAMEとBVを併用することで相乗的な細胞毒性を示すことを明らかにし、MCC-APC/Cを軸とした新規治療標的がBVの感受性増強や抵抗性克服に重要である可能性を突き止めた。PTCLの予後改善に向けた今後の臨床応用が期待される」と、研究グループは述べている。
▼関連リンク
・北海道大学 プレスリリース



