現行の遺伝子解析技術でも診断率低いミトコンドリア病、リピート異常伸長に着目
順天堂大学は10月25日、ミトコンドリア病を引き起こす、新たなリピート配列(GGGCCの塩基の繰り返し配列)の異常伸長を発見したと発表した。この研究は、同大大学院難治性疾患診断・治療学/難病の診断と治療研究センターの岡﨑康司センター長・教授(理研応用ゲノム解析技術研究チーム チームリーダー)、八塚由紀子助教、理化学研究所(理研)生命医科学研究センター応用ゲノム解析技術研究チームの尾崎心副チームリーダー(研究当時、現 客員主管研究員)、千葉県こども病院代謝科の村山圭部長(研究当時、現 順天堂大学大学院難治性疾患診断・治療学教授)、埼玉医科大学小児科学・ゲノム医療学の大竹明客員教授・名誉教授らの研究グループによるもの。研究成果は、「npj Genomic Medicine」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ミトコンドリア病は厚生労働省の定める指定難病の一つであり、筋肉や脳・心臓を中心に全身のあらゆる臓器に症状を起こし得る疾患群である。現在は根本的治療方法がなく、5,000人の出生に1人という、比較的頻度の高い遺伝性疾患群でもある。その未診断率は6~7割にも達し、現行の遺伝子解析技術を用いても診断できない患者が多くいることが課題である。これまで425個以上の遺伝子(細胞核にあるゲノムまたは、ミトコンドリア内にあるミトコンドリアゲノムに位置する)の異常によりミトコンドリア病を引き起こし得るとされてきた。その多くは一塩基のバリアントや短い挿入・欠失をもたらすバリアント、あるいはまれに構造多型と呼ばれるバリアントであることがわかっている。また、症例は少ないものの、リピート配列と呼ばれる、短い数塩基の配列の繰り返しから成る塩基配列が異常に長くなること(異常伸長)によって、そのリピート配列を保有する遺伝子の機能が障害されたり、毒性のあるタンパク質が生成されたりすることでミトコンドリア機能障害につながることが知られている。
別の観点から、リピート配列の異常伸長によるヒトの疾患(リピート病)は全てを合わせるとこれまで50余りが報告されており、多くは神経に障害を呈することがわかっている。これらのリピート病では数百塩基から数千塩基にも及ぶ長い繰り返し配列が患者検体に見られるが、それを正確に解析するには特別な遺伝子解析装置であるロングリードシーケンサーが有効であるといわれている。
NAXE遺伝子発現が著しく低下している症例を発見
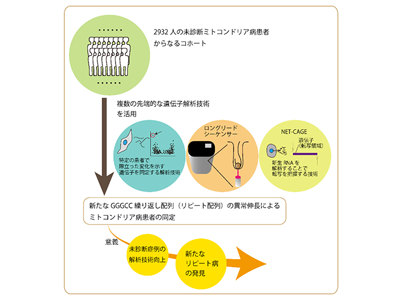
今回の研究では、ロングリードシーケンサーなど複数の技術を駆使して、ミトコンドリア病の原因となる新たなリピート異常伸長の同定を目指した。
研究グループは、2,932人の未診断ミトコンドリア病患者の国内コホートにおいて、それぞれの患者で病気の原因となる遺伝子変化を突き止める研究を進めていた。その過程で、2,932人のうち400人について、皮膚線維芽細胞から抽出したRNAの配列決定および定量解析を行ったデータの評価を行った。評価には、「OUTRIDER」という、集団の中でも際立って異常な遺伝子発現をしている個体を検出するプログラムを用いた。その結果、1症例でNAD(P)HX epimerase(NAXE)と呼ばれる遺伝子の発現が著しく低下していることを発見した。また、NAXE遺伝子の産物であるNAXEタンパク質の量も顕著に減少していた。しかし、同症例で全ゲノムシーケンシングを行ったが、そのようなバリアントは検出されなかった。
ロングリード解析でNAXEのプロモーター領域に200回のGGGCC繰り返しを検出
次に、長い配列を一気に読み取ることができるロングリードシーケンサーを用いてゲノム配列を解析した。その結果、この症例の患者ではNAXE遺伝子のプロモーター領域と呼ばれる転写の開始を制御する配列の中に、GGGCCの5塩基の繰り返し単位が正常では3~5回の繰り返しをしているところが、この症例では約200回も繰り返し、異常伸長していることがわかった。
さらに、理研が開発した、新しく転写され合成されたばかりのRNA(新生RNA鎖)を検出する技術(NET-CAGE:Native Elongating Transcript-Cap Analysis of Gene Expression)を用いて解析した。その結果、異常伸長しているNAXE遺伝子では転写される活性が著しく低下していた。このことから、プロモーター領域に存在するリピート配列の異常伸長により、NAXE遺伝子の転写が抑制されている状態であることが推定された。
GGGCCリピート伸長、NAXE遺伝子プロモーター領域のCpGメチル化亢進し機能喪失
また、ゲノムDNAのシトシン(C)がメチル化(メチル基が付加される化学的修飾)された状態となるCpGメチル化は、遺伝子の発現を抑制する方向に働く。ロングリードシーケンサーのデータを解析したところ、異常伸長しているNAXE遺伝子のプロモーター領域やその周辺では、CpGメチル化が亢進した状態であることがわかった。
以上のことから、今回、共同研究グループが発見したGGGCCのリピートの異常伸長が、NAXE遺伝子のプロモーター領域において、CpGメチル化の亢進を伴い遺伝子の発現を抑制していることがわかった。それによりNAXE遺伝子の産物(RNAとタンパク質)が著しく減少し、NAXE遺伝子の機能が喪失した状態になることで、ミトコンドリア機能障害が生じ、NAXE関連脳症を引き起こしていると考えられた。
GGGCCを繰り返し単位とするリピート異常伸長によるヒト疾患の病態解明は今回の研究が初めての報告となる。
同様の取り組みで未診断症例の診断推進につながると期待
今回の研究では、依然として多くの未診断ミトコンドリア病患者がいる状況で、複数の先端的な遺伝子解析技術を組み合わせることで、ミトコンドリア病の一種の原因となる遺伝子変化を同定し、これまで診断困難であった患者を分子診断することに成功した。このことから、同様の取り組みにより、未診断症例の診断を推進できることが期待される。
リピート病研究にも重要な知見となる可能性
同時に、近年注目を浴びているリピート病の観点においては、今回の研究はリピート配列としてGGGCCがヒト疾患の原因となり得ることを初めて明らかにした。このため、同様のGGGCCリピート配列を持つ遺伝子が潜在的にミトコンドリア病以外の遺伝性疾患につながる可能性を示唆している。ヒトゲノムの数割以上は繰り返し配列から成っている。このため、リピート病の研究成果はそれ以外の分野にも大きな影響のある知見を与えることが知られている。「今回の研究も、このようなリピート病研究を加速する知見をもたらすものと考えられる」と、研究グループは述べている。
▼関連リンク
・順天堂大学 ニュース&イベント



