大豆タンパク質β-CGの循環器疾患への効果は?
名古屋大学は10月16日、機能性大豆タンパク質であるβ-コングリシニン(β-CG)をタンパク質源とした餌を心不全モデルマウスに投与することで、いくつかの短鎖脂肪酸を産生する菌および主要短鎖脂肪酸(酢酸・酪酸・プロピオン酸)を増加させ、心機能低下・心肥大・心筋の線維化といった心不全の病態進行を抑制することを新たに発見したと発表した。この研究は、同大大学院医学系研究科 総合保健学専攻 オミックス医療科学の古川希助教、医学系研究科 神経遺伝情報学 伊藤美佳子講師、医学系研究科 総合保健学専攻 オミックス医療科学 上山純准教授の研究グループと、中部大学生命健康科学部・平山正昭教授、名古屋学芸大学管理栄養学部・大野欽司教授との共同研究によるもの。研究成果は、「Clinical Nutrition」に掲載されている。
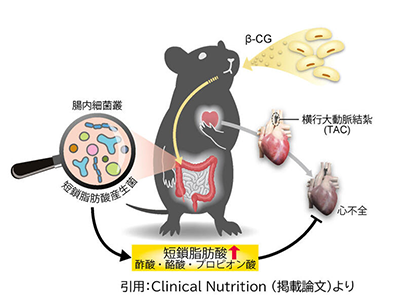
画像はリリースより
(詳細は▼関連リンクからご確認ください)
心不全は予後不良の難治性疾患で、高血圧など生活習慣病を基盤とした病的心ストレスが生じると、その負荷を代償しようと心筋の壁が厚くなり心肥大を呈し、さらに病態が進展すると収縮・拡張能が共に破綻した慢性心不全へと至る。
大豆やその成分は抗酸化・抗炎症機能を有し、心血管傷害から保護する作用がある。β-CGは抗肥満効果を示す機能性大豆成分であることが知られているが、循環器疾患への効果、特に心肥大-心不全の病態進行に関与するかについては明らかになっていない。
β-CGをタンパク質源とした餌で、心不全モデルマウスの心機能低下を抑制
研究グループが、β-CGをタンパク質源とした餌を圧負荷心不全(TAC)モデルの作成前後5週間摂食させたところ、圧負荷によって起こる左室リモデリング(心機能低下・心肥大・心筋線維化)がコントロール餌摂食群と比較して著明に抑制された。
餌摂食によるリモデリング抑制効果を示したため、腸内細菌叢に焦点を当て16S rRNA-seq・GC-MSによる腸内細菌叢・代謝産物の解析を行った結果、β-CG餌摂食により腸内細菌叢におけるいくつかの短鎖脂肪酸産生菌(genera Butyricimonas, Marvinbryantia, and Anaerotruncus)および主要短鎖脂肪酸が増加すること、β-CG餌で増加した一部短鎖脂肪酸産生菌の存在量は心筋線維化(%)と逆相関を示すことがわかり、短鎖脂肪酸が同病態に直接介入する可能性を見出した。
腸内細菌叢を介した心保護効果であることが判明
また、プロピオン酸ナトリウム投与でもβCG餌摂食時と同様に左室リモデリングを抑制すること、腸内細菌叢の効果を消失するための抗菌薬投与実験では、β-CG餌摂食によって増加した上記短鎖脂肪酸産生菌および短鎖脂肪酸は消失し、心保護効果もキャンセルされることから腸内細菌叢を介した心保護効果であることを解明した。
腸と心臓との臓器連関による新規心不全予防・治療法の開発を目指す
今回の研究で重要なことは、β-CGが腸内細菌叢の変化に介入し心保護効果を示している点にあると研究グループは指摘。β-CGは難消化性であること、また、オリゴマンノース型の糖鎖を多く含む糖タンパクであることが知られている。
同研究は、β-CGが近年注目されている有益な腸内細菌叢代謝産物である短鎖脂肪酸およびその産生菌を増加させ、短鎖脂肪酸の投与自体も左室リモデリング抑制効果を示すことを解明した。しかし大豆は高アレルゲンであり、全ての人に同様の効果を示すわけではない。
「今後の研究展開として、β-CGの難消化性・β-CG内糖鎖に注目し、糖鎖を消化・分解されずに腸管まで到達させることで、腸内細菌叢にて短鎖脂肪酸およびその産生菌増加につながるか、より詳細な分子メカニズムを究明し、腸と心臓との臓器連関による新規心不全予防・治療法の開発を目指す」と、研究グループは述べている。
▼関連リンク
・名古屋大学 プレスリリース



