ベムラフェニブの薬剤耐性を克服する効果的なアプローチは未確立
理化学研究所(理研)は9月6日、マウスモデルを使った実験により、抗がん剤に対する耐性を持ったがん細胞変異によって生じた免疫原性の高いネオ抗原は、通常のがん細胞に生じるネオ抗原よりも、免疫系に認識されやすい機能性が促進されていることを明らかにしたと発表した。この研究は、理研生命医科学研究センター免疫細胞治療研究チームの岡田匡央研究員(研究当時)、山﨑哲研究員、清水佳奈子上級研究員、藤井眞一郎チームリーダー(最先端研究プラットフォーム連携(TRIP)事業本部創薬・医療技術基盤プログラム副プログラムディレクター)らの研究グループによるもの。研究成果は、「Cancer Research」にオンライン掲載されている。
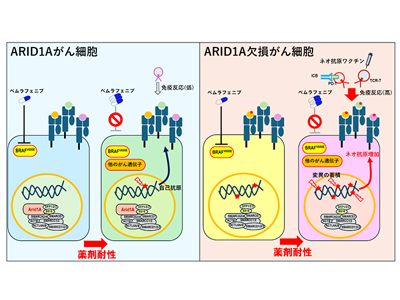
画像はリリースより
(詳細は▼関連リンクからご確認ください)
BRAFの持続的活性変異は、しばしば黒色腫や大腸がんにおける腫瘍形成の主な原因となる。中でも典型的なBRAFV600E変異は、最も頻度の高い発がん性変異であり、調節不能なマイトジェン活性化プロテインキナーゼ(MAPK)増殖シグナルを引き起こす。この変異に対する選択的阻害剤であるベムラフェニブなどの抗がん剤は、進行期の悪性黒色腫(メラノーマ)の有効な治療法として、多くの患者の生存期間を延ばしたが、メラノーマは薬剤耐性を獲得し再発することが知られている。さまざまな耐性メカニズムが臨床および実験結果によって同定されているが、耐性を克服する効果的なアプローチはいまだ確立されていない。
抗PD-1抗体の投与に代表される免疫チェックポイント阻害剤(ICB)療法は、T細胞の抑制シグナルをブロックし、腫瘍を標的とするT細胞を再活性化する。一方、腫瘍の体細胞変異に由来するネオ抗原は、がん細胞特異的に発現し、非自己としてT細胞の免疫標的になるため、多くの臨床研究においてネオ抗原の数とICB療法の効果に相関があることが明らかになっている。
BRAF阻害剤耐性の細胞株における、ARID1A発現の免疫への関与を検証
ARID1A(AT-rich interactive domain 1a)は腫瘍抑制因子と見なされている。このため、ARID1Aの欠損が腫瘍を変化しやすくし、ICB療法に対する効果に関与していると考えられている。ARID1Aの欠損と腫瘍免疫療法の臨床結果を結び付けるメカニズムを理解することは、ARID1A変異腫瘍患者におけるICB療法の正確な予測につながり、また難治性の腫瘍に対する代替治療法の開発にも役立つと期待できる。
研究グループは今回、メラノーマの代表的治療薬であるBRAF阻害剤に対してがん細胞が耐性になった場合において、遺伝子ARID1Aの発現に焦点を当てた免疫効果を研究した。第1に、BRAFV600E変異株を樹立し、さらにARID1A欠損株と、それぞれに対するBRAFV600E阻害剤であるベムラフェニブ耐性株を樹立した。第2に、ARID1A欠損と薬剤耐性が抗PD-1抗体治療による抗腫瘍免疫応答に及ぼす影響を検討した。第3に、薬剤耐性の間に新しく生成されたネオ抗原がワクチンによる免疫療法の標的として利用できるかどうかを検証した。
薬剤耐性ARID1A欠損株、抗PD-1抗体投与で持続的な抗腫瘍効果示す
研究グループはまず、hBRAFV600E改変マウスからBRAFV600E変異メラノーマ(以下、親株)を樹立し、ゲノム編集によるARID1A欠損BRAFV600E変異メラノーマ(以下、ARID1A欠損株)を作製した。これらの細胞をARID1A抗体とGAPDH抗体を用いて処理し、ウエスタンブロット解析を行ったところ、親株およびARID1A欠損株では、実際にARID1Aの欠損を確認し、in vitro(試験管内)ではベムラフェニブに対して同様の感受性を示した。さらに、親株およびARID1A欠損株を5μMのベムラフェニブを含む培地で8週間培養することで、親株およびARID1A欠損株メラノーマのBRAF阻害剤耐性(薬剤耐性)がん細胞を樹立した。
次に、樹立した親株、薬剤耐性株、ARID1A欠損株、薬剤耐性ARID1A欠損株をマウスに投与した結果、ARID1A欠損株、薬剤耐性ARID1A欠損株の腫瘍増殖は、それぞれ親株、薬剤耐性株よりも速く増殖したことから、ARID1Aの腫瘍抑制的な役割が示唆された。興味深いことに、抗PD-1抗体投与による持続的な抗腫瘍効果は、薬剤耐性ARID1A欠損株では観察されたが、薬剤耐性株では観察されなかった。また腫瘍浸潤リンパ球のフローサイトメトリー解析から、薬剤耐性ARID1A欠損株は抗PD-1抗体の投与によりIFN-γおよびTNF-α産生CD8+T細胞が増加することが示された。
ARID1A欠損株などと比較し、薬剤耐性ARID1A欠損株では高い免疫原性
さらに、これら4種類の腫瘍の免疫原性(免疫の抗原の強さの程度)を比較した。100Gyの放射線照射により不活化したがん細胞を静脈注射したマウスから、がん細胞投与後7日目に脾臓を回収しCD8+T細胞を分離し、抗原特異的CD8+T細胞の誘導をELISpotアッセイで解析した。刺激には、がん細胞と免疫反応を増強するPoly(I:C)を投与したマウス由来の樹状細胞を用いた。その結果、薬剤耐性ARID1A欠損株を投与したマウスのサイトカインIFN-γ産生CD8+T細胞数が、他の3群よりも多いことが示された。すなわち、薬剤耐性ARID1A欠損株は、親株やARID1A欠損株と比較して高い免疫原性を示すことが明らかになった。
薬剤耐性ARID1A欠損株の免疫原性ネオ抗原を同定
ARID1Aの欠損は、患者のARID1A非変異腫瘍と比較して体細胞突然変異の蓄積を促進する。薬剤耐性を獲得した後のDNA変異について調べ、薬剤耐性ARID1A欠損株における特異的なミスセンス変異の増加が明らかになった。これらのミスセンス変異における潜在的なネオ抗原を解析するため、変異ペプチド配列を調べるとともに、クラスI分子(H-2KbとH-2Db)との親和性を予測した。その結果、高い親和性が予測されるネオ抗原は薬剤耐性ARID1A欠損株に集中し、がん細胞特有のネオ抗原の数も薬剤耐性ARID1A欠損株で最も多いことがわかった。
また、薬剤耐性ARID1A欠損株の免疫原性ネオ抗原を特定し、選択するため、18個の変異ペプチドを合成し、スクリーニングにより薬剤耐性ARID1A欠損株特異的な免疫原性変異ペプチドを同定した。この変異ペプチドによる免疫応答について、変異ペプチドを投与したマウスの脾臓細胞をin vitroで再刺激し、CD4+T細胞およびCD8+T細胞の活性化をサイトカイン(IFN-γ、TNF-α)の産生と活性化マーカー(PD-1、CD137)の発現で評価した。その結果、薬剤耐性ARID1A欠損株特異的な免疫原性ネオ抗原が変異特異的な免疫応答を誘導することが示された。
薬剤耐性特異的ネオ抗原のワクチン、接種マウスにおいて抗腫瘍効果を確認
最後に、薬剤耐性ARID1A欠損株に新たに出現した免疫原性ネオ抗原がワクチン接種によって治療効果をもたらすかどうかを検討した。薬剤耐性ARID1A欠損株を皮下注射したマウスに、薬剤耐性特異的ネオ抗原ワクチンを腫瘍投与後7、14日目の2回投与した。抗PD-1抗体との併用療法では、抗PD-1抗体を腫瘍投与後7、10、13、16日目の4回投与した。無処置のマウスと比較して薬剤耐性特異的ネオ抗原ワクチンを接種したマウスで腫瘍サイズの縮小が観察され、薬剤耐性特異的ネオ抗原ワクチンと抗PD-1抗体併用療法のマウスではより高い抗腫瘍効果が確認された。この結果と一致して、無処置のマウスと比較して薬剤耐性特異的ネオ抗原ワクチン接種のマウスで生存期間が延びており、併用療法のマウスではより生存期間が延びた。以上の結果から、薬剤耐性ARID1A欠損株に新たに出現した薬剤耐性特異的ネオ抗原は、ワクチンによる抗腫瘍反応を誘導することが示唆された。
薬剤耐性後のネオ抗原を用いた免疫療法、難治性腫瘍の治療法として有望
今回の研究において、薬剤耐性ARID1A欠損株で抗PD-1抗体治療による抗腫瘍免疫応答が増強されることを観察した。また薬剤耐性獲得の間に蓄積した体細胞変異に由来するネオ抗原は、ARID1A欠損株で高発現し、腫瘍の免疫原性を促進することを明らかにした。そして、これらの新しく生成されたネオ抗原がワクチンによる免疫療法の標的として利用できる可能性が示された。「薬剤耐性後に新たに出現したネオ抗原を用いた免疫療法は、難治性腫瘍の有望な治療法になり得ると期待できる」と、研究グループは述べている。
▼関連リンク
・理化学研究所 プレスリリース



