ICU-AWはOOL低下の要因、特効薬はなく支持療法や栄養管理
三重大学は9月3日、重症敗血症の治療後に起こるICU関連筋力低下(ICU-AW)のメカニズムに関して、プログラム細胞死タンパク質1(PD-1)と、筋肉内に存在する免疫細胞のうち、2型自然リンパ球(ILC2)が産生するインターロイキン13(IL-13)が、敗血症後の筋力維持に果たす役割を明らかにしたと発表した。この研究は、同大大学院医学系研究科の赤間悠一医師、朴恩正准教授、島岡要教授らの研究グループによるもの。研究成果は、「Journal of Cachexia, Sarcopenia and Muscle」に掲載されている。
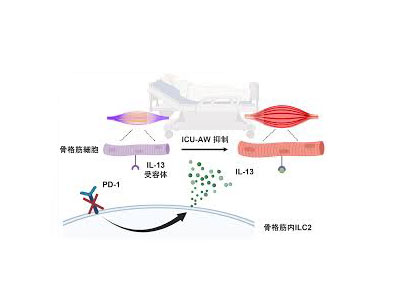
画像はリリースより
(詳細は▼関連リンクからご確認ください)
重症敗血症の治療後、患者が直面する最も深刻な問題の一つがICU-AWである。これは、長期的な骨格筋機能の低下を伴う疾患群であり、敗血症治療後の生活の質を著しく低下させる要因となる。しかし、ICU-AWに対する特効薬は現在のところなく、主に支持療法や栄養管理に頼っている。この問題を解決するために、ICU-AWの病態生理学的メカニズムを解明し、新しい治療戦略を模索することが求められている。
PD-1欠損マウスモデル、敗血症後でも筋力と筋重量を維持
研究グループは、敗血症によるICU-AWのメカニズムを解明するために、PD-1欠損マウスを使用した。敗血症を誘導した後、野生型マウスでは長期的な筋力低下を認めたが、PD-1欠損マウスでは筋力と筋重量が維持され、筋力低下が防がれていることを確認した。
この結果を受けて、敗血症後のそれぞれのマウスにおける筋タンパク質合成の機能を評価するため、筋肉を構成する主要なタンパク質の骨格筋内メッセンジャーRNA(mRNA)発現量を評価した。野生型マウスでは敗血症誘導後、長期的に遅筋線維関連遺伝子のmRNAが低下していたのに対し、驚くべきことに、PD-1欠損マウスでは、これらの発現が維持または増加しており、筋保護機能への関与が考えられた。実際に骨格筋断面積を詳しく調べてみると、PD-1が欠損しているマウスでは遅筋断面積が保たれていることがわかった。
PD-1欠損における筋力維持にはILC2由来のIL-13が関与
IL-13は筋肉のホメオスタシスを保っていることがこれまでの研究で示されていた。IL-13が敗血症における遅筋保護に重要な役割があると予想し、骨格筋の細胞株を用いた細胞実験で、敗血症を模してリポポリサッカライド(LPS)処理すると、野生型マウスでの結果と同様に遅筋関連遺伝子のmRNA発現量は減少したが、IL-13投与によってmRNA発現の低下は回復した。このことから、IL-13投与は敗血症で低下した遅筋の合成作用を少なくとも部分的には改善させることがわかった。
次に、骨格筋内ではT細胞と比較してILC2の方が、IL-13産生能が高く、ILC2が主要なIL-13産生細胞であることを確認した。最後に、野生型マウスに比べPD-1欠損マウスの筋肉内では、ILC2によるIL-13の産生量が増加していることも確認した。これらのことから、PD-1欠損における筋力維持にはILC2由来のIL-13が関与していることが明らかとなった。
「PD-1阻害剤はすでにがん治療において広く使用されているが、研究成果は、PD-1阻害剤が敗血症患者に対するICU-AWの新たな治療法となる可能性を示唆している。PD-1がICU-AWにおける筋力低下に重要な役割を果たしていることが明らかになり、PD-1を標的とした新しい治療戦略の開発が期待される」と、研究グループは述べている。
▼関連リンク
・三重大学 プレスリリース



