SLEで引き起こされるループス腎炎、臓器炎症誘発とILCの関連を解析
札幌医科大学は8月19日、ループス腎炎における臓器炎症の重症化に自然リンパ球(ILC:Innate Lymphoid Cell)が関与していることを世界で初めて明らかにしたと発表した。この研究は、同大医学部免疫・リウマチ内科学の神田真聡講師、ドイツシャリテ大学、マックスデュルブリックセンター、ドイツリウマチセンターらの研究グループによるもの。研究成果は、「Nature」にオンライン掲載されている。
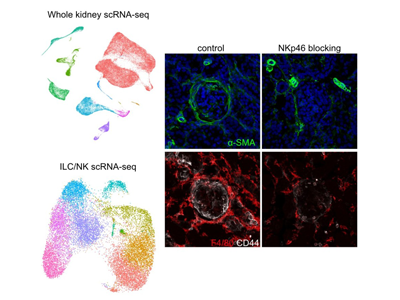
画像はリリースより
(詳細は▼関連リンクからご確認ください)
全身性エリテマトーデス(SLE)は主に妊娠可能年齢の女性が罹患する自己免疫疾患の一つであり、種々の臓器にさまざまな重症度の臓器障害を起こす。中でもループス腎炎と呼ばれるSLEによる腎障害はSLEの予後を規定する重篤な臓器病変の一つとされている。SLE患者のかなりの割合がループス腎炎を起こす一方で、その重症度は個々の患者により異なり、ほとんど治療を要さない軽症例から透析や腎移植を要する末期腎不全を起こすループス腎炎まで幅広いことが知られている。この差がどのようなメカニズムにより起こっているかはこれまでわかっていなかった。ループス腎炎の発症には抗DNA抗体をはじめとする自己抗体の産生が重要とされ、それが臓器障害を起こしているとされていることから、臓器炎症の重症化も主に獲得免疫が担っていると考えられてきた。
ILCは免疫担当細胞の一種だが、循環血液中に占める割合は極めて少なく、腸管や皮膚などの病原体の侵入にかかわる組織・臓器に特徴的に存在することが知られている。腸管などでは臓器炎症誘発においてILCが重要な役割を果たしていることがわかっていたが、これまで腎炎とILCの関わりについては検討されていなかった。そこで研究グループはILCがループス腎炎の臓器炎症にどのようにかかわるかについて検討した。
複数のループス腎炎モデルにおいて、腎組織内でILCの増加を確認
研究グループはまず、複数のループス腎炎モデル(poly(I:C)投与NZB/W F1マウス、イミキモド誘発ループスモデルマウス、B6.Sle1Yaaマウス)に対して、腎組織内・血管内細胞を分けてその割合の変化をフローサイトメトリーで解析した。その結果、ループス腎炎モデルにおいて、腎組織内でILC(主にILC1)が増加することを示した。
抗IFNAR1抗体、抗アシアロGM1抗体、抗NKp46抗体で、腎機能障害が改善
次に、ループス腎炎モデルに対して、抗IFNAR1抗体(I型インターフェロン刺激阻害)、抗アシアロGM1抗体(ILC/NK細胞除去)、抗NKp46抗体(NKp46刺激阻害)、抗GM-CSF抗体、抗CSF1R抗体を投与し、腎組織内の炎症の状態をフローサイトメトリーおよび蛍光免疫染色で評価した。また、イミキモド誘発ループスモデルとB6.Sle1Yaaマウスのループス腎炎モデルにおいて、それぞれNcr1、Trem2を遺伝子編集して、腎組織内の炎症の状態をフローサイトメトリーおよび蛍光免疫染色で評価した。加えて、poly(I:C)投与NZB/W F1マウスにおけるループス腎炎発症過程、NK細胞・ILC、抗アシアロGM1抗体投与によりおこるトランスクリプトーム変化をシングルセル解析で評価した。
その結果、抗IFNAR1抗体、抗アシアロGM1抗体、抗NKp46抗体により、腎組織内ILCの増加が抑制され、腎機能障害が改善した。この介入では自己抗体産生(抗DNA抗体の産生量)に変化は生じなかった。シングルセル解析により腎組織内のILCの中にNKp46の刺激を受けて活性化し、GM-CSFを特徴的に産生する集団を同定した。また、抗NKp46抗体、抗GM-CSF抗体、抗CSF1R抗体の投与およびNcr1ノックアウトにより腎組織内の単球由来炎症性マクロファージが減少すること、腎炎による腎障害が抑制されることを示した。シングルセル解析の結果からループス腎炎モデルにおいてTrem2陽性マクロファージが特徴的に増加していることを示した。しかしTrem2ノックアウトでは腎炎による腎障害を悪化させた。
さらに、既報のヒトループス腎炎のシングルセル解析においてILCが存在するかどうかについて再解析を行ったところ、ILCはヒトループス腎炎でも存在することを示した。
ILCを標的としたループス腎炎の新規治療法開発につながる可能性
今回の研究によりループス腎炎の重症化の機序が明らかとなった。ループス腎炎の臓器障害の出現には抗DNA抗体をはじめとする自己抗体産生が重要であるとされてきたが、臓器障害の重症化にはILC、それにより産生されるGM-CSF、GM-CSFにより誘導されるマクロファージが関与していることがわかり、この炎症メカニズムを制御することにより、ループス腎炎の重症化を制御できた。
これらのことから将来的にILCをターゲットにしたループス腎炎の新規治療法の開発の可能性がでてきた。特に研究で用いられたNKp46阻害抗体は、類似の作用を持ちヒトでも使用可能なものが開発中であり、今後臨床応用が期待される。
ヒト腎臓ではこの研究で明らかとなったようなメカニズム解明を行うことはなかなか難しく、モデルマウスなどによる病態メカニズム研究は極めて重要である。一方で、研究結果の大部分はモデル動物における結果に基づいており、ヒトのループス腎炎でも同様の機構が起こるのかについては今後の検証が必要となる。
「今回の研究成果を元にILCと臓器炎症の関係、ループス腎炎の重症化制御についてさらなる検討を続けていく予定」と、研究グループは述べている。
▼関連リンク
・札幌医科大学 プレスリリース




