ヒトiPS/ES細胞、構造的・機能的な小腸上皮細胞への分化誘導は困難だった
京都大学iPS細胞研究所(CiRA)は7月12日、マイクロ流体デバイスを用いて間質流を再現することで、ヒト多能性幹細胞(iPS/ES細胞)から、小腸における多層構造を持つモデルを開発することに成功したと発表した。この研究は、同研究所の出口清香特定助教、高山和雄講師(CiRA増殖分化機構研究部門)などの研究グループによるもの。研究成果は、「Cell Stem Cell」に掲載されている。
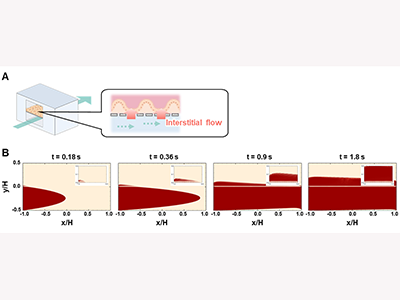
画像はリリースより
(詳細は▼関連リンクからご確認ください)
iPS/ES細胞から体細胞を分化誘導するためには、胚発生における細胞環境をin vitroで模倣することが重要だ。ヒトiPS/ES細胞から小腸への分化誘導においても、さまざまな増殖因子の組み合わせが検討され、成熟化が試みられてきた。しかし、依然として小腸の複雑な構造および機能を再現することは困難だった。小腸は、粘液層と上皮層、間質層が層状に整列した構造を有している。これまで開発されてきたin vitro小腸モデルの多くは小腸上皮細胞が並ぶ上皮層のみから構成されており、小腸上皮細胞を支える間質層は存在しなかった。また、過去の小腸モデルに含まれる小腸上皮細胞は未熟であり、小腸上皮細胞から分泌される粘液の層の形成も十分に見られなかった。
発生過程での間質流をin vitroで模倣、ヒトiPS/ES細胞から小腸モデル構築を試みる
間質流とは、血管から染み出した血漿成分が間質液となって形成する間質中の体液の緩やかな流れだ。発生過程では、小腸の基底側に動脈が接続しており、小腸を構成する細胞は間質流に晒されている。そのため研究グループは、間質流が小腸発生に重要な刺激ではないかと考えた。同研究では、発生過程での間質流をin vitroで模倣することで、ヒトiPS/ES細胞から小腸モデルの構築を試みた。
マイクロ流体デバイスを用いて間質流を再現
間質流をin vitroで再現するため、3.0μmの微細孔を持つ多孔質膜で上下に仕切られた流路を持つマイクロ流体デバイスを用いた。マイクロ流体デバイス内を流れる液体の数値シミュレーションを行ったところ、下部流路の培地を灌流することで、培地が多孔質膜の微細孔を通って下部流路から上部流路に垂直方向に染み出すことがわかった。さらに、下部流路の培地の灌流速度を最適化することで、生体内の緩やかな体液流である間質流と同等の速度および方向の流れを再現できた。
小腸モデル「マイクロ小腸システム」を作製
マイクロ流体デバイスの上部流路にヒトiPS/ES細胞を播種し、下部流路の培地を低速灌流しながら小腸への分化誘導を行うことで、小腸モデル「マイクロ小腸システム」を作製。組織学的解析により、間質流を作用しながらヒトiPS/ES細胞を分化誘導することで、絨毛様に隆起した三次元構造を有する上皮層が構築できた。上皮層の下層には間質層が整列し、多層構造を成すことがわかった。また、電子顕微鏡解析により、間質流を作用したマイクロ小腸システムでは、表面に微絨毛を持つ円柱状の均一な小腸上皮細胞が観察された。このように形態的に成熟した小腸上皮細胞は、静止培養を行った群では観察できなかった。
間質流、小腸としての成熟化促進を示唆
小腸は吸収上皮細胞や杯細胞(mucin 2:MUC2)、パネート細胞(lysozyme:LYZ)等の複数種類の上皮細胞から構成されている。また、小腸上皮細胞のマーカーであるvillin 1(VIL1)が頂端側に局在するなどの極性が見られる。こうした多様な小腸上皮細胞がマイクロ小腸システムにも存在するかどうかを調べるために、小腸上皮細胞の代表的なマーカータンパク質の発現を調べた。間質流の存在下では、小腸上皮細胞マーカー(VIL1)がより強く観察された。VIL1は、特にマイクロ小腸システムの頂端側に局在しており、極性を持った細胞が構築できたことがわかった。杯細胞やパネート細胞も間質流の存在下で数多く確認された。さらに、in situ ハイブリダイゼーション法により、間質流を作用したマイクロ小腸システムにおいて吸収上皮細胞マーカー(solute carrier family 26 member 2:SLC26A2)や幹細胞マーカー(leucine rich repeat containing G protein-coupled receptor 5: LGR5)、bestrophin 4(BEST4)を発現する細胞を確認。さらに、間質流を作用したマイクロ小腸システムでは、杯細胞から分泌される粘液層の主成分であるムチンが蓄積していた。これらの結果は、間質流が小腸としての成熟化を促進したことを示唆している。
小腸上皮細胞を支える線維芽細胞の局在、間質流で変化
小腸における上皮細胞の維持および分化は、間質細胞の一種である線維芽細胞によって支持されている。そこで、マイクロ小腸システムにおける線維芽細胞の特徴を調べた。線維芽細胞マーカーであるvimentin(VIM)は、間質流に応答して基底側へ局在した。静止培養を行ったモデルでは、線維芽細胞は配向せず、ランダムに配置していた。これら線維芽細胞が分泌する細胞外マトリックスの一種であるコラーゲン線維も、基底側に局在していた。これらの結果より、小腸上皮細胞を支える線維芽細胞の局在が間質流によって変化したことがわかった。
マイクロ小腸システム、小腸の薬物動態試験・感染症研究に応用可能
開発したマイクロ小腸システムの応用可能性を確認するため、薬物代謝実験およびウイルス感染実験を行った。マイクロ小腸システムを用いて、小腸で高発現する薬物代謝酵素cytochrome P450 family 3 subfamily A member 4(CYP3A4)の活性を測定。その結果、間質流を作用したマイクロ小腸システムは、高いCYP3A4活性を有することがわかった。また、ヒトコロナウイルスの一種であるhuman coronavirus 229E(HCoV-229E)は、alanyl aminopeptidase, membrane(ANPEP)というタンパク質を感染受容体として小腸に感染する。マイクロ小腸システムにおけるANPEPの発現パターンを確認したところ、間質流を作用したモデルでは、生体小腸と同様に、小腸上皮細胞の頂端側に局在していた。実際に感染実験を行ったところ、感染受容体を発現する頂端側からウイルスを作用した方が、受容体を発現しない基底側から作用するよりも、HCoV-229Eが効率よく感染した。以上の検討により、マイクロ小腸システムは小腸の薬物動態試験や感染症研究に応用可能であることが示唆された。
腸疾患研究や新薬開発への貢献に期待
今回の研究は、マイクロ流体デバイスを用いることでin vitroで間質流の再現を実現した。間質流の存在下でヒトiPS/ES細胞から小腸上皮細胞および間質細胞を同時に誘導することで、生体小腸に類似した多層構造を有した小腸組織モデル「マイクロ小腸システム」を作製できた。研究チームは同モデルが、腸疾患研究やそれらに対する新薬開発に貢献することを期待される、と研究グループは述べている。
▼関連リンク
・京都大学iPS細胞研究所(CiRA) プレスリリース



