再発時の治療法は未確立、既存治療の効果が弱まることが一つの要因
国立がん研究センター6月25日は、悪性脳腫瘍に対する新しい治療法として日本で開発された新規放射性治療薬64Cu-ATSMの第1相医師主導治験を実施して安全性と有効性を明らかにし、同試験の結果を受けて、2024年6月から、悪性神経膠腫患者を対象にランダム化第3相医師主導治験(STEP-64試験)を開始したことを発表した。この試験は、同センター中央病院と神奈川県立がんセンター、量子科学技術研究開発機構(QST)、リンクメッド株式会社(QST認定ベンチャー)の研究グループが実施しているもの。P1試験の結果は、米国臨床腫瘍学会(ASCO)2024で発表された。
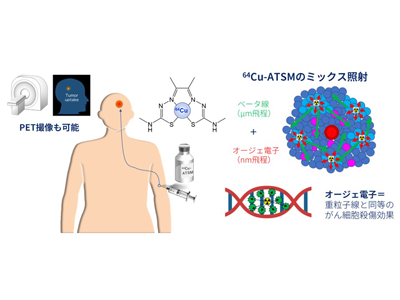
画像はリリースより
(詳細は▼関連リンクからご確認ください)
脳から発生する原発性脳腫瘍は国内の年間発生数が約3万人で、そのうち約7,000人程度が悪性脳腫瘍(がん)である。脳腫瘍は分類が複雑で、悪性脳腫瘍の中でも、最も多い膠芽腫や星細胞腫などは悪性神経膠腫(グリオーマ)と呼ばれている。膠芽腫の年間発生数は約2,100人で、5年生存割合は約15%程度と、最も治療が難しいとされるがんの一つだ。膠芽腫を含む悪性脳腫瘍は代表的な希少がんかつ難治性がんで、治療開発が十分とはいえない状況である。
悪性脳腫瘍の治療においては、既存の治療法(外科手術、放射線治療、化学療法等)で十分な効果が得られず再発した場合の治療法は確立していない。これは、悪性腫瘍は活発に増殖するため血管新生が追い付かず、酸素の供給が乏しい低酸素環境になるため、既存治療法の効果が弱まってしまうことが一つの重要な要因になっている。
64Cu-ATSM、殺傷効果が高く正常細胞への影響は極少、PETで薬剤集積の確認可能
がん細胞は低酸素下でも生き延びることが特徴で、治療抵抗性の原因となってきた。国立がん研究センターと量子科学技術研究開発機構は、低酸素環境下の腫瘍細胞に高集積し、高い治療効果が期待できる放射性治療薬64Cu-ATSM[64Cu-diacetyl-bis(N4-methylthiosemicarbazone)の略]を共同開発し、非臨床試験に続きP1臨床試験で検証を進めてきた。
放射性核種64Cuは、既存の放射性治療薬(131Iや 90Y、177Lu)で放出されるベータ線の他に、がん細胞DNAを効果的に損傷する特殊な電子(オージェ電子)を放出するため、がん細胞に対し高い殺傷効果が期待できる。64Cu-ATSM治療はこの新しいメカニズムで、低酸素化した治療抵抗性腫瘍を攻撃する治療法で、既存治療法で十分な効果が得られず再発した悪性脳腫瘍の治療において効果を発揮することが期待される。
64Cu-ATSMで用いられている64Cuは、銅の放射性同位体の一種で、ベータ線、オージェ電子並びにポジトロン(陽電子)を放出し、12.7時間で放射能が半分に減る。ベータ線は、一般に最大飛程がミリメートルオーダーで従来の放射性治療薬に使用される。オージェ電子は、一般に最大飛程がナノメートルオーダーと短いため薬剤のまわりに高いエネルギーを付与することにより、がん細胞DNAを効果的に損傷することができるため、がん細胞に対しアルファ線や重粒子線と同等の高い殺傷効果が期待できる。1個のがん細胞の大きさは、20マイクロメーター程度なので、薬剤が取り込まれがん細胞から発するベータ線やオージェ電子が、がん細胞周囲の正常細胞への影響は極めて少ないと考えられた。
ポジトロンとは、負電荷を持つ電子の反対の粒子で、正電荷を持っている。ポジトロンと電子は互いに引き寄せられ、結合して消滅する。このときに、2本のガンマ線を正反対の方向に放出する。この 2本のガンマ線を陽電子放射断層撮影診断(PET)装置で検出することにより、薬剤の集積を画像化することができる。64Cu-ATSMは、PETで腫瘍への集積を見ながら治療ができるという極めてユニークな性質を有する薬剤である。
P1試験、最大4回静脈投与で重篤な毒性兆候は観察されず、推奨用量決定
P1試験(STAR-64試験)は、悪性脳腫瘍に対する治療用放射性薬剤64Cu-ATSMの至適投与量、投与方法を明らかにする安全性試験として、2018年10月31日~2023年6月29日に実施された、多施設共同、単群、非盲検、用量漸増試験。標準治療終了後に再発した悪性脳腫瘍(神経膠腫、中枢神経系原発悪性リンパ腫、転移性脳腫瘍、悪性髄膜腫)の患者に、64Cu-ATSMを体重1kgあたり1回30、60、99または150MBqを静脈内にワンショットで投与、7日間隔で最大4回投与し、用量を制限する毒性兆候の発現割合を調べた。20 人を登録し、19人に対し投与を実施した。
その結果、64Cu-ATSMの投与に際し用量を制限する毒性兆候として一時的なリンパ球数の減少が観察されたが、その発現頻度や重篤度は大きく懸念されるものではなかった。またリンパ球数の減少の他には64Cu-ATSMの投与に起因する重篤な毒性兆候は観察されず、新たに留意すべき事象も無いと考えられ、悪性脳腫瘍患者に対する64Cu-ATSMの用量として、99MBq/kgの7日ごと最大4回の投与が推奨されると結論づけた。
再発膠芽腫患者9人中5人が1年以上生存
また、64Cu-ATSMを投与した後にPET検査を行い、脳腫瘍の病変に対し64Cu-ATSMが集積していることを確認できた。さらに、有効性の評価対象となった患者18人のうち、14人について6か月以上、12人については1年以上の生存が確認された。悪性脳腫瘍の中でも最も治療の難しい膠芽腫の患者は、再発すると1年後に生存している割合は30~40%程度である。今回再発した膠芽腫の患者9人に対して治療を実施し、1年以上生存できた患者の割合は5人(55.6%)だった。これらのことから、64Cu-ATSMの投与により効果が得られる可能性が示唆された。
P3試験は悪性・難治性神経膠腫対象、標準治療と比較
研究グループは、P1試験の結果を受けて、膠芽腫を含む、再発・難治性の悪性神経膠腫の患者を対象に、64Cu-ATSMの治療による生存期間の延長効果を標準治療と比較検証するためのP3ランダム化医師主導治験(STEP-64試験)を2024年6月に開始した。再発・難治性悪性神経膠腫を対象に、64Cu-ATSMによる治療の全生存期間における優越性を、主治医の考える最良の既存治療(Best physician’s choice:BPC)との非盲検ランダム化比較試験にて検証する。病理診断により悪性・難治性神経膠腫(膠芽腫または、グレード3・4星細胞腫、グレード3乏突起膠腫)と診断された56人の患者を登録し、無作為化割付という方法により28人ずつに分け、64Cu-ATSM(試験治療群)あるいはBPC(標準治療群)のいずれかの治療を受けてもらう。試験治療群では64Cu-ATSM 100MBq/kgを1週間に1回、最大4回まで静脈に投与する(P1試験で99MBq/kgと決定したが、投与量は、99MBq/kg±5%とプロトコールで決めていたので、P3試験では、100 MBq/kgとする)。
標準治療群では、現在日本で再発神経膠腫に対して保険適用されているテモゾロミドまたはベバシズマブから、担当医師が治療法を決定する。投与方法は、それぞれの薬の添付文書に従う。登録日から6週間ごとに画像検査を行い、1年間経過を観察、治療による全生存期間、無増悪生存期間、奏効率などの効果並びに安全性を比較する。
「今回の試験で64Cu-ATSMの既存の治療に対する優位性が示された場合は、新たな標準治療として治療選択肢が増え、また日本初の国産放射性治療薬となることが期待される。また、P1試験からP3試験へ進める薬剤は一般的には10~20%程度といわれる中、アカデミアが開発した日本発の新規放射性薬剤で、日本医療研究開発機構(AMED)の支援を受けてP3試験まで進んだことは、今後の日本におけるさまざまながんに対する治療薬の開発において開発環境と放射性薬の評価のあり方が整備され、多くの副産物や知的資産の蓄積を通じて日本における新規放射性薬の開発力向上に資すると考えられる」と、研究グループは述べている。
▼関連リンク
・国立がん研究センター プレスリリース



