肺炎症病態におけるEVsの治療的役割の解明を目指し、気道上皮細胞に着目
東京慈恵会医科大学は5月7日、細菌性肺炎やウイルス性肺炎、敗血症などさまざまな傷害によって引き起こされる致死的な急性肺傷害(Acute lung injury:ALI)に対し、肺由来の細胞が分泌するエクソソームを含む細胞外小胞(Extracellular vesicles:EVs)が、輸送する炎症や免疫応答に関与するリン脂質結合タンパク質であるアネキシンA1(ANXA1)やマイクロRNAを介したシグナル制御などによって、治療薬となることを発見したと発表した。この研究は、同大総合医科学研究センター次世代創薬研究部の藤田雄准教授、内科学講座呼吸器内科の門田宰助教、荒屋潤講座担当教授、外科学講座呼吸器外科の大塚崇講座担当教授、東京医科大学医学総合研究所の落谷孝広特任教授らの研究グループによるもの。研究成果は、「Communications Biology」に掲載されている。
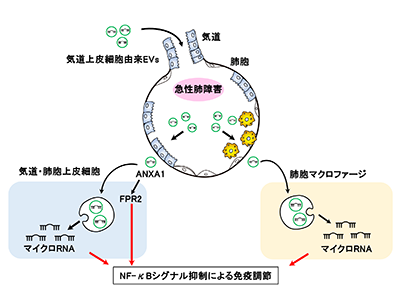
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ALIは、肺上皮および内皮の障壁の破壊に起因する呼吸不全を特徴とする、広く見られる肺疾患だ。その要因として、細菌性肺炎やウイルス性肺炎、誤嚥などの肺に直接起因するもの、敗血症や外傷などの肺外因子などがあり、ALIがさらに悪化することで急性呼吸窮迫症候群(Acute respiratory distress syndrome:ARDS)に進展する。例えば、SARS-CoV-2感染症の場合、肺上皮細胞への病原性刺激が自然免疫反応を引き起こしてALIを誘導し、進展に伴って全身のサイトカインストームやARDSを発症し重症化する。
ALI病態生理の理解が進んでいるにもかかわらず、全身ステロイド投与、肺保護換気、腹臥位などの治療法の有効性はしばしば限定的であり、肺の炎症を効果的に緩和し、肺傷害を減少させる新規の治療戦略を開発することが求められている。エクソソームを含むEVsは、あらゆるタイプの細胞から放出される脂質二重膜に包まれたナノ粒子だ。これらの小胞は、親細胞からのタンパク質、メッセンジャーRNA、マイクロRNA、脂質のキャリアとして機能し、それによって受容細胞におけるシグナル伝達を誘導することが知られている。さらに、肺内のみならず肺外の細胞から分泌されるEVsが、肺微小環境における気道や肺胞細胞のクロストーク現象を促進することにより、肺組織内の生理的・病理学的活動の両方を制御する上で重要な役割を果たしていることが判明している。
研究グループは今回、肺の炎症病態におけるEVsの治療的役割を解明することを目的に、EVsの供給源として気道上皮細胞に焦点を置いた。同研究グループの先行研究では、健康なヒト気道上皮細胞由来EVs(HBEC-EVs)が、トランスフォーミング増殖因子β(TGF-β)による筋線維芽細胞分化と肺上皮細胞の老化を効率的に抑制することが明らかになっており、肺線維症を緩和するHBEC-EVsの効果は、競合開発品の間葉系幹細胞(Mesenchymal stem cell:MSC)由来EVsよりも強力であることがわかっている。しかし、致死的な呼吸器疾患であるALI/ARDSの治療におけるHBEC-EVsの効果については、十分に検討されていなかった。
HBEC-EVs、ALIの細胞モデルで免疫抑制効果を示す
研究では、HBEC-EVsが肺の免疫調節に寄与する可能性を評価した。HBEC-EVsは、THP-1細胞マクロファージおよびHBECsの両方で炎症サイトカインの分泌を減少させることにより、ALIの細胞モデルで免疫抑制効果を示した。
ANXA1とFPR2受容体の相互作用がNF-κBシグナル伝達を抑制し炎症を抑える
また、HBEC-EVsがさまざまな免疫関連の表面マーカーを内在的に発現しており、その作用はToll-like receptor(TLR)-NF-κBシグナル伝達経路を制御する9種のマイクロRNAに一部起因することも明らかにした。さらに、HBEC-EVsのプロテオミクス解析により、炎症の調節に重要なWNTおよびNF-κBシグナル伝達経路に関与するタンパク質の存在が明らかになった。
さらに、HBEC-EVsに含まれるANXA1がFPR2受容体と相互作用し、NF-κBシグナル伝達を抑制することで炎症を抑制することが示唆された。マウスモデルでの実験では、HBEC-EVsの気道内投与が肺損傷、炎症細胞浸潤、およびサイトカインレベルの低下によってALIを軽減することが示された。
ステロイドに代わるALIに対する新規治療薬開発の可能性
ALI/ARDSに対する治療法として使われてきた全身ステロイド投与の有効性はしばしば限定的であり、副腎皮質ステロイドの副作用は患者の予後にも影響を与える可能性があるため、異なる免疫制御機構を持つ治療薬が必要とされている中、同研究でHBEC-EVsがALIの治療薬として有望であることが示唆された。HBEC-EVsは細胞から分泌される天然成分であり、in vitroにおいては一般的に使われる用量のデキサメサゾン(副腎皮質ステロイド)と同程度の炎症抑制作用を認め、in vivoにおいてはALIマウスモデルで優れた治療効果を認める安全性の高い治療薬候補と考えられる。
「今後、細菌感染や新型コロナウイルス感染などさまざまな要因に伴うALI/ARDSを標的として本シーズの社会実装を目指し、さらなる開発を推し進めて行く」と、研究グループは述べている。
▼関連リンク
・慈恵大学 プレスリリース




