感染から数日以内に高度脳浮腫を呈するインフルエンザ脳症、発症因子の探索は困難
大阪大学は5月7日、これまで未解明であった、インフルエンザ脳症の発症のメカニズムを解明したと発表した。この研究は、同大大学院医学系研究科感染症・免疫学講座ウイルス学の木村志保子特任助教(常勤)、上田啓次教授らの研究グループによるもの。研究成果は、「Acta Neuropathologica」にオンライン掲載されている。
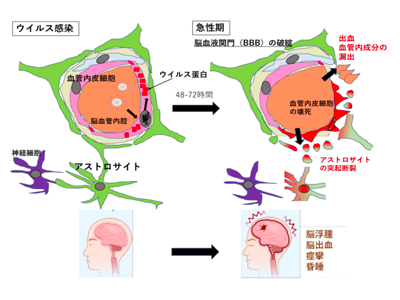
画像はリリースより
(詳細は▼関連リンクからご確認ください)
日本を含む東アジアに多いインフルエンザ脳症のうち、高度脳浮腫を呈し予後の悪い重症型では、ウイルス感染から早い症例で10時間以内にけいれんなどの神経学的所見を認め、24時間以内に高度脳浮腫で死亡、または重度の後遺症を残す。「インフルエンザ」という名前がついているが、SARS-COV2を含む他の病原体でも発症し、また近年は小児のみならず広い年齢層からの報告が相次いでいる。現時点ではこの疾患に対する根治療法は存在しない。ウイルス感染により高度脳浮腫を呈するという病態でありながら、患者の脳からはウイルスがほとんど検出されず、炎症も認めないことが、この疾患における大きな疑問点だった。感染される宿主側要因に関する研究は進んでいたが、ウイルス感染から脳浮腫を呈するまでのわずか数日間のウイルスの動きや脳浮腫の発症因子を探る、というウイルス側からのアプローチは、そのあまりにも早い臨床経過ゆえに困難だった。
今回研究グループは、ウイルス投与により脳症を発症する脳症モデル動物を確立した。そしてこの脳症モデル動物を利用することによって、ウイルス感染後から高度脳浮腫に至るまでのウイルスの動き、それに関与する細胞、病態を探った。
ウイルス投与後72時間までに脳浮腫発症するモデル動物確立
まず、ウイルス投与法や投与量を工夫して、インフルエンザウイルス投与後72時間までに脳浮腫を発症するモデル動物を確立した。併せて、この脳浮腫を発症するモデル動物がヒトにおけるインフルエンザ関連脳症と同様の病理学的、臨床的特徴を備えているかどうかの確認を、ヒトの脳の所見と比較しながら検証した。
ウイルスタンパク質が投与後早期から脳で増加、生きたウイルス粒子はわずか
次に、確立したモデル動物でウイルス動態を調べた。その結果、ウイルス投与後早期からウイルスタンパク質が脳血管内皮細胞やアストロサイトに存在することがわかった。このことから、脳に存在し時間とともに増加しているのは、大量のウイルスタンパク質であり、生きたウイルス粒子はわずかに存在するも脳では増殖していないことがわかった。
転写/タンパク質翻訳抑制する薬剤、タンパク質蓄積とモデル動物の症状を低減
さらに、このウイルスタンパク質の蓄積を抑制することができれば、脳症の発症を抑制し脳浮腫の進行を抑えることができるのではないかと仮定した。仮定に基づいて研究を進めると、これらのウイルスタンパク質は、mRNAの転写もしくはタンパク質翻訳を抑制する薬剤によって産生が抑制されること、またウイルスタンパク質の産生を抑制することにより、脳症モデル動物の症状を抑えることができることが判明した。
また、同じウイルス感染症でも、どこに、そしてどの細胞に感染するかにより、効果のある薬剤が異なってくることが判明した。今回のインフルエンザ関連脳症のモデル動物にはインフルエンザウイルスを感染させているが、通常のインフルエンザウイルス感染症では効果がある一部の既存の抗ウイルス薬が、このモデル動物には効果がなかった。
インフルエンザウイルス以外の急性脳症への治療法開発にもつながると期待
今回の研究成果により、現時点では根治療法の存在しないインフルエンザ関連脳症を予防・治療できる可能性が出てきた。「早期にウイルスタンパク質の産生を阻害することで救命、もしくは神経系後遺症を低減することができるかもしれない。また、同様の方法を用いることで、インフルエンザウイルス以外の急性脳症への治療法開発が進むことも期待される」と、研究グループは述べている。
▼関連リンク
・大阪大学 ResOU



