常染色体潜性遺伝形式発症とされてきた、希少遺伝性自己炎症性疾患ORAS
横浜市立大学は4月24日、希少遺伝性自己炎症性疾患のOTULIN関連自己炎症症候群(Otulin-related autoinflammatory syndrome:ORAS)について、世界で初めて常染色体顕性遺伝形式で発症することを証明したと発表した。この研究は、同大大学院医学研究科の松本直通教授、北海道大学大学院医学研究院の植木将弘特任助教、同大の有賀正名誉教授、京都大学大学院医学研究科の武田有紀子研究員、岩井一宏教授(プロボスト・理事・副学長)らの研究グループによるもの。研究成果は、「The Journal of Experimental Medicine」に掲載されている。
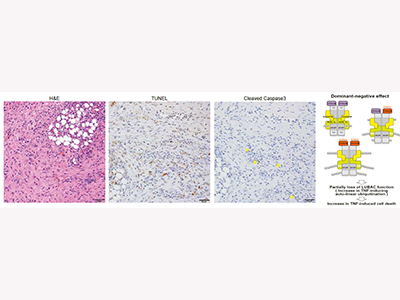
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ユビキチンによるタンパク質修飾は、タンパク質分解や生体内のシグナル活性化などさまざまな生体機能に重要な役割を担っている。直鎖状ユビキチン鎖はLinear-ubiquitin assembly complex(LUBAC)によって生成され、免疫細胞の活性化・炎症・細胞死の調節において重要なNF-κBシグナルの活性化に関与する。OTULINは、直鎖状ユビキチン鎖を脱ユビキチン化することでシグナル活性化の調節を行う。ORASは、その機能低下により、全身性炎症と好中球性皮膚炎を特徴とする、常染色体潜性遺伝形式で発症する症候群とされてきた。
疾患関連性が疑われるバリアント1つのみの患者、新生児期から全身性炎症と好中球性皮膚炎
研究グループは、新生児期から全身性炎症と好中球性皮膚炎を呈しており、TNF阻害治療が著しく有効だった患者に対して、遺伝子全エクソン解析を行い、OTULIN遺伝子に希少バリアントがあることを確認。これまでのORAS患者の解析報告では、疾患関連性が疑われるバリアントは2つの遺伝子座にそれぞれ存在することが通例だった。しかし、今回の解析結果では1つのみであったことから、今回の研究を開始した。
未報告のバリアント1つで直鎖状ユビキチン鎖の蓄積・細胞死増加、ORAS発症
まず、患者細胞および患者由来細胞(EBウイルスB細胞株、iPS細胞)を使用し、細胞における直鎖状ユビキチン鎖の蓄積および細胞死の評価を実施。解析の結果、患者細胞では既報のORASの特徴である直鎖状ユビキチン鎖の蓄積と細胞死の増加を確認した。次に、患者では2つの希少バリアントが各遺伝子座に確認されており、それぞれの評価を各種データベースでの検討やタンパク質立体構造、OTULIN欠損HeLa細胞株に正常・既報および研究グループの患者で確認されたOTULINを強制発現させて評価を行った。その結果、疾患関連性が疑われるバリアントが1つのみであることが強く示唆された。そこで、患者iPS細胞をCRISPR/Cas9システムを用いて遺伝子改変を行った後で、直鎖状ユビキチン鎖の蓄積と細胞死の評価を行った。その結果、未報告の1つのバリアントのみで直鎖状ユビキチン鎖の蓄積と細胞死増加を認め、ORASを発症することが示唆された。
異常OTULIN、正常なOTULINタンパク質機能阻害で疾患発症に寄与
最後に、OTULIN欠損HeLa細胞株に正常OTULINタンパク質と研究グループの患者で確認された異常OTULINの発現量を変化させて評価。その結果、疾患関連性が示唆されたバリアントでは、異常OTULINの発現量が増加するごとに直鎖状ユビキチン鎖の増加と細胞死の増加を認めた。これは異常OTULINが正常なOTULIN機能を阻害することを示し、疾患発症に寄与するということを表す。
未診断患者がORAS診断・有効な治療を受けられる可能性
今回の研究により、未診断であった患者がORASと診断され、有効な治療を受けられる可能性がある。また、今回の研究では患者由来iPS細胞をCRISPR/Cas9システムを用いて遺伝子改変を行うことで病態解析に活用した。今後、さまざまな遺伝性疾患で同技法を用いることにより患者病態解析の促進につながることが期待される。さらに、正常タンパク質の機能を阻害するOTULINタンパク質が発見されたことで、炎症や細胞死に新たな視点を提供し、研究の進展が期待される、と研究グループは述べている。
▼関連リンク
・横浜市立大学 プレスリリース



