網膜色素上皮下に脂質沈着物が蓄積するAMD前駆病変、発生機序や有効な治療法は不明
東京大学は4月18日、加齢黄斑変性(Age-related macular degeneration:AMD)の前兆として現れる変化(前駆病変)の一つである網膜下ドルーゼノイド沈着を発症する遺伝子改変マウスを用いて、AMD前駆病変が生じる仕組みを明らかにしたと発表した。この研究は、同大医学部附属病院眼科の寺尾亮助教と、ワシントン大学セントルイス医学部眼科のRajendra S. Apte教授(兼 ワシントン大学セントルイスマクドネル学術大使、慶應義塾大学グローバル教授)らの研究グループによるもの。研究成果は、「Cell reports」に掲載されている。
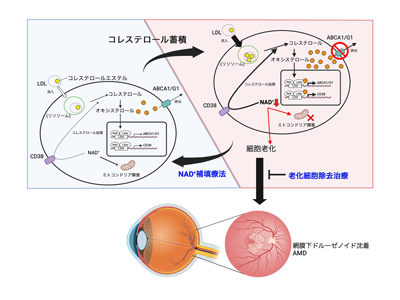
画像はリリースより
(詳細は▼関連リンクからご確認ください)
AMDは失明を引き起こす可能性のある重篤な加齢性眼疾患の一つである。AMDの前駆病変は脂質沈着物のドルーゼンが網膜色素上皮下に蓄積するが、現在この前駆病変の治療法はない。そこで、研究グループはAMD前駆病変の発生機序を明らかにし、これまで治療法のなかったAMD前駆病変に対する治療法を確立することでAMDの発症を抑えることを目的に、研究を行った。
NAD+枯渇で老化したマクロファージにドルーゼン主成分のリポフスチンが蓄積
研究グループは、網膜下ドルーゼノイド沈着を自然発症する遺伝子改変マウスを用いた。解析の結果、免疫細胞の一つであるマクロファージが網膜下ドルーゼノイド沈着に集積しており、それらのマクロファージは細胞老化を来していることがわかった。
そこで、なぜこのモデルマウスのマクロファージが細胞老化を来しているかを探ったところ、酸化還元反応で非常に重要な役割を果たす補酵素であるNAD+がマクロファージで枯渇することが原因と判明した。まず、マクロファージにコレステロールが蓄積することでNAD+の分解酵素であるCD38の発現が増加し、マクロファージのNAD+が消費分解され細胞老化を起こす。その結果、老化したマクロファージの中にドルーゼンの主成分であるリポフスチンが蓄積し、網膜下ドルーゼノイド沈着の原因となることがわかった。
疾患マウスへの老化細胞除去治療やNMN投与、網膜下ドルーゼノイド沈着を抑制
老化細胞除去治療を遺伝子改変マウスに行ったところ網膜下ドルーゼノイド沈着が抑えられたことからも、老化したマクロファージが原因であることが裏付けられている。また、NAD+補填のために前駆体であるニコチンアミド・モノヌクレオチド(NMN)を投与したところ、同様に網膜下ドルーゼノイド沈着を抑えることができた。これらの結果から、老化細胞除去治療やNAD+補填療法がAMDの前駆病変に対する治療として有効である可能性が明らかになった。
「AMDは不可逆性の視力低下を来す。AMD前駆病変に対する治療はAMDへの進展を抑えることで重篤な視力障害を予防できることが期待されるとともに、医療経済的にも意義が大きいものと考えられ、今後は実臨床への治療展開が期待される」と、研究グループは述べている。
▼関連リンク
・東京大学医学部附属病院 プレスリリース



