近年の脳腫瘍を対象とした第1相試験に用いられている評価指標を分析
筑波大学は4月1日、脳腫瘍治療薬の早期臨床試験における有効性評価基準設定の困難さを解明したと発表した。この研究は、同大医学医療系の渡邉真哉講師らの研究グループによるもの。研究成果は、「Therapeutic Innovation & Regulatory Science」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
医薬品の製造販売に先立って実施される臨床試験(治験)には、第1相~第3相までの3段階があり、各段階で有効性エンドポイント(評価指標)が異なる。特に脳腫瘍の治療薬に対する治験の場合、脳腫瘍に特有のバイオマーカーや複雑な評価方法が確立されていないため、最初の第1相試験における適切な有効性エンドポイントについてのコンセンサスがない。また、脳腫瘍の臨床試験における画像評価の課題として、評価対象となる病変が不規則であることが多く、RECISTのような標準的な評価方法の適用が困難であることなどが挙げられている。
研究グループはこれまでに、脳腫瘍の一種である膠芽腫を対象とした第2相試験において、適切な有効性エンドポイントについてコンセンサスがないことを報告しており、PFS(無増悪生存期間)、OS(全生存期間)などのイベント発生までの時間に関連する有効性エンドポイントが使用された場合には対照群がないなど、試験結果の解釈が困難なケースが散見されることを指摘した。また、髄膜腫を対象とした第2相臨床試験においては、さまざまなイベント発生までの時間に関する有効性エンドポイントに対するコンセンサスがなく、時間に関する効果指標の標準化のためには、詳細な予後データを蓄積することが重要であることを明らかにした。そこで今回の研究では、脳腫瘍を対象とした第1相試験で、次相に先駆けて探索的に用いられている有効性エンドポイントについて分析を行った。
DORやDCRも含め、複数の有効性評価指標が用いられている
近年の脳腫瘍を対象とした第1相試験において探索的に使用された有効性評価方法を検討するために、まずClarivate社の検索ツール「Cortellis Clinical Trial Intelligence(TM)」を用いてデータベース検索を行い、検討対象とする試験を特定した。次に、これらの試験に関して、第1相試験における探索的有効性評価に焦点を当てて主要評価項目と副次評価項目の設定を調査し、全体集団と2つのサブグループ集団(脳腫瘍のみを対象疾患とした試験と、脳腫瘍だけでなく他の固形がんも対象疾患とした試験)の解析を行った。
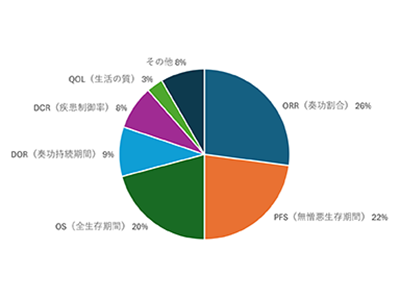
その結果、近年の脳腫瘍を対象とした第1相試験では、ORR(奏効割合)、PFS、OSなど複数の有効性エンドポイントが探索的に用いられているものの、DOR(奏効持続期間)やDCR(疾患制御率)も使われる場合があることがわかった。これは第2相試験にはみられない特徴だという。また、脳腫瘍以外の固形がんも対象に含む第1相試験コホートにおいては、脳腫瘍のみを対象としたコホートと比べ、RECISTの使用頻度が統計学的に優位に高いことを明らかにした。これらのことは、とりわけ脳腫瘍と他の固形がんが同時に組み入れられた第1相試験の場合、脳腫瘍に対する有効性評価が困難で、多次元な評価基準を用いる必要があることを示唆している。さらに臨床試験で行われる画像評価についても、脳腫瘍に関しては、その種類に応じた評価基準の利用が不可欠であると考えられる。
脳腫瘍の治験における有効性評価は、早期の第1相試験でも困難
今回の結果と上述の先行研究を合わせると、脳腫瘍の治験における有効性評価は、第2相試験だけではなく、より早期の第1相試験においても大きな困難さがあり、他の固形がんに対する治験とは全く異なる状況であることが明らかになった。
さまざまなデータベース情報を使用して長期的な予後情報の分析を実施予定
今回の研究は、脳腫瘍を対象とした第1相試験における有効性エンドポイントを評価する初めての研究となった。今後、早期治験における有効性エンドポイントに応じて、試験期間、コスト、次の段階への進行率、および第3相臨床試験の成功率を比較するため、さまざまなデータベース情報を使用して長期的な予後情報の分析を実施するとしている。
「近年、WHO(世界保健機関)より発行された新しい脳腫瘍ガイドラインの分類に基づくエビデンスの蓄積を進める。さらに、遺伝子変異などの新しい分類に基づいた有効性評価方法などについても検討を行う予定だ」と、研究グループは述べている。
▼関連リンク
・筑波大学 TSUKUBA JOURNAL




