開頭術前に遺伝子変異状態を低コストかつ迅速に判別するには?
東北大学は3月12日、脳腫瘍の1つである神経膠腫について、患者群と健常対照者群の血液の赤外吸収スペクトルを解析することにより、神経膠腫の発症および悪性度を決定づけるイソクエン酸デヒドロゲナーゼ(IDH)遺伝子の変異状態を早期に判別することに成功したと発表した。この研究は、同大大学院医工学研究科の松浦祐司教授、同大学院医学系研究科神経外科学分野の金森政之准教授らの研究グループによるもの。研究成果は、「BMC Cancer」に掲載されている。
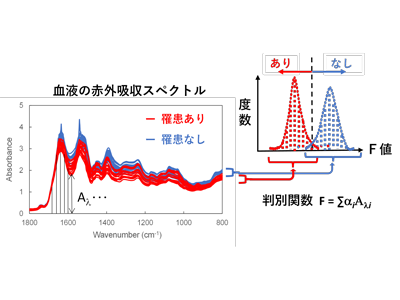
画像はリリースより
(詳細は▼関連リンクからご確認ください)
神経膠腫のような脳実質内腫瘍では、再発を避けるために摘出切除範囲を拡大すると、術後の患者のQOLが著しく低下してしまうというジレンマがある。切除範囲は化学療法や放射線治療の有効性/予後予測を考慮の上で決定すべきであるが、これらを大きく左右する特定遺伝子の変異状態については、切除後の腫瘍組織片の染色画像やゲノム解析により判断しているのが現状だ。開頭手術前に血液からこの遺伝子の変異状態を予測することができれば、摘出術に踏み切るかどうかの判断を含めた神経膠腫の治療方針決定に大きく貢献できる。
血液中には疾患の存在を示す、いわゆるバイオマーカー物質が多数含まれている。有力なマーカー1種を標的とし、その血中濃度を高精度で計測する技術は日々進歩しているが、標的ごとに特定の試薬や前処理を必要とするなど、時間的・人的資源を含め高コストである。また単一のマーカーからの判別精度には限界もあった。一方、血液の赤外吸収スペクトルにはあらゆる血中成分が高感度で反映されるうえ、測定にあたり試薬や試料の前処理も不要だ。全マーカー物質の濃度変動を網羅的に捉えることで、疾患の有無や重症度の低コストかつ迅速な判別が可能となることが期待される。
新たに開発したFTIR-ATR用いて血液の赤外吸収スペクトルを取得
研究グループは、臨床研究に同意を得た神経膠腫患者84人(IDH変異型30人、IDH野生型54人)および健常者72人の血漿検体を収集した。血漿の赤外吸収スペクトルは赤外フーリエ変換減衰全反射分光法(FTIR-ATR)によって取得した。研究グループはこれまでに、小型の多重反射ATRプリズムの開発を進めてきた。20マイクロリットルというごく少量の血液試料に対し、約30マイクロメートルの試料内実効光路長を確保した高感度かつ安定的な測定が可能だ。
発症判定の精度83%、IDH遺伝子変異による悪性度判定精度は75%
得られた赤外吸収スペクトルを多変量解析し、神経膠腫の有無、およびその悪性度を決定的に左右するIDH遺伝子変異状態の判別を試みた。神経膠腫群の健常群からの判別では、全体の70%を学習データとし、残りの30%をテストデータとする交差検証において、10回試行の平均精度83%を達成した。スペクトルからは血中成分の同定も可能であり、神経膠腫の判別ではタンパク質の立体構造組成変化に加え、イムノグロブリン(Ig)などの吸収の寄与度が高いことがわかった。
患者群内でのIDH遺伝子変異状態の判別では、精度75%(30%交差検証試行10回の平均)を達成し、IDH変異型では血漿中タンパク質の重合・凝集度が高くなることがわかった。この現象は脳神経へのダメージを反映し、アルツハイマー病の血中バイオマーカーとして知られるアミロイドβやタウタンパク質の発現量と密接な関わりがあると考えられ、神経膠腫の亢進機序の解明にもつながることが期待される。
治療後以降の変化を継続的に辿ることで再発予測につながる可能性
今回は神経膠腫発症後、治療開始前の患者の血液だけを解析した。研究グループは、「今後は同じ患者の治療終了後~寛解中~症状増悪時と、血液の赤外吸収スペクトル変化を継続的に辿っていくことで、低侵襲かつリアルタイムの全身状態を反映する血液検体からの神経膠腫再発予測の可能性を探っていきたい」と、述べている。
▼関連リンク
・東北大学 プレスリリース




