東アジア人におけるSScのGWASは過去に2つのみで、規模も小さかった
理化学研究所(理研)は1月31日、難治性全身性自己免疫疾患の全身性強皮症(SSc)におけるアジア人最大規模の全ゲノム関連解析(GWAS)を行い、新規疾患関連一塩基多型(SNP)を同定し、病態形成における機能を解明したと発表した。この研究は、理研生命医科学研究センター ゲノム解析応用研究チームの寺尾知可史チームリーダー(静岡県立総合病院 臨床研究部 免疫研究部長、静岡県立大学 薬学部ゲノム病態解析講座 特任教授)、石川優樹研究員、東京大学 大学院新領域創成科学研究科 メディカル情報生命専攻の松田浩一教授らの共同研究グループによるもの。研究成果は、「Nature Communications」オンライン版に掲載されている。
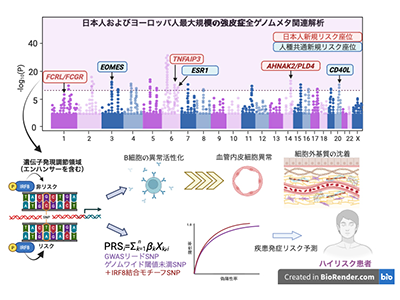
画像はリリースより
(詳細は▼関連リンクからご確認ください)
SScは発症に複数の遺伝因子と環境因子の相互作用が関与する複合性疾患と考えられている。関節リウマチ・高血圧・糖尿病などもこの複合性疾患に含まれる。複合性疾患における遺伝因子の同定には、未知の遺伝因子を含めた網羅的解析「GWAS」が有用だ。SScにおいても欧州人を中心としたGWASは、疾患リスク遺伝子の同定と病態解明に貢献してきた。
一方、欧州人とは遺伝的背景の異なる東アジア人におけるSScのGWASは過去にわずか2つしかなく、欧州人GWASと比較して規模が小さく統計学的検出力に限界があったことから、東アジア人SScの遺伝的背景の解明は十分に進んでいなかった。そのため、サンプルサイズを十分に大きくして統計学的検出力を上げた東アジア人SScのGWASを行い、欧州人SScと共通の遺伝因子および東アジア人特有の遺伝因子を同定することは、SScの病態解明に意義があると考えられた。
日本のSSc患者1,428人、マイクロアレイによる遺伝子型タイピングを実施
研究グループは今回、厚生労働省研究班を中心に全国の多施設で参加を募った患者1,428人から同意の上で提供された末梢血由来のDNAを用いて、マイクロアレイによる遺伝子型タイピングを実施。アレイによる遺伝子型に基づいて、インピュテーションにより、全ゲノムの遺伝子型を決定した。
このインピュテーションには、約3,000人の日本人全ゲノムシークエンス(WGS)サンプルを含む参照パネルを用いており、高い精度でインピュテーションを行うことで正確な推定に基づいた遺伝子型の決定を行った。また、SScに関連する臨床情報として血中の自己抗体、臨床亜型、間質性肺炎などの合併症の有無などの情報も同意の上で提供された。
6つの疾患関連SNPを同定、FCGR/FCRL領域が日本人に特異的な可能性
非SScコントロールサンプルとして、バイオバンク・ジャパンを中心とした合計11万2,599人のサンプルを用いてGWASを行い、3つの新規疾患関連SNPを含む6つの疾患関連SNPを同定した。
3つの新規疾患関連SNPのうち、FCGR/FCRL領域のrs6697139は、東アジア人において全身性エリテマトーデス(SLE)の疾患リスクSNPであり、同研究におけるSSc患者においてもマイナーアレルによるオッズ比(OR)が高い値を示したが(OR 1.366)、よりマイナーアレル頻度が高い欧州人においては統計学的に有意な関連はなく、ORも低値だった(OR 1.026)。このことは、FCGR/FCRL領域のSNPの関連が日本人に特異的である可能性を示しているという。
rs10917688、IRF8結合親和性の変化でSSc病態形成に関連
同SNPに関する機能解析を行ったところ、同SNPと連鎖不平衡にあるrs10917688が遺伝子発現調節領域にあり、免疫細胞の分化および機能調節に関わる転写因子IRF8の結合モチーフを形成することが判明した。
さらにIRF8のSNPであるrs11117420は、欧州人SScにおいて既知の疾患関連SNPであることから、rs10917688とrs11117420におけるアレルの組み合わせによる疾患リスクを日本人SScで比較したところ、rs10917688はIRF8のリスクアレルが存在する場合にのみ疾患リスクを上昇させることがわかったという。これらの結果から、rs10917688はIRF8の結合親和性を変化させることで、SScの病態形成に関連していることが示唆された。
また、欧州人最大のSScメタGWAS解析要約統計量を用いたメタ解析により、さらに3つの新規疾患関連領域を同定した。いずれの領域も免疫学的に重要な領域であること(EOMES、CD40)、また疾患の男女差を説明し得る領域であること(ESR1)など、SScの病態形成において重要な領域が同定されたと言える。
B細胞を標的とした薬剤のSScへの有効性が遺伝的に説明可能に
遺伝子発現を制御するのに重要なエンハンサーに関連するヒストン修飾部位(H3K9Ac、H3K27Ac、H3K4me1、H3K4me3)への遺伝性の集積を細胞種ごとに見た解析では、欧州人と日本人の両方において、特にB細胞への集積が認められた。これはリツキシマブやトシリズマブなどB細胞を標的とした薬剤がSScに有効であることを遺伝的に説明できる知見として有意義な結果であったと言える。
上位5%のPRSを有する被験者は、SSc発症リスク「高」
SScを含む多因子疾患においては、ゲノムワイド閾値未満のSNPも含めて複合的に病態を形成している。このため、GWASにおける効果量と遺伝子型とを用いてスコア化したPRSは、疾患予測や患者の層別化に有用であることが知られている。
同研究においてもPRSに基づいた疾患発症リスクの層別化およびPRSの発症予測能の評価を行った。適切なSNPの選定により作成したPRSの疾患予測能はROC曲線下面積(AUC)約0.610と臨床応用のレベルには及ばなかったが、上位5%のPRSを有する被験者は、有意に疾患発症リスクが高いことも示された。PRSのSSc診療における有用性を示した意義は大きく、今後SNP選定の改善により、さらなるパフォーマンスの向上と臨床応用の可能性が示唆された。
SScを含む自己免疫疾患のゲノム研究の進展や治療の発展への貢献に期待
日本人をはじめとする東アジア人強皮症における疾患関連SNPの同定に至ったことが同研究の最も大きな成果であるとともに、今後の強皮症研究につながる発見と言える。特にFCGR/FCRL領域のSNPは東アジア人に特異的な疾患関連SNPである可能性がある一方で、IRF8との相互作用は欧米人と共通であることが予測され、SNPをはじめとする遺伝因子の病態形成における役割の解明に貢献することが期待される。
「今後のGWASの発展と、より改善されたSNPの選定により、疾患発症予測のみならず罹患臓器や治療反応性、疾患経過の予測といった実臨床に有用なPRSの構築も期待される」と、研究グループは述べている。
▼関連リンク
・理化学研究所 プレスリリース




