課題となるCAR-T治療後の遅発性血球減少、既存の予測マーカーは正確性などに課題
京都大学は2月2日、悪性リンパ腫に対してCAR-T細胞療法を受けた90症例を対象に、CAR-T細胞輸注後のサイトカイン放出症候群(CRS)の発症や持続期間および炎症マーカーで遅発性血球減少の発症を予測できないかの検討を行い、遅発性血球減少の発症や持続期間を精度高く予測できるモデルを作成したと発表した。この研究は、同大医学部附属病院血液内科の中村直和医員、検査部・細胞療法センターの城友泰助教、新井康之助教(病院講師、副センター長)、長尾美紀教授(センター長)、血液内科の髙折晃史教授(病院長)らの研究グループによるもの。研究成果は、「Transplantation and Cellular Therapy」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
キメラ抗原受容体T細胞(CAR-T)療法は、再発難治性悪性リンパ腫の有力な治療法の一つであり、日本では2019年に承認後、実施件数が増加している。臨床の現場でサイトカイン放出症候群(CRS)などの急性期合併症の管理は徐々に向上しつつある一方で、遅発性血球減少を筆頭とする晩期合併症に対してはいまだ課題が多い現状がある。CAR-T療法において遅発性におこる血球減少は、重症感染症や出血リスクの増加、入院日数の延長によるCAR-T施設への負担増加、輸血や顆粒球コロニー刺激因子(G-CSF)製剤投与の可否を決定するための通院による紹介元施設への負担増加を引き起こす。そのため、事前に正確に遅発性血球減少の発症およびその期間を予測することで、より適切なCAR-T治療を実現することができるが、既存の予測マーカー(CAR-HEMATOTOXスコア)は、予測タイミングと正確性の問題で課題があった。今回、「正確性」という点に重点を置き、CRSの発症および炎症マーカーと遅発性血球減少の関連性について調査することとした。
予測能高い「KyoTox-a scoreモデル」作成、治療後の遅発性血球減少に関連の4因子から
研究グループは、同大医学部附属病院血液内科で、CAR-T細胞療法としてチサゲンレクルユーセル、リソカブタゲンマラルユーセル、アキシカブタゲンシロルユーセルを投与されたびまん性大細胞型B細胞リンパ腫(DLBCL)、濾胞性リンパ腫(FL)の90例を対象に、CAR-T細胞輸注後のCRSの発症および炎症マーカーと遅発性血球減少の発症や期間の関連性について調査した。
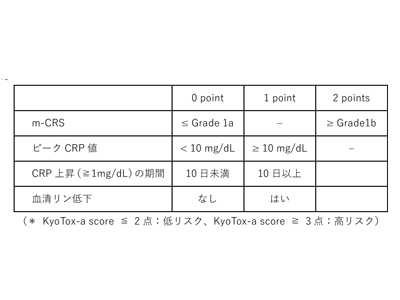
全体での輸注後100日時点の遅発性血球減少累積発症率は、好中球減少57.5%、貧血36.7%、血小板減少49.8%だった。サイトカイン放出症候群(CRS)の重症度と遅発性血球減少に相関が認められた。より詳細に臨床症状の期間でCRSの重症度を細分化したm-CRS grade(grade1のうち発熱期間5日以内のものをgrade 1a、6日以上のものをgrade 1bと評価)を用いると、さらに正確に遅発性血球減少を予測できることがわかった。また、CAR-T輸注後の炎症マーカーの中で、C反応性タンパク質(CRP)ピーク値、CRP上昇の期間、血清リン低下の有無が、遅発性血球減少の発症および持続期間と関連があることも示された。これら4因子(m-CRS grade、CRPピーク値、CRP上昇の期間、血清リン低下の有無)を用いて、KyoTox-a scoreモデルを作成した。KyoTox-a scoreモデルを用いると、全系統の遅発性血球減少(好中球、赤血球、血小板)の発症および持続期間・入院期間の層別化が可能で、また、既存のCAR-HEMATOTOX scoreモデルと比べ、より予測能が高いことも示された。
「KyoTox-a scoreモデルを実際に臨床現場で活用することで、血球減少が発症を事前に予測できるため、CART細胞療法後の感染症対策や輸血の準備などが行いやすくなるだけでなく、CAR-T施設における入院病床のより効率的な運用や、紹介元施設への逆紹介後のより適切な副作用マネージメントが可能となり、治療を受ける患者をはじめ、医療従事者全てにとっての恩恵につながる可能性がある」と、研究グループは述べている。
▼関連リンク
・京都大学 最新の研究成果を知る



