IMAT蓄積、サルコペニアの要因とされるが詳細なメカニズムは不明
秋田大学は11月1日、食後に分泌が増加する消化管ホルモンGIP(Gastric inhibitory polypeptide)が骨格筋の間葉系前駆細胞の脂肪分化を促進し、サルコペニア(老化による筋量・筋機能の低下)の一因となること、そして、このホルモンの作用シグナルを抑制することがサルコペニアの改善につながることを明らかにしたと発表した。この研究は、同大大学院医学系研究科代謝・内分泌内科学講座の髙橋侑也医員、藤田浩樹准教授、脇裕典教授、関西電力医学研究所、藤田医科大学、岐阜大学らの研究グループによるもの。研究成果は、「Journal of Cachexia, Sarcopenia and Muscle」にオンライン掲載されている。
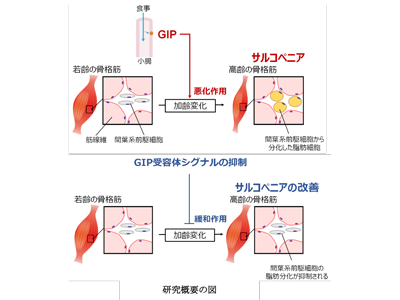
画像はリリースより
(詳細は▼関連リンクからご確認ください)
日本は世界有数の長寿国だが、平均寿命と健康寿命の間には男女とも約10年の隔たりがあり、健康寿命の延伸が課題となっている。身体を動かす筋肉を総称して骨格筋と呼ぶが、骨格筋は身体を動かすのみならず、血糖値をはじめとした代謝調節の作用を持つなど健康を保つうえで重要な役割を果たしており、骨格筋を若い状態に維持することが健康寿命延伸には不可欠である。しかし、骨格筋は加齢に伴ってその量と機能が低下することが知られている。この骨格筋の老化をサルコペニアといい、近年解決すべき健康課題の一つとなっている。
サルコペニアは種々の要因で引き起こされるが、その一つに骨格筋内脂肪(Intramuscular adipose tissue:IMAT)蓄積がある。これは、いわば「牛肉の霜降り」のごとく骨格筋内に脂肪が沈着している状態だが、これがヒトでも起こっており、加齢とともにこのIMATが増加し、そして、IMATが増加すると筋力は低下することが示されている。骨格筋内にある間葉系前駆細胞 Fibro/adipogenic progenitors(FAPs)が脂肪細胞に分化(特定の機能を持つ細胞に変化すること)して、IMATを構成することが知られているが、これを調節するメカニズムについては十分明らかとなっていない。研究グループは長年、GIPと呼ばれる消化管ホルモンを研究してきた。GIPは脂肪細胞の成熟化を促し、肥満を促進する作用があることから、このGIPが間葉系前駆細胞の脂肪分化の調節を介して、IMATを増加させると考え、研究に取り組んだ。
高齢GIP受容体欠損マウス、脚の筋肉群重量は大きく握力強
まず、GIPの役割を明らかにするため、GIPの受け手であるGIP受容体を欠損している遺伝子改変マウス(GIP受容体欠損マウス)について高齢条件で検討を行った。GIP受容体が働いている通常の野生型マウスでは、高齢になると体脂肪率が増え、逆に筋肉量が減り、握力が弱くなる。しかし、GIP受容体欠損マウスは高齢になっても、骨格筋を含む除脂肪組織の割合が多く、脚の筋肉群は重量が大きく、また握力が強いことを示した。
間葉系前駆細胞にGIP受容体発現、GIP添加で脂肪分化効率上昇
続いて、野生型マウスの骨格筋から間葉系前駆細胞を取り出して、この細胞の性質を調べた。間葉系前駆細胞にはGIP受容体が発現しており、GIPを添加することで間葉系前駆細胞の脂肪分化の効率が上昇することがわかった。
GIP受容体の欠損マウスや拮抗薬投与、グリセロール筋注後もIMAT形成抑制/筋線維断面積大
実験的にIMAT形成を誘導する方法として、グリセロール筋注法がある。これはマウスの前脛骨筋と呼ばれる脚の筋肉にグリセロールを注射する実験方法である。GIP受容体欠損マウスではグリセロール筋注後のIMAT形成が抑制されていた。また、筋線維の断面積が大きくなっていることを確認した。また、野生型マウスにGIP受容体の働きをブロックする薬(GIP受容体拮抗薬)を投与したところ、同様に、グリセロール筋注後のIMAT形成が抑制され、また、筋線維の断面積が大きくなっていることを確認した。
GIP受容体シグナル抑制でIMAT減、骨格筋量増に寄与の可能性
間葉系前駆細胞は脂肪分化しIMAT形成に関わる一方で、未分化な間葉系前駆細胞は筋形成を促進する物質を放出して、筋肉量の維持に寄与することが近年注目されている。従って、GIP受容体シグナルの抑制により、単にIMATを減らすのみならず、骨格筋量の増加に寄与することが考えられる。「GIP受容体拮抗薬によりIMATの形成を抑制できたという研究結果は、サルコペニアに対する治療法開発の基盤となると期待される」と、研究グループは述べている。
▼関連リンク
・秋田大学 プレスリリース




