歯周病原細菌P.g.の感染が心血管系に悪影響を及ぼす分子メカニズムは不明だった
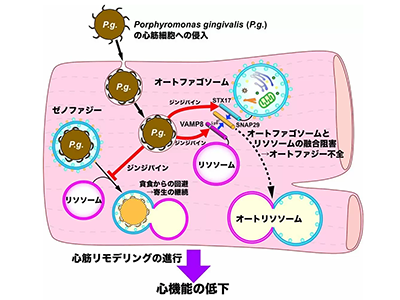
東京医科歯科大学は9月21日、歯周病原細菌「Porphyromonas gingivalis(P.g.)」から放出されるプロテアーゼであるジンジパインがオートファゴソームとリソソームの融合に必須の分子VAMP8の分解を介してオートファジーを抑制することにより、心筋梗塞後のリモデリング悪化作用を発揮していることを発見したと発表した。この研究は、同大大学院医歯学総合研究科循環制御内科学分野の前嶋康浩准教授と渡辺由佳非常勤講師(日本学術振興会特別研究員RPD)の研究グループによるもの。研究成果は、「International Journal of Oral Science」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
歯周病は世界で最も多くの患者を抱える感染症であり、その影響は歯や歯周組織に留まらず全身のさまざまな臓器に及ぶ。歯周病原細菌は心血管系組織にも感染し、急性心筋梗塞・心不全・大動脈瘤・脳梗塞など、生命に関わる疾患の発症と進展に関与していることが明らかになっている。しかし同知見は、主に疫学研究の解析や、歯周病が心血管疾患の発症と進展に影響を及ぼす可能性を動物モデルで再現した基礎研究の成果に基づいており、詳細な分子メカニズムの解明には至っていなかった。
オートファジーは細胞内の不要物の分解やアミノ酸のリサイクルを担当する細胞内機構で、かつては非選択的な細胞内分解システムと考えられていたが、近年、ダメージを受けた細胞内の小器官など特定の物質を選択的に分解する「選択的オートファジー」というメカニズムが存在することがわかってきた。このうち、細胞内に侵入した病原体を選択的に除去する役割を担っているのがゼノファジーだ。
P.g.が歯周組織に常在することができる理由の一つとして、P.g.がゼノファジーを回避するメカニズムを持っている可能性が示唆されてきた。このメカニズムとして、オートファゴソームとリソソームとの融合を阻害することにより自らが分解を受けるのを回避している可能性が想定されていたが、その詳しい分子メカニズムは未解明だった。このメカニズムは健全なオートファジーを妨げ、殊に非分裂細胞である心筋細胞などの生存性を脅かす可能性が高く、種々の歯周組織以外の傷害をもたらす重大な病原因子であると考えられている。このような背景を踏まえて研究グループは、P.g.によりオートファジーを抑制する分子メカニズムの解明、さらにP.g.の感染が心筋梗塞後の心筋に及ぼす影響について検討した。
P.g.が放出するジンジパインがVAMP8を切断・不活化し、オートファジーを阻害
まず、P.g.を感染させた培養心筋細胞を蛍光ラベル法とクリック電子顕微鏡法で観察したところ、心筋細胞内にP.g.が侵入してとどまっていることを確認した。次に、P.g.野生株が感染した培養心筋細胞の方がP.g.ジンジパイン欠損株が感染した培養心筋細胞よりも細胞生存率が低下し、オートファゴソームとリソソームの融合が、より阻害されることを見出した。また、オートファゴソームとリソソームの融合に関連するタンパク質であるVAMP8はジンジパインによって切断・不活性化されること、ジンジパインによる切断部位のアミノ酸を置換した変異VAMP8(VAMP8-K47A)はジンジパインによって切断されないことを明らかにした。
ジンジパインのVAMP8の分解を介したオートファジー抑制をモデルマウスで確認
続いて、P.g.を感染させたマウスを用いて心筋梗塞モデルを作成したところ、P.g.野生株感染群における死亡率はP.g.ジンジパイン欠損株感染群と比較して有意に高く、その死因が心破裂であることが判明。
さらに、ゲノム編集技術によってVAMP8遺伝子を改変したマウス(VAMP8-K47Aマウス)と、オートファジー活性を測定するプローブタンパクを発現するマウス(TG-GFP-LC3-RFP-LC3ΔGマウス)を交配したマウスにP.g.野生株を感染させると、心筋細胞においてオートファジーの抑制が起こらなくなることが確認された。また、VAMP8-K47AマウスにP.g.野生株を感染させた心筋梗塞マウスモデルでは、野生型マウスモデルと比較して心破裂による死亡率が有意に低下することも明らかになった。
ジンジパインによるVAMP8分解阻害がP.g.感染における心機能障害治療に有効な可能性
今回の研究成果により、P.g.の感染がもたらす心筋細胞におけるオートファジーへの影響と制御機構の一端が解明された。P.g.が心筋梗塞後リモデリングの病態に及ぼす影響が明らかとなり、結果、ジンジパインによるVAMP8の分解を阻害することがP.g.の感染に関連した心機能障害に対する治療に有効である可能性が示された。これは将来的な治療領域開拓への応用が期待できる成果と言える。
「難治性の感染症である歯周病とその合併症に対する新規治療の開発は社会における喫緊のニーズだが、本研究成果はそのニーズに応える一助になるものと考えている。さらに、P.g.の感染は心疾患に限らず、神経変性疾患や糖尿病、動脈硬化症などの発症にも深く関わっていることが知られているため、本研究で得られた知見は心臓領域の治療応用に限らず、広く他の疾患へ応用していくことが可能であると考えられる」と、研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース




