Th17細胞の脂質代謝と自己免疫疾患の病態との関連性は?
かずさDNA研究所は8月3日、自己免疫疾患を引き起こす病原性Th17細胞の制御に関わる5つの脂質代謝酵素や機能性脂質を明らかにしたと発表した。この研究は、同研究所の遠藤裕介室長の研究チームと、東京大学医学部の村上誠教授、千葉大学の中山俊憲学長らの共同研究によるもの。研究成果は、「Science Immunology」に掲載されている。
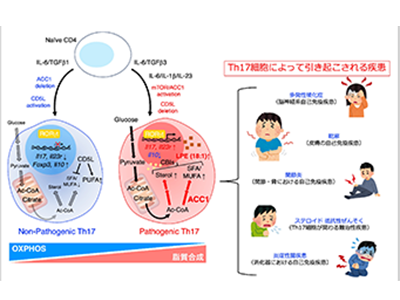
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ここ数年の研究から、免疫システムと代謝システムを担う細胞の相互作用により、生活習慣病や免疫疾患の治療を目指したイムノメタボリズム研究が注目されている。例えば、肥満環境下においては、自己免疫疾患を誘導する能力が非常に高いTh17細胞が増加する一方、免疫反応の収束や抑制に関わるTreg(Regulatory T)細胞が減少することが報告されている。
Th17細胞はヘルパーT細胞の一種で、多発性硬化症、関節リウマチ、乾癬、炎症性腸疾患などの自己免疫疾患を引き起こす悪玉細胞と考えられている。これまでに研究グループは、Th17細胞は脂質代謝によってコントロールされることを明らかにしてきたが、具体的にどのような脂質がTh17細胞を増加させるのかは不明だった。
研究グループは今回、Th17細胞の脂質代謝に焦点をあて、その質の変化をコントロールする特異的な因子を探索し、自己免疫疾患の病態との関連性および誘導メカニズムを明らかにすることを目的として研究を行った。
大規模スクリーニングでTh17細胞を増加させる5つの脂質代謝酵素を発見
研究グループは、ゲノム編集技術を用いた大規模スクリーニングにより、Th17細胞を増加させる5つの脂質代謝酵素(GPAM、GPAT3、LPLAT1、PLA2G12A、SCD2)を新たに発見した。
RORγtの脂質リガンドとしてLPE[1-18:1]を同定
また、1-オレオイル-リゾホスファチジルエタノールアミン(LPE[1-18:1])は、Th17細胞の主要な転写因子「RORγt」と特異的に結合して機能することが明らかになった。
PLA2G12A酵素の機能抑制でEAEの病態が顕著に改善
さらに、5つの酵素のうち最終段階で働くPLA2G12A酵素の機能を抑えることで、多発性硬化症の動物モデルであるEAE(実験的自己免疫性脳脊髄炎:Experimental Autoimmune Encephalomyelitis)の病態が顕著に改善されることが認められた。
今回研究グループが同定した5つの脂質代謝酵素や LPE [1-18:1]は、疾患を引き起こすTh17細胞の増加に非常に重要な役割を果たしていることから、自己免疫性炎症疾患の「ドライバー因子」であると言える。今後、これらの脂質代謝酵素やLPE[1-18:1]と種々の自己免疫疾患病態との関連についてヒト臨床検体を用いて評価することで、Th17細胞による炎症性疾患の予防、新規診断マーカー、治療に結びつく可能性が広がると考えられる。また、研究グループはこれまでの研究で肥満患者のTh17細胞と脂質代謝の割合に相関を認めていることから、今後、これらの因子が関わる脂質代謝経路を創薬ターゲットとすることで、将来的にメタボリックシンドロームの克服に役立つことが期待される。
さらに、今回の研究成果により、これまで長い間発見されていなかったRORγtの脂質リガンドの同定に至った。RORγtはTh17細胞以外にもリンパ節の形成や概日リズムなど多様な役割を担っている。今回発見した脂質が、こうしたTh17細胞以外の生命現象にも影響するのか、新たな研究の発展につながることが期待される。
「今回の研究で同定したLPE[1-18:1]について、今後臨床医と連携してさらに研究を進めていくことで、疾患治療や検査へと役立てていく。将来的には、このような脂質免疫研究を発展させていくことで、自己免疫疾患や肥満症だけでなくアレルギーや感染症に対しても食習慣と免疫の観点から克服し、健康寿命の増進へとつなげていく」と、研究グループは述べている。
▼関連リンク
・かずさDNA研究所 ニュース



