MELAS、遺伝子変異からミトコンドリア機能の低下につながるメカニズムは不明
九州大学は7月20日、サイブリッド細胞を構築してミトコンドリア機能とミトコンドリアtRNAを解析し、tRNA遺伝子内部に3243A>G変異と3290T>Cハプロタイプの2つをもつとき、tRNAのタウリン修飾が改良することでミトコンドリア機能が改善することを明らかにしたと発表した。この研究は、同大医学系学府博士課程の上田沙央理氏、大学院医学研究院臨床検査医学の康東天名誉教授、保健学部門検査技術科学の内海健教授、東京大学工学系研究科化学生命工学の鈴木勉教授らの研究グループによるもの。研究成果は、「Nucleic Acids Research」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ミトコンドリアは、細胞内でエネルギー産生の役割を担う細胞小器官である。細胞内の核やミトコンドリアがもつDNAのうちミトコンドリア機能に関わる遺伝子で変異が生じると、心臓、骨格筋、神経系などでさまざまな症状を呈するミトコンドリア病を発症する。ミトコンドリア病の発症頻度は10万人に9~16人程度で、現在までに有効な治療法は確立していない。なかでも最も発症頻度の高いミトコンドリア脳筋症の一つMELASでは、脳卒中様発作を中心とした重篤な症状が引き起こされ、発症後数年で多くの人が亡くなっている。MELASをはじめとするミトコンドリア病は厚生労働省による指定難病の対象となっており、治療法の開発が望まれている。
MELASを発症する多くの場合では、ミトコンドリアDNAのうちtRNAをコードする遺伝子に変異が生じている。MELASを発症するメカニズムは解明されていないが、アミノ酸の一種であるタウリンによるtRNAの修飾が関与していると報告されている。研究グループは、MELASの患者では、tRNAの構造が不安定になることでtRNAのタウリン修飾が低下し、その結果、ミトコンドリア機能が低下することを既に報告している。しかし、ミトコンドリア機能の低下に関わる詳細なメカニズムはいまだ解明されていない。
軽度の臨床症状を示す患者、3243A>G以外に非病原性変異3290T>Cが存在
研究グループは、MELASで頻繁に報告されているミトコンドリアDNA遺伝子変異3243A>Gを高い割合でもつにも関わらず、軽度の臨床症状を呈する患者の共通点を見出した。この発見はMELASの治療やメカニズムの解明に役立つと考え、研究を進めてきた。
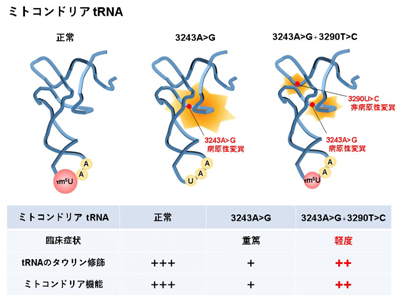
ミトコンドリアDNAの解析結果から、軽度の臨床症状を示す患者にはtRNAの遺伝子内部に病原性変異3243A>Gに加えてもう1つの非病原性変異3290T>Cが共通して存在することを見出した。
2つの変異をもつ細胞はtRNAのタウリン修飾が改善
そこで、ミトコンドリア機能を評価するために培養細胞を用いた解析を行ったところ、3243A>Gと3290T>Cの2つの変異をもつ細胞(2KD)は3243A>Gのみをもつ細胞(2SD)と比較して、ミトコンドリア依存的にエネルギーを産生して増殖できることがわかった。そして、ミトコンドリア機能障害の程度を示すマーカーの遺伝子発現を調べたところ、3243A>Gと3290T>Cをもつ細胞(2KD)では3243A>Gのみをもつ細胞(2SD)ほどの障害が起きていないことがわかった。また、tRNAのタウリン修飾を調べたところ、3243A>Gと3290T>Cをもつ細胞(2KD)では3243A>Gのみをもつ細胞(2SD)よりもタウリン修飾が改善していることがわかった。したがって、3243A>Gと3290T>Cをもつ細胞(2KD)ではtRNAのタウリン修飾の改善に伴い、ミトコンドリア機能が改善していることが今回の研究で明らかになった。
ミトコンドリア機能の改善に関与するメカニズム、新規治療薬の開発につながる可能性
「今回の研究では、tRNAの遺伝子内部に病原性変異に加えてもう1つの特定のハプロタイプをもつとき、tRNAのタウリン修飾やミトコンドリア機能が改善することを確認し、臨床症状も比較的軽度であることを世界で初めて報告した。このハプロタイプにはtRNAの構造を安定化させる働きがあると考えられるが、ミトコンドリア機能の改善に関与するメカニズムを解明することで、MELASをはじめとしたミトコンドリア病の新規治療薬の開発に貢献できる可能性があると考えている」と、研究グループは述べている。
▼関連リンク
・九州大学 研究成果




