傷ついた脳の修復、脳内の脂質はどのように関与するのか?
東京医科歯科大学は7月25日、脳梗塞後に産生される脂肪酸代謝物が脳梗塞巣周辺部に生き残った神経細胞に作用してシトルリン化酵素PADI4の発現を誘導し、PADI4によるヒストンタンパク質がシトルリン化されることによって神経修復で働く遺伝子の発現が増加する新たな神経修復メカニズムを発見したと発表した。この研究は、同大難治疾患研究所神経炎症修復学分野の中村朱里大学院生、酒井誠一郎助教、七田崇教授、東京大学大学院医学系研究科の村上誠教授、東京都医学総合研究所、慶應義塾大学らの研究グループによるもの。研究成果は、「Neuron」にオンライン掲載されている。
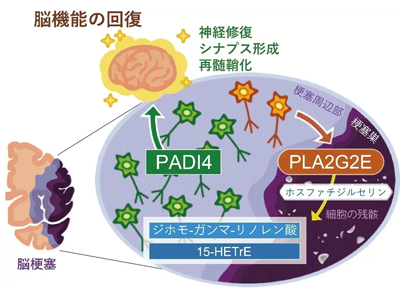
画像はリリースより
(詳細は▼関連リンクからご確認ください)
脳卒中は、脳の血管が詰まって脳組織が壊死する脳梗塞と、脳の血管が破れて出血する脳出血に分けられるが、いずれも発症すると神経細胞がダメージを受けて、手足を上手く動かせなくなったり、感覚が鈍くなったり、上手く話せなくなったりするなどさまざまな脳の機能に障害が生じる。脳卒中によって失われた脳の機能はリハビリテーションによってある程度回復するが、このとき脳の中ではシナプスが新たに作られるなどして、失われた脳の機能を代償するための神経修復が起こっていると考えられている。このように、傷ついた脳は自ら修復する能力を持っているが、脳卒中で生き残った神経細胞がどのようなメカニズムでこのような修復能力を獲得するのかはわかっていなかった。
組織の損傷によって死んだ細胞からは細胞内のタンパク質などが放出され、それらが免疫細胞に作用することで炎症が起こる。脳卒中においても、死んだ神経細胞から放出された細胞内の物質が炎症を引き起こし、脳にさらなるダメージを与えることがわかっている。これら炎症を引き起こす物質が脳内から取り除かれることで炎症が収束し、神経の修復へと移行する。また、組織損傷後に産生されるさまざまな脂質が炎症の制御に関わっていることが知られており、炎症を促進する脂質や炎症を抑制する脂質がこれまでに報告されている。研究グループは、脳損傷後の神経修復において脳内の脂質が重要な役割を担っているのではないかと考え、神経修復の引き金となる脂質を探索し、脂質代謝を介した神経修復のメカニズムを調べた。
PLA2G2E欠損マウス、脳梗塞巣周辺部で神経修復に働くPADI4発現低下
今回の研究では、まず脳梗塞モデルマウスを用いて、脳梗塞発症から1週間後までの脳内にどのような脂質が存在するかを解析した。脳梗塞巣周辺部の組織から脂質を抽出し、質量分析法により脂質の種類と量を調べた結果、脳梗塞発症3~6日後に不飽和脂肪酸の量が増加していた。そこで、細胞膜を構成するリン脂質から不飽和脂肪酸を切り出す酵素ホスホリパーゼA2(PLA2)を欠損するマウスにおいて、脳梗塞の症状が変化しているかマウスの行動評価と脳組織の染色により調べた。数種類のPLA2欠損マウスを用いて検討した結果、PLA2G2Eを欠損するマウスでのみ、脳梗塞後の神経症状の悪化と脳梗塞体積の増加が見られた。
また、野生型マウスとPLA2G2E欠損マウスで脳梗塞巣周辺部の遺伝子発現を比較したところ、PLA2G2E欠損マウスでは神経修復で働く遺伝子の発現量が低下していたが、特にシトルリン化酵素PADI4の発現が顕著に低下していた。脳梗塞モデルマウスおよびヒト脳梗塞患者におけるPLA2G2EとPADI4の発現を免疫組織染色によって調べたところ、脳梗塞発症3日~1週間後に脳梗塞巣周辺部に生き残っていた神経細胞でPLA2G2EおよびPADI4の発現が見られた。PLA2G2Eは細胞外に放出されて働く酵素であり、脳梗塞巣周辺部の神経細胞からPLA2G2Eが放出されて、死んだ神経細胞の細胞膜残骸から不飽和脂肪酸を産生していると考えられる。
PADI4によるヒストンシトルリン化が神経修復に関わる遺伝子の発現を活性化
次に、神経細胞で特異的にPADI4を欠損するマウスを用いて脳梗塞の症状を調べたところ、PADI4欠損マウスでは野生型マウスと比較して脳梗塞による神経細胞死が増えており、脳梗塞後の神経症状の悪化と脳梗塞体積の増加が見られた。また、脳梗塞周辺部から神経細胞を単離して、次世代シークエンス解析によって単一細胞レベルで遺伝子発現を調べた結果、脳梗塞発症4日後の野生型マウスでは神経修復で働く遺伝子の発現量が神経細胞で全体的に増加していたが、神経細胞特異的にPADI4を欠損したマウスでは神経修復で働く遺伝子の発現量があまり見られなかった。
ゲノムDNAはヒストンタンパク質に巻き付いたクロマチン構造としてコンパクトに核内に収納されているが、PADI4がヒストンタンパク質をシトルリン化することによってクロマチンの構造が緩んで遺伝子の転写が活性化されることが他の幹細胞研究などで報告されている。そこで、脳梗塞後の神経細胞における修復性の遺伝子発現変化もPADI4によるヒストンのシトルリン化が寄与しているのではないかと考え、ゲノムDNAのどの領域に結合しているヒストンがシトルリン化されているか次世代シークエンス解析によって調べた。その結果、神経修復で働く遺伝子の転写調節領域にあるヒストンがPADI4によってシトルリン化されており、遺伝子の発現が活性化していることがわかった。
DGLA/15-HETrEの投与、PLA2G2E欠損マウスの神経症状と脳梗塞体積を改善
研究グループは、脳梗塞後に増加していた不飽和脂肪酸のうちジホモ-ガンマ-リノレン酸(DGLA)の量がPLA2G2E欠損マウスで低下していたので、PADI4を介した脳梗塞後の神経修復メカニズムにDGLAが関与しているのではないかと考えた。そこで、脳梗塞を作製したPLA2G2E欠損マウスにDGLAを経口投与したところ、脳梗塞巣周辺部の神経細胞でPADI4の発現が増加し、脳梗塞後の神経症状の改善と脳梗塞体積の減少が見られた。また、培養神経芽腫細胞の培地にさまざまな脂肪酸代謝物を添加してPADI4の発現量が変化するか調べたところ、DGLA代謝物の一つ15-HETrE(15-hydroxy eicosatrienoic acid)の添加によってPADI4の発現量が大きく増加した。15-HETrEを脳梗塞モデルマウスに投与すると、脳梗塞巣周辺部の神経細胞でPADI4および神経修復で働く遺伝子の発現が増加し、脳梗塞後の神経症状の改善と脳梗塞体積の減少が見られた。
以上の結果から、DGLAおよびその代謝物である15-HETrEにはPADI4を介した神経修復を促進する働きがあることがわかった。
脳の神経修復における脂質の新たな機能が明らかに
脳損傷後に神経の修復が起こって脳機能がある程度回復することは知られていたが、どのような分子メカニズムで神経の修復が開始されるのかはこれまでわかっていなかった。今回の研究では、脳梗塞後に産生される脂肪酸代謝物が神経修復の引き金となり、PADI4によるヒストンのシトルリン化を介して神経修復で働く遺伝子の発現が誘導される神経修復の新たなメカニズムを発見した。この研究により、組織損傷後における脂質の機能として炎症の制御に加えて、神経の修復においても脳内の脂質が重要な役割を担っていることが初めて示された。
「神経細胞にPADI4の発現を誘導させる修復性の脂質であるDGLAや15-HETrEには、神経修復を促進して脳梗塞後の神経症状を改善させる働きがあった。これら脂質は食事による摂取が可能であり、修復性の脂質を食事で摂取することで脳卒中後の機能予後を向上させる新たな治療法に応用されることが期待される」と、研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース




