再生医療実現に向け、ヒト臨床で使用可能な下垂体ホルモン産生細胞が求められていた
名古屋大学は6月9日、ヒト胚性幹細胞(ヒトES細胞)およびヒト人工多能性幹細胞(ヒトiPS細胞)を用い、高効率かつ高純度で下垂体ホルモン産生細胞を作製する方法を開発したと発表した。この研究は、同大大学院医学系研究科糖尿病・内分泌内科学の多賀詩織共同研究員(兼 住友ファーマ株式会社)、須賀英隆准教授、有馬寛教授らと、住友ファーマ株式会社再生・細胞医薬神戸センターの桑原篤グループマネージャー、住友化学株式会社生物環境科学研究所の中野徳重 主任研究員、藤田医科大学医学部生理学の長崎弘教授らの共同研究グループによるもの。研究成果は、「Stem Cell Reports」に掲載されている。
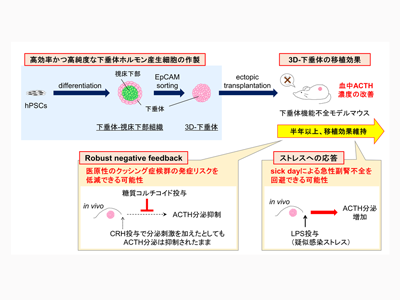
画像はリリースより
(詳細は▼関連リンクからご確認ください)
下垂体はさまざまなホルモンを制御する中心で、司令塔とも言うべき働きをしており、恒常性・成長・代謝・ストレス反応・生殖など多岐にわたる生命現象をコントロールしている。従って、下垂体の機能が低下するとさまざまな症状を引き起こす。特に下垂体で副腎皮質刺激ホルモン(ACTH)が低下すると、副腎不全を起こして生命の危機に陥ることもある。現在、下垂体機能低下症に対する根治療法は存在せず、不足しているホルモンを投与する補充療法が行われている。しかし、ホルモンの必要量は状況に応じて変動するため、現行の補充治療では十分には対応できない場合があり、補充不足による副腎不全や補充過多による医原性クッシング症候群などの発生リスクがある。
生体と同じように周囲の環境に応答する下垂体ホルモン産生細胞が作製でき、それを臨床使用可能なレベルに洗練させることができれば、これまでの補充療法よりも優れた治療法になる可能性がある。研究グループは、2016年にヒトES細胞から、2020年にヒトiPS細胞から下垂体-視床下部組織を作製することに成功している。再生医療の実現に向けては、ヒト臨床で使用可能な基準を想定しつつ、効率良く純度の高い下垂体ホルモン産生細胞を作製する必要があった。
ACTH産生細胞をほぼすべての細胞塊が含む培養法を開発
研究グループが2016年と2020年に報告した下垂体-視床下部組織の作製法は、胎児におけるこの部位のでき方を試験管内で再現するところに特徴がある。今回、ヒト臨床で使用することを想定した下垂体-視床下部組織の分化法を開発するにあたって、下垂体の発生を試験管内でより精密に再現することを目指し、新たにWntおよびTGFβシグナルの阻害物質を作用させた。その結果、作製した下垂体-視床下部組織のうち、ほぼすべての細胞塊がACTH産生細胞を含んでおり、以前の培養方法では約30%であったのと比較して安定性と効率が大きく改善した。
EpCAMをマーカーに下垂体ホルモン産生細胞のみ選別、精製
しかし、今回開発した分化誘導法であっても、下垂体-視床下部組織における下垂体と視床下部への分化誘導、特に後者を厳密に一定に制御することが難しいという課題が残った。そこで、下垂体表面抗原マーカーのEpCAMを用いたセルソーティングを行い、下垂体-視床下部組織から下垂体ホルモン産生細胞のみを単離することで、高純度な下垂体組織の作製を目指した。
さまざまな条件を検討し、例えば、細胞の選別時期については分化60日以降のセルソーティングが望ましいことがわかった。精製後に再凝集した細胞(3D-下垂体)はACTH産生細胞を豊富に含む高純度な下垂体ホルモン産生細胞で構成され、試験管の中で高いACTH分泌能を示した。この3D-下垂体が生体内と同様の制御を受けて下垂体ホルモンを分泌するかどうか、まず試験管内で検討しました。副腎皮質刺激ホルモン放出ホルモン(CRH)を作用させるとACTHの分泌が増加し、デキサメサゾンを作用させるとACTHの分泌が抑制されることを確認した。
精製後に再凝集した細胞をマウスへ移植し、長期有効性と環境に応答する分泌制御を確認
次に、移植した生体内でもこの3D-下垂体が機能するかを確かめるために、下垂体を除去したマウス(下垂体機能不全モデルマウス)に3D-下垂体を移植して検討した。移植した細胞はマウス内で半年以上生着し、マウス血中ACTH濃度の改善を認めた。さらに、ホルモンの反応性を検討したところ、環境に対応する応答性も持ち合わせることが示唆された。例えば、デキサメサゾン投与状態では移植細胞にきちんと抑制がかかり、ACTHは分泌されなかった。この結果は、移植後も分泌が止まるべき時に止まり、移植細胞からの分泌過剰によって副作用が引き起こされるリスクが低いことを示唆している。
また、疑似感染ストレスとしてリポ多糖(LPS:Lipopolysaccharide)投与を行ったところ、LPSに反応してACTH分泌が増加した。すなわち、風邪などの強いストレスがかかった緊急時(sick day)には、移植片からACTHが追加分泌されることで急性副腎不全に陥るリスクを低減可能であることを示唆している。
下垂体機能が低下した患者に対する再生医療の実用化に向けて一歩前進
ヒトES細胞およびヒトiPS細胞を材料にして、ヒト臨床での使用を想定しつつ高効率で高純度な下垂体ホルモン産生細胞を作製可能にしたことで、下垂体の機能が低下した患者に対する再生医療の実用化に向けて一歩前進した。「今後、研究成果をもとに、臨床投与方法や併用薬等の臨床プロトコルの検討、臨床用細胞を製造するための大スケール化・さらなる高効率化等の製法検討、非臨床安全性評価を行い、下垂体の再生医療の実現化に向けた研究開発を進めていきたい」と、研究グループは述べている。
▼関連リンク
・名古屋大学 研究成果発信サイト




