免疫系の異常を引き起こす「RelA異常症」、重症型の原因は不明だった
東北大学は6月6日、周期性発熱や炎症性腸疾患、自己免疫性疾患、皮膚疾患などを発症した5家系の患者で、「RELA遺伝子変異」による新規病型を発見したと発表した。この研究は、防衛医科大学校小児科 森谷邦彦助教(研究当時:東北大学大学院医学系研究科小児病態学分野助教)、東北大学医学部小児科 中野智太助教の研究グループと広島大学大学院医系科学研究科小児科学 岡田賢教授、津村弥来研究員)の研究グループ、京都大学の井澤和司助教、本田吉孝特定助教、九州大学の石村匡崇講師、園田素史助教、米国ロックフェラー大学の大岸誠人大学院生らとの共同研究によるもの。研究成果は、「Journal of Experimental Medicine」にオンライン掲載されている。
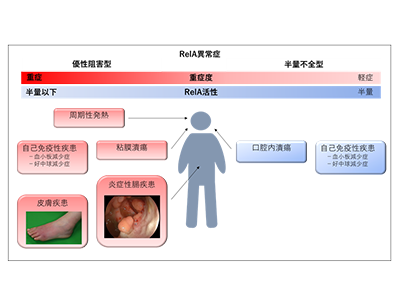
画像はリリースより
(詳細は▼関連リンクからご確認ください)
原発性免疫不全症は400種類以上の病型が知られており、免疫系の異常により易感染性、自己炎症、自己免疫症、アレルギーなどさまざまな病態を起こす。その中で「RelA異常症」は、反復する皮膚・粘膜潰瘍を生じる4人の患者から2017年に同定された疾患だ。RELA遺伝子にコードされている転写因子RelAは、NFκBシグナル経路の重要な因子で、サイトカインなどの刺激により活性化し、炎症や細胞増殖に関連する遺伝子群の働きを調節することで免疫反応の制御を行う。RELA 遺伝子の変異のうち、半量不全をきたす変異では皮膚や粘膜に潰瘍をつくる軽度の自己炎症疾患を引き起こすことが知られていたが、自己免疫性の血球減少や炎症性腸疾患など重症化する病型の原因は不明だった。
一方、「I型インターフェロン」はウイルスや細菌などの病原体に対して働くサイトカインだ。細胞内に取り込まれたウイルスは、TLRにより認識される。TLRには多くの種類があるが、そのうちTLR7/8/9はインターフェロンの調節因子であるIRF7やMyD88を介してI型インターフェロンの産生を誘導する。このI型インターフェロンが過剰に産生されることにより発症する遺伝病は「I型インターフェロン症」と呼ばれ、2011年にCrowらによって提唱された比較的新しい疾患概念だ。I型インターフェロンの亢進により発症する疾患としては、エカルディ・グティエール症候群のような遺伝病が代表的だ。他方で近年、全身性エリテマトーデスや関節リウマチなどの膠原病や先天性感染症においてもI型インターフェロンの亢進が知られるようになり、その病態の解明が急速に進んでいる。
5家系6例の患者を解析、重症患者の変異RelAは「優性阻害効果」を持つと判明
研究グループは今回、RELA遺伝子変異を持つ5家系6例の患者を同定し、これらの患者においてRelA変異タンパク質が体内で作られていることを確認した。詳細な機能解析の結果、RelA変異タンパク質は、正常なRelAタンパク質に結合することで機能を阻害することから、優性阻害効果を持つことが判明した。そのため、これまで知られていた病型と比較して重症になることがわかった。
TLR7遺伝子発現上昇により複数のインターフェロンが過剰分泌
次に、患者の白血球を検討したところ、I型IFNシグネチャーを認め、既知のI型インターフェロン症と同様の病態が示唆された。患者白血球は、TLR7刺激によりさまざまなインターフェロン(INF-α2,INF-β,INF-γ1,INF-γ2/3)を過剰分泌することも判明した。
この現象を詳細に解析するため、患者白血球を用いてシングルセルRNAシークエンス解析を実施。その結果、患者の骨髄系樹状細胞(mDC)と形質細胞様樹状細胞(pDC)において、TLR7の遺伝子発現が上昇していることが判明した。
NFκB経路の異常でI型インターフェロンの亢進が誘導
一方、リンパ球や骨髄球細胞では、IRF7やMyD88の遺伝子発現の上昇が認められたという。IRF7はI型インターフェロン産生に必要な分子で、NFκB経路により制御されることが知られている。そのため、優性阻害効果を持つRelA変異タンパク質が、TLR7やIRF7遺伝子の発現を強く誘導することでI型インターフェロンの亢進をきたすと考えられた。
I型インターフェロン制御機構の解明に期待
今回の研究成果により、NFκB経路の異常によりI型インターフェロンの亢進が誘導されることが初めて示された。優性阻害効果によるRelA異常症という新規病型の発見は、同症患者に対する効果的な治療薬の選択に貢献するのみならず、I型インターフェロンの制御機構の解明にもつながる重要な発見と言える。
「今回の発見により、本症に対する効果的な治療薬の選択や、I型インターフェロン制御機構の解明につながることが期待される」と、研究グループは述べている。
▼関連リンク
・東北大学 プレスリリース




