XPの8つの原因遺伝子はヌクレオチド除去修復に関連、その詳細は不明だった
神戸大学は4月20日、紫外線や化学発がん物質などによって生じるさまざまなDNA損傷を修復する過程で、修復の失敗を防いでいる精巧な分子メカニズムの解明に成功したと発表した。この研究は、同大バイオシグナル総合研究センターの菅澤薫教授、国立遺伝学研究所の花岡文雄所長、米国国立衛生研究所のWei Yang博士らの研究グループによるもの。研究成果は、「Nature」に掲載されている。
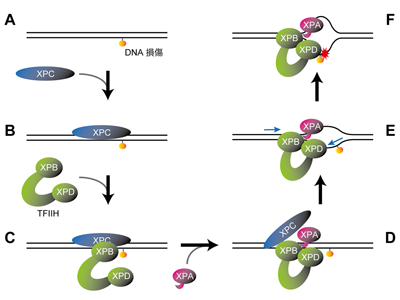
画像はリリースより
(詳細は▼関連リンクからご確認ください)
ゲノムDNAは、活性酸素などの内的要因、紫外線・放射線・化学物質などの外的要因によって絶えず傷つけられている。DNA損傷を放置すると突然変異や細胞死を引き起こし、やがてがんをはじめとするさまざまな疾患の発症につながる可能性がある。このような事態を防ぐための防御機構として、細胞にはDNAの傷を見つけて修復するためのさまざまなメカニズムが備わっている。
ヌクレオチド除去修復(NER)は、紫外線や化学発がん物質によって生じる幅広いDNA損傷を治すことができる重要な修復機構である。潜性遺伝疾患である色素性乾皮症(XP)は、日光に対する皮膚の過敏症状と皮膚がんの好発を特徴とする。XPの患者は8種類の原因遺伝子のいずれかに変異を持ち、このうちXPA~XPGの7種類の遺伝子の塩基配列情報をもとに合成されるタンパク質(XPA~XPGタンパク質)はすべてヌクレオチド除去修復 (NER)の反応に直接関わっている。日本国内では難治性疾患に指定されており、そのうちXPA遺伝子に変異を持つ患者が半数以上を占める。XPの患者の多くはNERが正常に働かず、特に紫外線による皮膚がんを発症しやすいことからも、NERが発がんに対する防御機構として働いていることがわかる。
NERでは、まずXPの原因遺伝子産物の一つであるXPCタンパク質が、DNAの構造異常を見つけ出す「センサー」として働く。XPCは非常に幅広い損傷に対応できる反面、例えばDNAの塩基の組み合わせの間違い(ミスマッチ)など、実際には損傷がないところにも結合してしまう性質がある。そのような場所で無用な修復反応が進んでしまうと、かえって突然変異を引き起こす危険があるため、実際に修復すべき損傷が存在するかどうかを確認することが非常に重要である。この損傷確認のステップに基本転写因子TFIIHとXPAタンパク質が関わることが以前から示されていたが、その詳しいメカニズムは明らかになっていなかった。
DNA損傷部位に結合のタンパク質複合体、分子構造を電顕で詳細に解析
今回、研究グループは、既にわかっているNERの反応ステップに沿って、損傷を含むDNAにXPC、TFIIH、XPAが順次結合した複合体を調製し、それらの分子構造をクライオ電子顕微鏡法により詳細に解析した。ここで用いたTFIIHはXPB、XPDタンパク質を含む7種類のタンパク質によって構成される大きな複合体で、NERだけでなく転写(遺伝子発現)にも必要とされる非常に重要な因子である。TFIIHは通常、馬蹄形(U字形)の構造を取っており、開いた二本の腕の先端にXPB、XPDタンパク質がそれぞれ配置されている。損傷DNA、XPC、TFIIHから成る複合体では、TFIIHは馬蹄形の構造を保っており、XPBを介して損傷部位のXPCと結合する一方で、XPDはDNAやXPCと接触していなかった。ところが、ここにさらにXPAが加わると、TFIIHの構造が大きく変化することがわかった。開いていた馬蹄形の両腕の部分が閉じて環状になると同時に、XPBと損傷との距離が少し離れ、その間にできたスペースでXPDがDNAと結合していた。
XPDの狭い穴でDNA鎖の移動が止まることで損傷の有無を確認、NERによる修復を判断
それでは、ここからDNA損傷の存在がどのようにして確認されるのか。XPBはDNAの二重らせんに結合した上で、DNAの一方の鎖に沿って移動する性質を持つことが知られている。今回明らかになった構造から、XPBはDNA上を損傷から離れる方向に移動すると予想された。ただし、他のタンパク質と結合しているために実際にXPB自身が移動することはできず、逆にDNAの方が動いて複合体の方に引き込まれる。この時、XPAの一部がDNAの二本の鎖の間に挿入されており、あたかもファスナーを開くように二重らせんがほどけて一本鎖の状態になることがわかった。
さらにXPDは一本鎖状態のDNAに結合して、ある決まった方向(5’→3’)に移動する性質がある。XPBとXPAによってほどかれた二本の鎖のうち、XPDは損傷を含むDNA鎖と結合していたが、XPBと同様にXPD自身が移動することはできないため、やはりその損傷鎖が複合体の方に引き込まれる。XPDがDNAと結合する部分は非常に狭い穴のような構造になっており、DNA鎖はその穴をくぐって移動するが、損傷でDNA鎖の構造が大きく変わっているとその部分が穴の入り口に引っかかって止まってしまう(糸の結び目が針穴を通らないイメージ)。
このXPDを通したDNA鎖の移動が止まるかどうかで損傷の有無が確認され、修復反応を進めるかどうかを最終判断しているというメカニズムの詳細が今回の研究で明らかになった。実際、XPDの穴を通過できると予想される比較的軽微な損傷(塩基の脱離など)は、NERによる修復の対象にならないことが過去の研究で示されている。
NERの修復反応への理解進むほか、XPの治療法の開発にも貢献すると期待
今回の研究から、NERによるDNA損傷の修復過程で、XPA、XPB、XPDといったタンパク質のどの部分が、どのような働きをしているかが詳しく明らかになった。XPの患者で起こっている変異によってこれらのタンパク質に引き起こされる構造変化が、修復反応にどのような悪影響を及ぼして症状の発現につながっているのか、理解が格段に進むとともに、将来的には創薬などの治療法の開発にも貢献できる可能性がある。「特に日本ではXPAに変異を持つXPの患者の割合が圧倒的に高く、タンパク質の構造と機能の関係について理解が進むことは非常に大きな意義がある」と、研究グループは述べている。
▼関連リンク
・神戸大学 研究ニュース



