治療方法の限られるCBT、その遺伝学的背景を含めた検討は十分ではない
慶應義塾大学は3月1日、頸動脈小体腫瘍(Carotid Body Tumor:CBT)の遺伝学的検査およびタンパク質発現の解析を行い、その臨床遺伝学的な背景を解明したと発表した。この研究は、同大医学部耳鼻咽喉科学の小澤宏之教授、吉浜圭祐医師、東京医療センター聴覚・平衡覚研究部の松永達雄部長、慶應義塾大学医学部臨床遺伝学センターの小崎健次郎教授らの研究グループによるもの。研究成果は、「Clinical Genetics」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
CBTは、1年あたり約1000万人に1人が頸部に発症するまれな腫瘍である。頸動脈は脳に血流を送る重要な血管であり、CBTが増大すると頸動脈を取り囲むように進行し、脳血流障害や神経障害を引き起こす可能性がある。CBTを根治する方法は手術による切除しかないが、手術には大量出血・脳梗塞・神経障害などのリスクが伴う。従って年齢や基礎疾患によってはハイリスクな手術に耐えることができない場合がある。また、非常に大きくなったCBTでは、頸動脈以外にも周囲を走行する脳神経や頭蓋底骨を取り除く必要が生じることがあるため、手術時に合併症を生じるリスクが高く、摘出術を行うことが出来なくなることがある。さらに、CBTの一部の症例ではリンパ節および遠隔転移を認め、転移を伴う症例の5年生存率は50%と予後不良であると知られている。転移例や手術困難で根治方法がないCBTに対しての薬物治療や放射線治療などの効果は限定的で、今後は新規治療の開発が必要であり、その糸口となる新たな病態の解明が待たれている。
CBTは遺伝性腫瘍としての側面も知られており、その約10%は常染色体顕性(優性)遺伝の形式が想定される家族発症であると知られている。CBTを含めた頭頸部傍神経節腫の発症には、コハク酸脱水素酵素(Succinate dehydrogenase:SDH)のサブユニットタンパク質発現に必要な遺伝子をはじめ、いくつかの遺伝子の変異が関与するとされている。SDHはミトコンドリア内膜上に存在するタンパク質で、SDHA、SDHB、SDHC、SDHDの4つのサブユニットタンパク質からなり、それぞれSDHA、SDHB、SDHC、SDHDという遺伝子がその発現を司っている。これらの遺伝子の変異が細胞内の疑似的な低酸素を引き起こし、腫瘍を発生させるという仮説が報告されている。しかし、CBTの原因遺伝子がこのSDHだけなのか、他の遺伝子がどの程度関わっているのか、その頻度などについてまだ十分解明されていない。加えて遺伝性腫瘍は地域や人種による遺伝学的特徴の差異があると考えられている。日本でのCBTの臨床疫学的な特徴は、全国施設の症例登録により行われた全国調査(JCBTRG-1)により報告されたが、遺伝学的背景を含めた検討はない。遺伝学的検査を行った報告も症例報告に留まっており、日本およびアジアにおける遺伝学的特徴の解明が望まれている。
半数症例からSDHB、SDHA、SDHD、SDHAF2遺伝子に原因とみられる病的バリアント検出
研究グループは今回、同大大学病院でのCBT症例を対象にその遺伝学的背景を探り、さらに免疫組織化学を用いたタンパク質発現の評価と臨床所見の解析を行った結果から解明された分子遺伝学的な病態について報告を行った。
研究に同意されたCBT患者30名を対象に、末梢血DNAの遺伝学的検査を行った結果、15名(50%)に原因とみられる病的なバリアントが検出された。原因と判明した遺伝子はSDHB(7例、23%)、SDHA(4例、13%)、SDHD(3例、10%)、SDHAF2(1例、3%)だった。さらに、その他のがん関連遺伝子に合計68か所の病気との関係が不明なDNAバリアントを検出した。現時点で病気との関係が不明と判断されたDNAバリアントについては、今後の研究を継続することで新たにCBT発症や進展に関連について判明する可能性がある。
SDHD遺伝子を原因とする3名は全員がCBTの家族発症例(うち2名は同じ家系)だったが、その他の遺伝子を原因とする12名にCBTの家族発症例はなかった。SDHD遺伝子変異の保因者は他の原因遺伝子に比べてCBTの生涯発症率が高い可能性が示唆された。また、病的バリアントが検出された症例の中で、腫瘍切除を行った3例では、腫瘍組織から抽出したDNAの検査を行った。その結果、末梢血DNAでみられたものと同一のバリアントを認めたものの、腫瘍細胞が新たに獲得した体細胞変異は検出されなかった。これは常染色体顕性(優性)遺伝の遺伝性腫瘍の多くが持つKnudsonの2ヒット仮説に合致しない結果であり、今回の検査方法で検出できなかった何らかの体細胞変異が存在する可能性がある。
SDHBタンパク質発現解析により、知られていない新たな発症原因の存在が明らかに
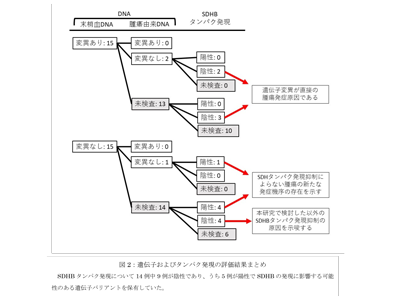
さらに、対象患者のうち手術治療を受けた腫瘍に対しては、SDHBタンパク質発現を評価するための免疫組織化学を行った。その結果、14例中9例でSDHBタンパク質発現が陰性であり、うち5例が末梢血DNAにSDHBの発現に影響する可能性のある遺伝子バリアントを保有していた。これはSDHに何らかの異常が生じるとSDHB発現が消失するとした欧米での既報の通りだった。SDHB免疫組織化学が陰性で末梢血DNAに病的なバリアントを保有しなかった4例では、今回の研究で検討したものの他に何らかのSDH発現を抑制する原因が存在する可能性が示唆された。一方、SDHB免疫組織化学が陽性であった残りの5例は、全て末梢血DNAに原因とみられるバリアントを検出せず、SDHの機能低下によらない新たなCBTの発症原因の存在を示すものだった。
傍神経節腫全体に研究を拡大し、発症や進展に関わるメカニズムの解明を目指す
今回、明らかにしたCBTの臨床遺伝学的背景は、この腫瘍の正確な診断と遺伝カウンセリングに活用できる。さらに研究グループは2022年に、頭頸部に発生する傍神経節腫を対象として「日本頭頸部傍神経節腫研究会」を立ち上げた。「CBTを始め、迷走神経傍神経節腫やグロムス腫瘍をふくめた頭頸部に発生する傍神経節腫全体に研究を拡大することで、本研究内容をさらに発展させ、腫瘍の発症や進展に関わるメカニズムの解明を目指している。これらの成果が将来には新規の治療法開発につながることを期待している」と、研究グループは述べている。
▼関連リンク
・慶應義塾大学 プレスリリース




