生活の質や生命予後を悪化させるがん悪液質、強力に抑制する方法は見つかっていない
京都大学は2月1日、1細胞トランスクリプトームと空間トランスクリプトームという二つの手法を組み合わせることで、がんが宿主個体の肝臓の空間的遺伝子発現パターンをかく乱することを発見したと発表した。この研究は、同大医生物学研究所のAlexis Vandenbon准教授、東京大学大学院新領域創成科学研究科の鈴木穣教授、東北大学加齢医学研究所の河岡慎平准教授(兼:京都大学医生物学研究所)、京都大学医学部附属病院、岐阜大学大学院医学系研究科、熊本大学大学院生命科学研究部らの研究グループによるもの。研究成果は、「Communications Biology」にオンライン掲載されている。
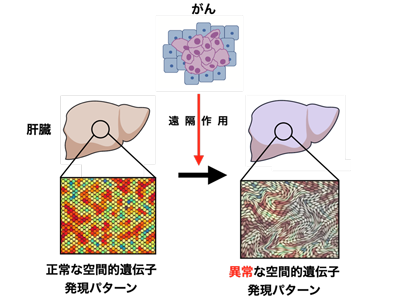
画像はリリースより
(詳細は▼関連リンクからご確認ください)
進行がんは身体にさまざまな悪影響を及ぼす。その実態は、宿主個体の臓器や細胞におけるがん依存的な異常の集まりである。これらの異常は臨床的にはがん悪液質として知られ、患者の生活の質や生命予後を著しく悪化させる。医療費を増大させることも知られており、がん悪液質を適切に制御する方法の開発が望まれている。
しかしながら現時点では、がんによって身体に生じる不調を強力に抑制する方法は見つかっていない。がんに起因する病態の全貌が正確に理解されていないことがその一因であると考えられる。研究グループは、がんに起因する不調に関わる宿主側の因子を見つける、というアプローチによってこの問題に取り組んできた。
がんによる肝臓への影響を、1細胞の解像度かつ空間的な構造を保持したまま解析
研究グループはこれまでに、がんが肝臓に与える影響に着目してきた。以前の研究では、がんを発生させたマウスの肝臓を採取し、これを破砕、肝臓に含まれる分子を抽出して分析するという手法を採用してきたが、これまでの手法には二つの課題があった。肝臓には肝細胞や免疫細胞など、さまざまな細胞が含まれている。肝臓全体を破砕して一挙に分析した場合、測定した分子がどの細胞に由来するかという情報を得ることはできない。また、肝臓には空間的に制御された構造が存在する。同じ肝細胞であっても、酸素や栄養を受け取りやすい位置にある肝細胞とそうでない肝細胞では、遺伝子の発現やその機能に違いがある。これまでの手法では、肝臓に含まれる一つ一つの細胞や空間的な遺伝子発現パターンに対してがんがどのように影響するのかを明らかにすることはできなかった。
今回、研究グループは、1細胞トランスクリプトームならびに空間トランスクリプトームという技術を用いて、この課題に取り組んだ。乳がんマウスモデルの肝臓を取り出し、がんによる肝臓への影響を、1細胞の解像度で、かつ、空間的な構造を保持したまま調べた。この二つのデータを統合的に解析することで、「1細胞の解像度」と「空間解像度」という二つの軸でこれまでの研究を発展させた。
乳がんマウスの肝臓、空間的な遺伝子発現のパターンが生物学的経路ごとに異なる様態で攪乱
その結果、乳がんマウスの肝臓において、空間的な遺伝子発現パターンが撹乱されていることがわかった。興味深いことに、この撹乱は、生物学的な経路ごとに固有だった。例えば、アスパラギン酸に関わる代謝は栄養・酸素に富んだ領域で活発であるが、アスパラギン酸代謝に関わる遺伝子の空間的な発現パターンは、がんによる影響をそれほど強く受けなかった。その一方で、解毒系の代謝経路は栄養・酸素に乏しい領域で活発であるが、このパターンはがんによってほぼ失われていた。このほか、急性期応答が栄養・酸素に富んだ領域で活発になっていることもわかった。以上、肝臓の空間的な遺伝子発現パターンが生物学的な経路ごとに異なる様態で撹乱されていることを発見した。空間的な肝機能制御という根本的なプロセスががんによって破綻するという新しい発見であり、今回の研究により、がんが肝臓に与える影響に関する理解を深める基盤を構築できたと考えている。
がんが肝臓に与える悪影響の全貌を理解する手法開発につながる
今回の研究を基盤として、がんが肝臓に与える悪影響の全貌を理解し、かつ、これを制御するための手法を開発したいと考えている。重要な課題として、今回の成果は一つのマウスモデルで得られたもので、今回の成果の一般性はこれから検証する必要がある。特に、ヒトで同様の異常が起こっているのかを明らかにすることが重要である。がんによる宿主の病態生理はさまざまな異常が関わる複雑なものである。「今回のような研究を積み重ねることで、がんによって全身に不調が生じるのはなぜか、がんによって命を落とすのはなぜなのか、という根本的な疑問に答えていきたいと考えている」と、研究グループは述べている。
▼関連リンク
・京都大学 最新の研究成果を知る



