血管平滑筋に発現のTRPC6に着目し、血管内皮細胞機能に関与しない新治療法開発へ
九州大学は12月16日、末梢循環障害後の血流回復を促すメカニズムを解明したと発表した。この研究は、同大大学院薬学研究院の西田基宏教授、加藤百合助教ら、自然科学研究機構生理学研究所/生命創成探究センター、信州大学、京都大学などの研究グループによるもの。研究成果は、「British Journal of Pharmacology」と「Cells」に掲載されている。
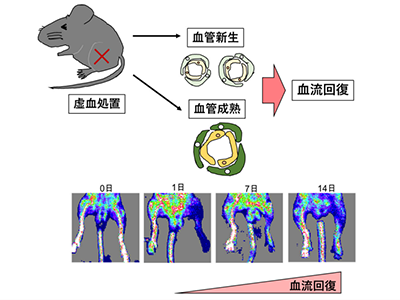
画像はリリースより
(詳細は▼関連リンクからご確認ください)
末梢血管の閉塞によって引き起こされる末梢循環障害は、高齢化社会が進むにつれて罹患者数も増加し続けている。現在、日本国内で末梢循環障害と推定されるのは600~700万人。閉塞の原因には加齢、動脈硬化や高脂血症、糖尿病などが挙げられ、複数の疾患を持つ人も多く、重篤化すると血流が滞るため血液供給を受けられなかった組織が壊死することもある。血管閉塞からの血流回復には、血管内皮細胞の活性化による血管新生やその後の血管の動脈化(血管平滑筋細胞の成熟)が重要と考えられてきた。しかし、現在使用されている治療薬は血管内皮細胞を標的とした血管拡張薬や抗凝血薬であり、加齢や疾患のため血管内皮細胞の機能が落ちている場合は、十分な効果が期待できなかった。
研究グループは、受容体活性型のCa2+透過型カチオンチャネルTRPC6の69番目のトレオニンをリン酸化することでチャネル活性を抑制し、血管平滑筋細胞の筋分化(血管成熟)を促進することを細胞レベルで明らかにしてきた。今回の研究では、血管平滑筋に発現するTRPC6に着目。遺伝子改変マウスを用いて、血管内皮細胞の機能に関与しない新たな治療法の開発を目指した。
TRPC6リン酸化によるチャネル活性阻害、血管新生・血管成熟を促す
マウス下肢の動脈を結紮し下肢虚血モデルを作製した結果、虚血肢において顕著なTRPC6のmRNA発現量の増加が見られた。野生型マウスと比べてTRPC6ノックアウトマウスでは血流回復が促進。このことから、TRPC6が虚血後の血流回復を妨げていることが明らかになった。また、虚血処置をした野生型マウスのTRPC6タンパク質をリン酸化させると、血流回復が促進され、さらに新生血管の指標であるCD31陽性血管数の上昇や血管平滑筋細胞が筋分化することで見られる血管径の増大が見られた。このことから、TRPC6のリン酸化によるチャネル活性阻害は血管新生や血管成熟を促すことがわかった。
下肢虚血後の血流回復、TRPC6阻害剤1-BPが最も強く促進
次に、TRPC6ノックアウトマウスの血管平滑筋特異的にTRPC6(野生型)、TRPC6リン酸化変異体(T69A:リン酸化阻害)を過剰発現させた遺伝子改変マウスを用いて虚血に対する血流回復効果を検証。その結果、TRPC6(野生型)を発現させたマウスではTRPC6をリン酸化することで血流回復が見られた。一方、TRPC6リン酸化変異体(T69A)を発現させたマウスでは回復効果は見られなかった。
血管内皮機能障害をもつ動脈硬化モデルApoEノックアウトマウスに虚血処置をして、TRPC6阻害剤を投与。その結果、野生型マウスと同様に血流が回復したことから、マウスにおいて血管内皮機能に依存せずTRPC6チャネル活性を抑制することで血流回復を促していることが明らかになった。さらに、TRPC6阻害剤の中から最も強く血流回復を促進する化合物1-BPを見出した。
以上の結果から、末梢循環障害後、TRPC6を阻害することで血管内皮細胞の機能に関係なく血管を新生し、さらに血管の成熟を促進させることが示唆された。
加齢や生活習慣などの患者背景に依存しない、末梢循環障害治療の新たな可能性
今回の研究により、末梢循環障害に対して血管内皮細胞の機能が落ちている場合にでも有効な新たな治療標的としてTRPC6を見出した。今回の発見は、加齢や生活習慣など様々な患者背景に依存しない末梢循環障害治療の新たな可能性を提案するものとして期待されるという。TRPC6阻害によって誘導される新生血管数の増大や血管成熟のメカニズムは不明なため、これから明らかにしていく必要がある。今後は、より特異的なTRPC6阻害剤を探索し、複数の疾患を持つ患者でも使用可能な有用な治療薬を探索していく予定だ、と研究グループは述べている。
▼関連リンク
・九州大学 プレスリリース




