慢性心不全にかかる医療費負担は世界的な問題
東京大学医学部附属病院は11月18日、心筋梗塞後に心臓の中のどこにある細胞がどのような遺伝子を働かせているかを経時的に明らかにし、心筋梗塞後の急性期に梗塞領域の周辺の心筋細胞でCsrp3というメカノストレス応答遺伝子が活性化し、それが慢性期に生じる心機能の悪化を防ぐ役割を果たすことを解明したと発表した。この研究は、同大病院循環器内科の候聡志特任助教、野村征太郎特任助教、山田臣太郎特任研究員、初瀬慧医師、小室一成教授、東京大学の油谷浩幸名誉教授らの研究グループによるもの。研究成果は、「Nature Cardiovascular Research」に掲載されている。
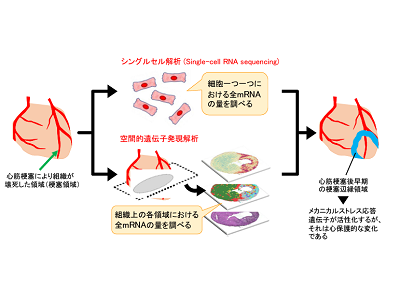
画像はリリースより
(詳細は▼関連リンクからご確認ください)
心筋梗塞は、心臓に血液を供給する冠動脈が閉塞することで生じる代表的な循環器疾患の一つ。日本では年間7万人以上が罹患し、カテーテル治療をはじめとした急性期治療の進歩により救命率は向上しているものの、依然として年間6,000人以上が亡くなっているのが実情だ。また、たとえ急性期でうまく救命できても、その後に慢性心不全を来すことが多く、その医療費負担は日本のみならず世界的に問題となっている。
シングルセル解析と空間的遺伝子発現解析を用いて、心臓の各領域で生じる変化を解析
心筋梗塞のこれまでの基礎研究は、心臓全体で生じる変化を解析する研究がほとんどであり、心筋梗塞が生じた領域・その周囲の領域・遠隔領域といった心臓の各領域で生じる変化の違いを時系列的に解析する研究はほとんどなかった。
そこで今回研究グループは、シングルセル解析と空間的遺伝子発現解析という手法を用い、心筋梗塞後に心臓の各領域に存在する細胞で時系列的に働く遺伝子の変化を網羅的に調べた。通常シングルセル解析では、分析した細胞が元々組織内のどこに存在していたかがわからなくなってしまうが、空間的遺伝子発現解析の手法を併用することで、この制約を克服した。
心筋梗塞後の急性期、梗塞領域周辺の心筋細胞でCsrp3などのメカノストレス応答遺伝子が活性化
その結果、心筋梗塞後翌日の心臓では、梗塞領域の周辺に存在する心筋細胞で特異的にメカノストレス応答遺伝子が活性化することが明らかとなった。そのうちの代表的な遺伝子としてCsrp3に着目。心筋梗塞後のマウスの心臓でその働きを活性化もしくは抑制すると、メカノストレス応答が活性化もしくは抑制され、慢性期に生じる心不全が改善もしくは悪化することがわかった。つまり、心筋梗塞後の梗塞領域周囲で急性期に生じるメカノストレス応答の活性化は心機能の悪化を防ぐ役割があると考えられた。
Csrp3は、心筋や骨格筋における収縮単位であるサルコメアを構成するタンパク質MLP(Muscle LIM protein)をコードする遺伝子。細胞が周囲から機械的な刺激を受けるとそれを感受してこの遺伝子の働きが活性化する。また、この遺伝子の変異は肥大型心筋症や拡張型心筋症といった心臓疾患の発症につながることが知られている。
Csrp3活性化による慢性期心機能悪化を防ぐ治療法の開発が期待される
研究で見出されたCsrp3は、心筋梗塞における新しい治療標的分子と考えられ、その働きを活性化させることで慢性期の心機能悪化を防ぐ治療法開発につながると期待される。また、研究に用いたシングルセル解析や空間遺伝子発現解析のデータは同分野の新たな研究開発に役立つと期待される。「研究ではマウスを用いて心筋梗塞の病態を解析したが、今後はヒト組織検体をシングルセル解析と空間的遺伝子発現解析の統合解析によってさまざまな循環器疾患の病態を明らかにしていきたい」と、研究グループは述べている。
▼関連リンク
・東京大学医学部附属病院 プレスリリース



