開発した「PAS-CPP-GLP-2」は経鼻投与後、どのような経路で作用部位に到達するのか?
東京理科大学は11月14日、神経ペプチド誘導体「PAS-CPP-GLP-2」を経鼻投与すると、鼻腔から三叉神経を介して神経細胞を乗り継ぎ、中枢神経へと効率よく移行することを明らかにしたと発表した。この研究は、同大薬学部生命創薬科学科の山下親正教授、秋田智后講師らの研究グループによるもの。研究成果は、「Journal of Controlled Release」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
うつ病など中枢神経系疾患の多くが、アンメット・メディカル・ニーズの高い疾患だ。有効な治療薬開発のためにBBBを回避して、薬剤を作用部位である中枢神経に確実に送達するDDSとして経鼻投与が注目され、過去数十年に渡り研究が続けられている。しかし、経鼻投与による中枢神経へのDDS技術は、いまだ実用化されていない。その主な要因として、これまでの研究ではヒトの鼻粘膜構造のわずか2%にすぎない嗅上皮の嗅球を介した経路に着目していたことがあげられる。
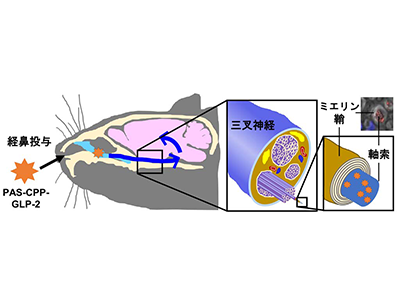
そこで研究グループは、鼻粘膜構造の98%を占める「呼吸上皮を経由する経路」に着目した。しかし、神経細胞では軸索輸送が非常に遅いという問題があり、また、三叉神経の周囲には毛細血管が多く存在するため、薬剤が血管に入り全身へ運ばれてしまうという問題があった。
研究グループは、抗うつ様作用が認められるグルカゴン様ペプチド(GLP-2)に、機能性配列(膜透過性促進配列CPP、エンドソーム脱出促進配列PAS)を付加することで、これらの課題をクリアし、鼻腔から効率良く呼吸上皮の三叉神経に取り込まれ、作用部位まで神経細胞を乗り継いで中枢を移行する、新規の神経ペプチド誘導体「PAS-CPP-GLP-2」を創製した。PAS-CPP-GLP-2を経鼻投与した場合、脳室内投与と同じ用量で抗うつ様作用を発揮することが報告されている。そこで研究グループは今回、この高い薬理効果の背景にある機序を解明するべく、この神経ペプチド誘導体が、どのような経路で作用部位に到達するかを詳細に調べた。
IN投与では血管周囲腔に分布せず、脳脊髄液を介さない経路の関与が示唆
まず、PAS-CPP-GLP-2(以下、GLP-2誘導体)を、マウス脳室内(intracerebroventricular, ICV)投与、または経鼻(intranasal, IN)投与し、脳全体への移行量をELISA法で定量した。すると、IN投与した場合には検出限界以下であったのに対し、ICV投与では多量のGLP-2誘導体が脳内に検出された。
以前の研究で、IN投与したGLP-2誘導体はICV投与と同用量で抗うつ様作用を示した。そこで、IN投与では、脳内移行量が少ないにも関わらず、ICV投与と同用量で薬理効果が生じた理由を明らかにするため、各投与による中枢移行経路の違いに着目した。
脳室内は脳脊髄液で満たされているため、ICV投与した場合に薬剤はまず、脳脊髄液中で拡散する。また、IN投与した場合にも、嗅上皮細胞の細胞間隙から脳脊髄液へと拡散する。そこで次に、脳脊髄液中のGLP-2誘導体濃度を測定した。投与から5分後、ICV投与群では脳脊髄液中にGLP-2誘導体が検出されたが、IN投与群では検出されなかった。また、投与から20分後には、ICV投与群、IN投与群ともにGLP-2誘導体は検出されなかったという。
脳脊髄液は、血管周囲腔(毛細血管の外側を囲む空間)にも常に流れ込んでいる。そこで、さらに海馬の血管周囲腔におけるGLP-2誘導体分布を調べた。すると、ICV投与群で、特に多くのGLP-2誘導体が血管周囲腔に分布していた。このことから、ICV投与では、脳脊髄液中に拡散したGLP-2誘導体は、血管周囲腔へと移行することが示唆された。一方、IN投与群では血管周囲腔には分布していなかった。このことから、IN投与では、脳脊髄液を介さない経路が関与することが示唆された。
IN投与<三叉神経の軸索から取り込み<神経回路に沿って移行<海馬や視床下部に到達
そこで、IN投与した場合のGLP-2誘導体の経時的脳内分布を調べ、また、その時点での抗うつ様作用を強制水泳試験(forced swim test, FST)によって調べた。GLP-2誘導体は、投与3分後、三叉神経主知覚核(橋)で観察された。しかし、その時点では、FSTの結果に抗うつ様作用はみられなかった。投与5分後および10分後、GLP-2誘導体は、三叉神経主知覚核に加えて、嗅球でも観察された。しかし、この時点でもFSTに抗うつ様作用はみられなかった。投与20分後、GLP-2誘導体は、作用部位である海馬および視床下部で観察された。この時、FST結果において無動時間が有意に減少し、抗うつ様作用を示した。これらの結果から、GLP-2誘導体は、三叉神経を介して海馬や視床下部に到達し、抗うつ様作用を示したものと推察された。
最後に、GLP-2誘導体をIN投与した5分後、マウスから三叉神経を回収し、顕微鏡で観察した。すると、GLP-2誘導体は三叉神経節で観察された。このときに神経内部を見ると、GLP-2誘導体は軸索中に観察された。また、経鼻投与されたGLP-2誘導体は三叉神経を通り、さらに三叉神経毛帯に到達することが確認された。
これらの結果は、IN投与されたGLP-2誘導体が三叉神経の軸索に取り込まれ、神経回路に沿って神経細胞を乗り継いで移行し、海馬や視床下部にまで到達したことを示すという。
アンメット・メディカル・ニーズの高い神経変性疾患への適用に期待
今回の研究成果は、DDS研究と神経科学の既成概念を覆す、全く新しい概念の中枢デリバリー技術だと言える。山下教授は「現在、このシステムをうつ病だけでなく、アルツハイマー病などへ適用できる可能性を示唆するデータも得られている。このDDS技術は、種々の神経ペプチドに適用できるだけでなく、神経細胞へと効率よく取り込ませることができるため、アンメット・メディカル・ニーズの高い神経変性疾患への適用が期待される」と、同研究の応用可能性を述べている。
▼関連リンク
・東京理科大学 プレスリリース



