BCR-ABL1チロシンキナーゼ阻害剤は効果に個人差
東京大学は10月14日、慢性骨髄性白血病(chronic myeloid leukemia, CML)の治療薬であるニロチニブの治療効果を患者ごとにかつ早期に予測できる数理モデルを開発したと発表した。この研究は、同大生産技術研究所の岡本有司特任研究員(研究開始当時、現在:京都大学医学研究科特定助教)、梶田真司助教(研究開始当時、現在:福井大学学術研究院工学系部門助教)、合原一幸教授(研究開始当時、現在:東京大学特別教授・名誉教授/東京大学国際高等研究所ニューロインテリジェンス国際研究機構副機構長)、同大医科学研究所の東條有伸教授(研究開始当時、現在:東京医科歯科大学理事・副学長)らの研究グループによるもの。研究成果は、「npj Systems Biology and Applications」に掲載されている。
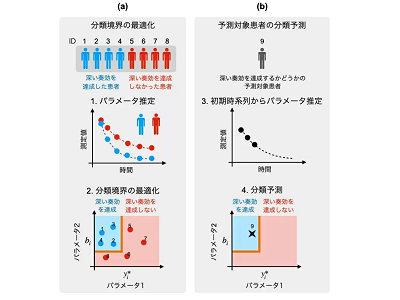
画像はリリースより
(詳細は▼関連リンクからご確認ください)
慢性骨髄性白血病は、白血球、赤血球、血小板などの基となる造血幹細胞の異常により発症する白血病である。この異常な造血幹細胞から分化してできる白血病細胞(以下、CML細胞)は二つの染色体間の相互転座によって形成されたBCR-ABL1融合遺伝子をもち、この遺伝子が作る酵素チロシンキナーゼの異常な活性化によりCML細胞の無秩序な増殖が起こる。現在はBCR-ABL1チロシンキナーゼ阻害剤(TKI)と呼ばれる有望なCML治療薬があり、これがBCR-ABL1融合遺伝子によるチロシンキナーゼの活性化を抑制することでCML細胞を大幅に減少させることができる。実際にTKIは多くのCML患者の予後を改善するが、一方でその効果には個人差があることも知られている。
別のTKIへの切り替えが治療選択肢に、早期予測可能な数理モデルが必要
CMLの治療効果には、国際標準(International Scale, IS)値と呼ばれる指標が用いられている。IS値はBCR-ABL1融合遺伝子の発現量を反映したもので、血液検査で測定することができる。CML治療によって、CML細胞の量が十分減少し、深い奏効(deep molecular response, DMR)を得られると、IS値も十分小さくなる。CML治療の実際的な目標はTKIの導入によって深い奏効を達成することといえる。
現在、新たに診断されたCML患者に投与されるTKIには、第一世代TKIであるイマチニブ、さらに第二世代TKIのダサチニブ、ニロチニブ、ボスチニブがある。投与中のTKIの効果が乏しい場合は、別のTKIへの切り替えが治療選択肢となる可能性がある。したがって、TKI療法の効果を患者ごとに早期に予測できる数理モデルが求められている。
末梢血中のCML細胞の量の時間変化に焦点を当てたモデル
今回研究グループは、短い時系列データからCML患者ごとのニロチニブの有効性を予測できる数理モデルを提案した。具体的には、ニロチニブ投与開始時と開始後3、6か月目のIS値と末梢血中の総白血球細胞の量から、ニロチニブ投与開始後2年以内にCML患者が深い奏効を達成するかどうかを推定できる分類方法を構築した。成功の鍵は、末梢血中のCML細胞の量の時間変化に焦点を当てたことだ。
まず、CML細胞と正常な白血球の末梢血中の量の時間変化を4つのパラメータからなる、単純な常微分方程式モデルで表現した。このパラメータを患者ごとに変えることで、患者ごとのCML細胞と正常な白血球の末梢血中の量の時間変化をシミュレーション可能にした。しかし、一般的な血液検査ではCML細胞と正常な白血球を区別して測定することはでない。そこで、測定可能なIS値と総白血球細胞の末梢血中の量から、直接測定できないCML細胞と正常な白血球の末梢血中の量を推定する数理モデルを開発した。
約94%という高い正解率で深い奏効の達成の有無を予測
次に、慢性骨髄性白血病患者を対象にした臨床試験N-road studyのデータを用いて、個々のCML患者のIS値と末梢血中の総白血球細胞の量の2年分の時系列データから、CML細胞の量に関する常微分方程式モデルのパラメータを患者ごとに推定した。その結果、この推定パラメータに基づき、深い奏効を達成した患者と深い奏効を達成できなかった患者に分類できることがわかった。
さらに、患者を分類モデルの学習用グループと奏効予測用グループに分割。まず、学習用グループの患者の2年分の時系列データから推定された個々の患者のパラメータ値と深い奏効の達成の有無に基づき、分類境界を最適化して決定した。その後、予測用グループの患者の6か月目までのデータから予測対象患者のパラメータ値を推定し、分類境界に基づく深い奏効の達成の有無を予測した。その結果、MR4.5と呼ばれる深い奏効の基準では、最適な分類境界決定法を用いた場合、約94%という高い正解率で深い奏効の達成の有無を予測することができた。
大規模データによる検証、他TKIへの適用の検討により実用化の可能性
研究で開発した数理モデルを用いることで、CMLの患者がTKIの内服を開始してから2年以内に深い奏効を達成できるかどうかを、6か月という短期間で、また一般的な血液検査のデータを使うことだけで、患者ごとに予測できる可能性がひらかれた。これにより、ある患者がニロチニブでは効果に乏しいと予測された場合、ニロチニブ以外のTKIに切り替えるなど、深い奏効の達成に向けて患者ごとに治療法を最適化する個別化医療への展開が期待される。
ただし、実用化にはいくつかの課題がある。一点目は被験者数の課題である。N-road studyの被験者のうち基準に適合した患者32人のデータを使用したが、今後、より大規模な臨床試験のデータを用いて有効性を検証することが必要だ。二点目は、ニロチニブ以外のTKIへの適用可能性である。「ニロチニブのみで有効性を検証しているため、今後はニロチニブ以外のTKIへの有効性を確認することで、より包括的なCMLの個別化医療の実現が可能になると考えられる」と、研究グループは述べている。




