特殊な形態的特徴を持つ肝臓の肝類洞内皮細胞とがん細胞の相互作用に着目
大阪公立大学は9月29日、がん細胞が肝臓へ転移する経路を特定し、それに関わる分子機構を明らかにしたと発表した。この研究は、同大大学院医学研究科肝胆膵病態内科学のTruong Huu Hoang大学院生、河田則文教授、獣医学研究科獣医学専攻の松原三佐子准教授らの研究グループによるもの。研究成果は、「Science Advances」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
がん関連死の約90%は転移が原因であり、肝臓は、胃腸の悪性腫瘍、黒色腫、乳がんおよび肉腫などさまざまな臓器由来のがん細胞が最も転移しやすい臓器。さらに、肝転移切除後の5年生存率は30~50%と低く、転移を抑制する治療法の開発は急務である。一般に、がん細胞の転移初期段階には微小環境が複雑に相互作用し、がん細胞の転移を助長している可能性がある。その中でも、特にがん細胞と肝類洞内皮細胞(LSEC)との相互作用を理解することは、がん細胞の肝臓への転移を阻害することを目的とした新しい治療薬を開発する上で重要だ。
LSECは肝臓の毛細血管内皮細胞であり、細胞質に直径100~150 nmの多数の小孔(フェネストラ)を有し、基底膜を欠くなど他の血管内皮細胞と異なる特徴的な形態を有する。LSECはこの無数に開いた小孔を通して血液の液性成分やカイロミクロンのような小粒子を自由に肝細胞側へ取り込むことができる。同時に、体内の解毒機能を担うLSECは、血液から運ばれる有毒物質に絶えず晒されている。そのため、化学療法や一部の化学物質による病理学的条件下において、フェネストラの破壊が起こり、細胞内のギャップ形成(iGap、直径200nm以上)が生じる。研究グループは、このようなLSECの特殊な形態的特徴に着目し、がん細胞との細胞間相互作用メカニズムを詳細に調べることで、転移に関する新しい現象を明らかにした。
肝転移マウスモデルで、がん細胞がLSEC-iGap形成を誘導し肝臓内へ侵入する現象を捉えた
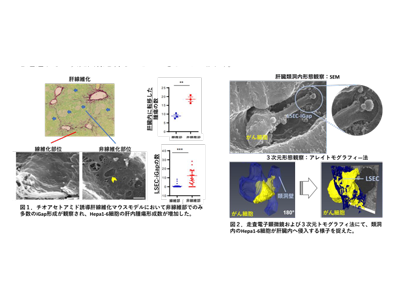
研究では、初めにマウス肝がん細胞由来のHepa1-6細胞株を脾臓内に注入し、in vivoの肝転移マウスモデルを作製した。まず、LSECのiGap形成を誘導することが知られているアセトアミノフェン(APAP)を注射した6時間後、LSECを走査電子顕微鏡で観察するとLSEC-iGap形成は対象群に比べ、APAP投与群で有意に増加した。また、HE染色像から、APAP投与3日後の観察により、APAP投与群で肝臓内の腫瘍形成数の増加を認めた。次に、チオアセトアミド誘導肝線維化マウスモデルを作製し、同上の方法でHepa1-6細胞を脾臓内に注入後、肝臓内の転移巣の局在を調べた。その結果、非線維部で多数のiGapが形成され、その非線維部では線維部に比べて転移Hepa1-6細胞由来の腫瘍数が有意に増加していた。そこで、Hepa1-6細胞を脾臓内に注入した6時間後に肝類洞内を走査電子顕微鏡で観察したところ、がん細胞の肝臓実質内への侵入像を捉えることに成功した。また、がん細胞の侵入像をより詳細に観察をするためにアレイトモグラフィ法を用いて1個のがん細胞が1個のLSEC内を通過する3次元画像を得ることができた。
MMP阻害剤はiGap形成を消失し肝内腫瘍形成を大幅に減少
さらに、がん細胞とLSECを共培養して遺伝子解析を行った結果、Hepa1-6細胞ではIL-23が発現上昇し、LSECではTNF-αシグナルが活性化した。また、TNF-αシグナルの下流分子である、MMP9、ICAM1、炎症性サイトカインの発現が誘導された。さらに、リコンビナントTNF-αおよびがん細胞との共培養によりLSECのF-アクチン脱重合が起こることでiGap形成が観察され、TNF-α中和抗体によりこの現象は抑制された。ヒトにおいて肝細胞がん(HCC)の血管侵入を伴うHCC患者の外科的手術組織検体を用いてMMP9とICAM1発現を調べたところ、これらの分子の発現は肝がんの肝内転移数および患者の全生存率と相関した。さらに、腫瘍部におけるMMP9の高発現は無再発生存期間と負の相関を示した。これらの結果を基に、MMP発現誘導剤(MCT)を培養LSECに投与するとiGap形成は促進し、一方、MMP阻害剤およびMMP2/9低分子阻害剤はiGap形成を消失させた。また、これらの阻害剤はHepa1-6細胞の肝内腫瘍形成を大幅に減少させた。この結果は、がん転移を防ぐための治療標的としてMMP9が有望であることを示唆している。以上の研究成果により、「がん細胞がLSECにおけるiGap形成をTNF-α-MMP9経路で惹起し、iGapを介して肝実質内へ侵入する」という転移に関する新しい現象を明らかにした。
研究グループは、「研究は、iGap形成を阻害する薬剤はがん転移の予防や治療につながる可能性があるという、今までにない視点に基づく研究であり、今後の抗がん転移治療法の開発に大きく貢献する。また、既に世界の研究グループによるマウス実験の結果からMMP9を標的とした治療薬の有効性が期待され、がんや線維症など慢性疾患に対する臨床治験が進んでいるが、多くの薬は副作用が問題となり中止となっている。そこでMMP9の局所的な作用をさらに明らかにできれば副作用を軽減した薬の開発につながると考え、MMP9を標的とした新しい治療薬の開発を目指す」と、述べている。
▼関連リンク
・大阪公立大学 プレスリリース




