がん免疫療法の妨げになる免疫関連副作用、特に皮膚炎の頻度が高い
東京医科歯科大学は7月15日、がん免疫療法の際の乾癬悪化の原因が、皮膚常在ランゲルハンス細胞上の免疫チェックポイント分子PD-L1をブロックしてしまうことによることをつきとめたと発表した。この研究は、同大大学院医歯学総合研究科皮膚科学分野の沖山奈緒子教授、筑波大学らの研究グループによるもの。研究成果は「The Journal of Investigative Dermatology」誌にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
現在、がん免疫療法が多くのがん治療に応用され、その高い効果が期待されている。がん免疫療法では、免疫チェックポイント分子と呼ばれる免疫抑制性分子に対する抗体医薬が使われており、がんを攻撃するT細胞というリンパ球上に発現しているPD-1と、その刺激分子であるPD-L1、また樹状細胞という抗原提示細胞が発現する免疫刺激分子がT細胞に働きかけることを邪魔しているCTLA-4といった分子が標的となっている。その治療効果の一方で、人工的な免疫賦活化による免疫関連副作用と呼ばれる現象が、がん免疫療法の妨げとなっており、特に皮膚炎は最も頻度が高く、がん患者の治療意欲をそいでいるという。
副作用に含まれる乾癬、PD-1-PD-L1進展抑制機構の詳細は不明
乾癬は慢性炎症性皮膚疾患であり、鱗屑を多く付すくっきりした紅斑が多発し、爪の変形を来し、時にリウマチのような関節炎を伴う。インターロイキン(IL)-17を産生する自然リンパ球γδ T細胞や、獲得免疫系リンパ球の一つであるTh17細胞が皮膚炎を形成しており、この病原性細胞はIL-23を産生する表皮常在ランゲルハンス細胞や真皮樹状細胞といった抗原提示能を持つ細胞が誘導していると説明されている。そのため、治療薬として、IL-17やIL-23を標的とした抗体医薬が広く使われる。
がん免疫療法に伴う皮膚の免疫関連副作用には乾癬が含まれ、もともとある乾癬を急激に悪化させる場合と、初めて発症させてしまう場合がある。研究グループは、この免疫関連副作用としての乾癬は、がん免疫療法によって、細胞傷害性T細胞と呼ばれるリンパ球上の免疫チェックポイント分子PD-1が遮断されて異常に活性化し、皮膚を攻撃することから始まること、PD-1に対する刺激分子としてはPD-L1とPD-L2があるが特にPD-L1が乾癬の発症を抑えていることを報告している。しかし、この乾癬の進展抑制機構であるPD-1-PD-L1機構において、どの細胞が発現するPD-L1が特に重要であるかなどは不明だった。
ランゲルハンス細胞でのPD-L1ノックアウトにより重症化した乾癬を発症
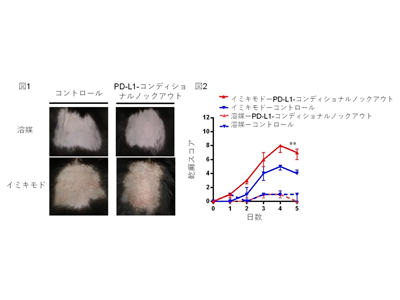
乾癬のモデルマウスとして、イミキモド(自然免疫活性化剤)塗布誘導乾癬様皮膚炎が最も広く用いられている。今回、研究グループがこのイミキモド誘導乾癬様皮膚炎マウス病変部皮膚にて、PD-L1を発現している細胞を探索したところ、表皮角化細胞、表皮常在ランゲルハンス細胞、真皮樹状細胞など多くの細胞が発現していた。そこで、乾癬の発症において、所属リンパ節に遊走して病原性γδ T細胞の誘導・活性化に大きな役割を果たすとされるランゲルハンス細胞に着目した。CRISPR-Cas9という遺伝子改変技術を用い、PD-L1をLoxPで囲む遺伝子改変マウスを新規に作出し、ランゲルハンス細胞特異的マーカーLangerinとともにCre酵素を発現させたマウスと掛け合わせることで、ランゲルハンス細胞上でのみPD-L1を遺伝子的に欠損させたコンディショナルノックアウトマウスを作製した。このLangerin-PD-L1コンディショナルノックアウトマウスへ、イミキモド誘導乾癬様皮膚炎を惹起したところ、明確に重症化した乾癬を発症した。
また、コンディショナルノックアウトマウスでは、野生型コントロールマウスと比べ、皮膚にはγδ T細胞が多く浸潤し、この細胞はよりIL-17産生能が高いこと、さらにその所属リンパ節では、表皮向性のある病原性γδ T細胞が特に増多・活性化していることを見出した。
これらの結果は、ランゲルハンス細胞は特に所属リンパ節でγδ T細胞を活性化して乾癬の病態を成立させているが、PD-L1も同時に発現してブレーキをかけている一方、PD-L1シグナルが遮断された状態ではこのブレーキがなく、いわゆる「タガが外れた」状態になっており、これががん免疫療法における免疫関連副作用としての乾癬で起こっている状態と考えられるという。
副作用として起きている乾癬だけでなく一般的な乾癬も説明できる
今回の研究において、一般の乾癬、またがん免疫療法の免疫関連副作用として起きている乾癬、双方を説明する免疫制御機構を、新しい遺伝子改変技術を用いて明確に示すことができた。「この結果は、通常の乾癬においてはランゲルハンス細胞上のPD-L1発現を上昇させるような治療ストラテジーの確立、またがん免疫療法においてはランゲルハンス細胞上のPD-L1シグナル遮断を回避することで、皮膚免疫関連副作用を回避するという、ブラッシュアップストラテジーへ発展していくことが期待される」と、研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース



