PD-1阻害療法の有害事象、原因となる免疫応答やその発生機序は未解明
京都大学は7月13日、免疫チェックポイント阻害療法に伴う有害事象(免疫関連有害事象、immune-related adverse events;irAE)の発現に関わる免疫応答の誘導メカニズムの一端を明らかにしたと発表した。この研究は、同大がん免疫総合研究センターの塚本博丈特定准教授、熊本大学、虎ノ門病院の共同研究グループによるもの。研究成果は「Proceedings of the National
Academy of Sciences of the United States of America」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
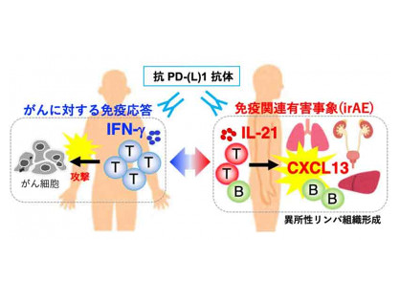
現在、がん免疫療法の主流となっているPD-1阻害療法は、がんに対する免疫を強く活性化すると同時に、通常は抑制されている自己の組織に対する免疫応答も同時に活性化するリスクがある。この免疫応答を介した自己組織の傷害はirAEと呼ばれ、がん免疫療法の副反応として、がん患者のさまざまな臓器に現れる。重篤な症状が発生する場合には治療の中断も余儀なくされるが、irAEの原因となる免疫応答の本体、およびその発生機序は明らかにされていない。
老齢の担がんマウスに対するPD-1阻害療法で異所性リンパ組織形成、臓器傷害が起こることを確認
irAEの原因となる免疫応答の解析、実態解明には、実験動物が有用であると考えられるが、がんを有する若いマウスではPD-1阻害療法の抗がん効果が観察される一方、正常臓器には病理学的変化、機能的変化は何も観察されない。つまり、若い担がんマウスモデルではirAEを再現できず、irAEの詳細な解析に利用できない。
そこで研究グループは、がん患者の多くが高齢であるということに着目して、より実臨床に近い、がんを有する老齢のマウスに対してPD-1阻害療法を行い、正常臓器を解析した。その結果、担がん老齢マウスの肺、肝臓、腎臓において、若いマウスでは観察されないCD4陽性T細胞、CD8陽性T細胞、B細胞の異常な集積(異所性リンパ組織)が観察された。さらにPD-1阻害療法を受けた老齢マウスのこれらの臓器では抗体の沈着が観察され、臓器の傷害、ダメージが起こっていることがわかった。そのため、担がん老齢マウスを用いたこの実験系は、従来の若いマウスでは見られないヒトirAE病態を模倣する臓器傷害と、それをもたらす免疫反応を解析できる有用なモデルとなると考えられた。
CD4T細胞、B細胞の活性化を介してirAE様症状が発生、抗腫瘍免疫応答に必須であるIFN-γは必須ではない
次に、新たに樹立したこの実験モデルを用い、PD-1阻害療法に伴う臓器傷害を引き起こす免疫応答について、さらに解析を行った結果、老齢担がんマウスのCD4陽性T細胞あるいはB細胞を体内から除去すると、正常臓器における異所性リンパ組織の形成、抗体沈着が消失した。さらに、irAE症状を起こした老齢マウスの血清から精製した免疫グロブリンを、無処理の若齢および老齢マウスへ移入すると、老齢マウスの臓器にのみ免疫グロブリンの沈着が観察され、irAE症状の移行が観察された。つまり、CD4T細胞、B細胞の活性化を介して誘導された自己抗体が老齢組織に沈着することによりirAE様症状が起こることが示唆された。
irAE臓器である肺に集積するCD4T細胞はIFN-γ、およびIL-21を強く産生することから、老齢のIL-21欠損マウスあるいは老齢のIFN-γ欠損マウスを作成し、それぞれのirAE症状を観察した。その結果、IL-21は老齢個体で観察されるPD-1阻害療法に伴う臓器傷害、異所性リンパ組織形成、抗体沈着を誘導する上で必要であることが明らかになった。一方で、がんに対する免疫応答に必須であるIFN-γについては、irAE様症状発現に必須ではなく、抗腫瘍免疫応答とirAEを誘導する免疫応答は質的に同一でないことが示唆された。そして、irAE臓器で発現上昇し、IL-21により制御される因子を網羅的な遺伝子発現解析により探索したところ、B細胞の遊走因子(ケモカイン)であるCXCL13が、IL-21を産生するCD4T細胞により発現上昇する候補分子として選出された。そして、CXCL13の活性を阻害する実験により、実際にCXCL13がPD1阻害療法に伴う異所性リンパ組織形成、および臓器傷害に寄与することがわかった。
irAE誘導機序の解明や新たなirAEマネジメント戦略の構築につなげる
今後、さまざまな治療戦略との併用を含めPD-1阻害療法はさらに普及が進むと考えられ、がんに対する免疫応答とirAEを誘導する免疫応答の質的違いを見極められる知見を蓄積し、irAEの発症リスクを予測すること、そしてirAEを引き起こす免疫応答のみを制御する方法の開発が求められる。「今回の研究は、irAE発症に関わると思われる免疫応答の一端を明らかにしたに過ぎず、樹立した実験モデルの解析をさらに進めることによりirAE誘導機序の解明、そして新たなirAEマネジメント戦略の構築につなげたい」と、研究グループは述べている。
▼関連リンク
・京都大学 最新の研究成果を知る




