多くの腫瘍組織でcGASまたはSTINGの発現抑制、膵臓がんとの関連を検討
東京医科歯科大学は6月30日、膵臓がんにおけるcGAS-STINGシグナルが、がん間質細胞との相互作用に関与し、がん細胞への細胞傷害性T細胞の浸潤を促進することを明らかにしたと発表した。この研究は、同大大学院医歯学総合研究科分子腫瘍医学分野の田中真二教授と新部(樺嶋)彩乃助教の研究グループと、肝胆膵外科学の田邉稔教授、東北大学大学院医学系研究科消化器病態学の正宗淳教授らとの共同研究によるもの。研究成果は、「Scientific Reports」に掲載されている。
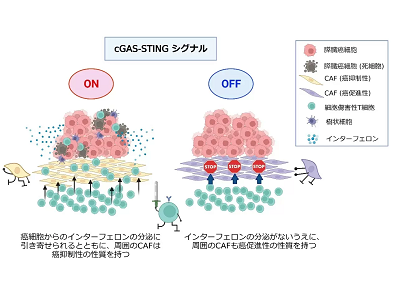
画像はリリースより
(詳細は▼関連リンクからご確認ください)
膵臓がんは、腫瘍組織内にがん関連線維芽細胞(Cancer-associated fibroblasts:CAFs)、コラーゲンなどの細胞外基質からなる、多くの間質組織を含むことが特徴だ。膵臓がん組織は血流に乏しいことから、がん細胞局所への薬剤や免疫細胞の到達が障害されていることも考えられ、膵臓がんが一般的に「治療がしにくい」腫瘍であることの一因ともなっている。がん間質からは腫瘍細胞の増殖を促進する因子が分泌され、がんの進展を促進すると長年考えられてきたが、近年、腫瘍組織を構成するCAFにも多様性(heterogeneity)が存在することが示され、研究が進んでいる。
cGAS-STINGシグナルは、ウイルス感染などの際、インターフェロン産生を促すことで周囲の免疫反応を活性化させる生体防御シグナルの1つ。近年このシグナルが腫瘍免疫にも関与していることを示す論文が報告されている。多くの腫瘍組織ではシグナル構成因子であるcGASまたはSTINGの発現が抑制されていることも多く、このシグナルの活性化が腫瘍免疫反応を取り戻すためのキーともなっている。そこで研究グループは、膵臓がんにおけるcGAS-STINGシグナルが関与する免疫反応と間質細胞の相互作用について検討した。
78例の手術組織を解析、cGAS/STING両方発現群の生存率が有意に「高」
研究グループはまず、膵臓がん組織においてどの程度cGAS-STINGシグナルか活性化されているのか免疫組織化学染色を用いて調べた。同大肝胆膵外科で行った膵臓がん手術検体から78例を対象に、cGASとSTINGタンパク質について発現レベルを調べた結果、約50%の症例で同一組織内でのcGASおよびSTING両方の発現(double-positive)が確認された。また、cGASおよびSTING double-positive症例群とそれ以外の症例群に分けて手術後の生存率を比較したところ、double-positive群で有意に生存率が高まることがわかった。
cGAS-STING活性組織では多数の細胞傷害性T細胞が浸潤
この時の免疫細胞の浸潤について解析したところ、cGASとSTINGの発現に一致して腫瘍免疫を担う細胞傷害性T細胞のがん組織への浸潤が高く、cGAS-STINGシグナル活性組織ではがんに隣接する間質部からがん組織内部にかけて多数の細胞傷害性T細胞の浸潤が見られることを発見した。一方、cGAS-STINGシグナル非活性組織において細胞傷害性T細胞は間質部の一部に固まって存在し、浸潤像は認められなかった。
cGAS-STING活性化でMeflin/TIMP-1発現亢進、T細胞浸潤誘導
次に、細胞傷害性T細胞の浸潤を規定する因子としてCAFに着目した。cGAS-STINGシグナル活性組織と非活性組織においてCAFの量に違いは認められなかったが、がん抑制性CAFのマーカーであるMeflinとTIMP-1の発現を調べたところ、cGAS-STINGシグナル活性組織において、よりMeflinとTIMP-1の発現が亢進していることがわかった。
また、Transwellチャンバーを用いた、がん-CAF-免疫細胞の共培養系における検討では、cGAS-STINGシグナルに対して活性化処理を行わない群で、CAFにおけるMeflinとTIMP-1の発現が低下するとともに、T細胞の下部チャンバーへの浸潤はコントロール群と変化しなかった。一方、cGAS-STINGシグナル活性化を行った群では、CAF内の両遺伝子の発現が保たれるとともにT細胞の下部チャンバーへの浸潤誘導が起こり、下部チャンバー内がん細胞への抗腫瘍効果が発揮された。
膵臓がんに対する免疫チェックポイント阻害剤の効果の手助けになる可能性
以上のことから、cGAS-STINGシグナルは免疫細胞を局所に集めるのみではなく、周囲のCAFとの相互作用により間質組織内への浸潤を積極的に促進することで抗腫瘍効果に寄与していることがわかった。近年、多くの腫瘍で免疫チェックポイント阻害剤の適応が増えているが、膵臓がんではほとんど効果が認められていない原因の1つとして、間質細胞による障壁が考えられている。「cGAS-STINGシグナルの活性化によりこの障壁を打破できれば、免疫チェックポイント阻害剤の効果を手助けできることにつながる可能性が期待される」と、研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース






