老化肝星細胞から放出のSASP因子、放出メカニズムとがん増殖進展のメカニズムは?
大阪公立大学は6月23日、肝臓に移行した腸内細菌叢の成分である「リポタイコ酸」が、肝がん微小環境を変化させ、がんの増殖進展を促進するSASP(Senescence-associated secretory phenotype、細胞老化随伴分泌現象)因子を老化肝星細胞から放出させるメカニズムを明らかにしたと発表した。この研究は、同大大学院医学研究科・病態生理学の大谷直子教授、山岸良多助教を中心とするグループと、同肝胆膵病態内科学の河田則文教授、慶應義塾大学先端生命科学研究所の福田真嗣特任教授、広島大学大学院・統合生命科学研究科の中江進教授らの共同研究グループによるもの。研究成果は、「Science Immunology」電子版に掲載されている。
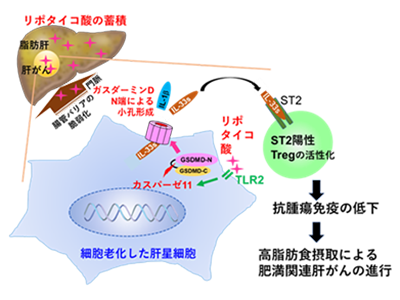
画像はリリースより
(詳細は▼関連リンクからご確認ください)
がんの組織は、がん細胞そのものだけでなく線維芽細胞や免疫細胞など、さまざまな種類の細胞種が集まって「がん微小環境」を構成している。進行したがん組織の微小環境では、がん細胞周囲の細胞が、がんの促進を助長していると考えられている。脂肪肝を素地とする肝がん微小環境では、肝星細胞と呼ばれる線維芽細胞が細胞老化を引き起こしており、「細胞老化随伴分泌現象(senescence-associated secretory phenotype, SASP)」というさまざまな分泌因子を放出する現象が見られ、その分泌因子(SASP因子)が、がん細胞の増殖を促進することを、研究グループは見出していた。
しかしこれまで、SASP因子がどのように放出されるのかは不明であり、放出されたSASP因子がどのようにがんの進行に作用するのかは、十分には明らかにされていなかった。そこで研究グループは今回、近年増加傾向にある脂肪肝を素地とする肝がん(NASH肝がん)のマウスモデルを用いて、老化肝星細胞からのSASP因子の放出メカニズムとSASP因子による抗腫瘍免疫抑制により、がん増殖を進展させるメカニズムについて研究を行った。
SASP因子のIL-33、肝がん微小環境で高発現し肝がん増殖促進をマウスで確認
まず、肝がん組織においてどのようなサイトカインが産生されているのか、網羅的遺伝子発現解析で調べたところ、非腫瘍部と比較して腫瘍部では「IL-33」が最も高い発現を示し、がん微小環境における老化肝星細胞にIL-33の発現が認められた。IL-33ノックアウトマウスでは肝腫瘍形成が抑制され、野生型マウスにIL-33を投与すると肝腫瘍形成が促進されたことから、肝がん微小環境で高発現するIL-33は肝がんの増殖を促進する作用があると考えられた。また、IL-33は同じく老化肝星細胞で発現が上昇するSASP因子、IL-1βに依存して著しく発現が誘導され、CELA-1というエラスターゼで切断され活性化型になることを明らかにした。
高脂肪食摂取による肥満マウス、腸内細菌叢の成分リポタイコ酸が肝臓に移行・蓄積
次に、SASP因子であるIL-1βやIL-33が老化肝星細胞からどのように放出されるのか解析を行った。高脂肪食摂取による肥満マウスの腸内ではグラム陽性腸内細菌が増加しており、肝臓においてはグラム陽性腸内細菌の細胞壁成分であるリポタイコ酸が多く蓄積していることがわかった。
リポタイコ酸が老化肝星細胞に作用し細胞膜上に小孔を形成、そこからSASP因子が細胞外に放出
そこで、この脂肪肝の状態を培養レベルで再現するため、肝臓から単離した老化肝星細胞にリポタイコ酸を添加したところ、SASP因子であるサイトカインIL-1βとIL-33が、細胞外に放出されることがわかった。また、肝腫瘍部から単離した老化肝星細胞では、ガスダーミンDというタンパク質が高発現しており、リポタイコ酸の添加によりカスパーゼ11により切断されたガスダーミンDの切断体、GSDMD-Nが検出された。このGSDMD-Nは、細胞膜上に小孔を形成することが知られているが、ガスダーミンDの発現をノックダウンしたところ、リポタイコ酸によるIL-1βとIL-33の細胞外への放出が抑制された。このことから、SASP因子はGSDMD-Nで形成される小孔を介して、老化肝星細胞から細胞の外部に放出されることが明らかになった。
GSDMD-Nによる小孔が形成されると、マクロファージなど他の細胞種では、細胞死の一種であるパイロトーシスが促進されることが知られていた。しかし、老化した肝星細胞では、細胞膜上で小孔が形成されても、パイロトーシスはなかなか生じないことがわかった。老化肝星細胞でパイロトーシスが生じにくいことは、老化細胞からのSASP因子の放出が続くことを示唆しており、SASP因子の作用が持続するメカニズムのひとつと考えられるという。
放出されたIL-33、ST2陽性のTreg細胞に作用して抗腫瘍免疫を抑制し肝がんを進展
また、老化肝星細胞から放出されたIL-33は、その受容体ST2が陽性のTreg細胞に作用して抗腫瘍免疫を抑制し肝がんを進展させることがわかった。
さらに、ヒトのNASH肝がんの腫瘍部に存在する肝星細胞において、GSDMD-Nの存在がその特異的抗体を用いた組織染色により確認できた。このことから、マウスモデルを用いて得られたこれらの新知見は、ヒトのNASH肝がんの一部においても同様に認められる可能性が示唆された。
最後に、ガスダーミンDによる小孔形成を阻害する薬剤をこの高脂肪食誘導性肝がんモデルマウスに投与したところ、肝腫瘍形成が有意に抑制された。これらの結果から、ガスダーミンDによる小孔形成を阻害する薬剤は、肝がんの予防や治療につながる可能性があるという。
3つのポイントをコントロールすることが脂肪肝による肝がんの進行抑制につながる可能性
今回の研究により、「腸管バリア機能の改善が肝がんの予防につながる可能性」「GSDMD-N による細胞膜上の小孔形成の阻害で、肝がんの進行を予防できる可能性」「ST2受容体の阻害剤や阻害抗体で、肝がんの進行を予防できる可能性」という3つのことが明らかになった。それぞれのポイントをコントロールすることが、脂肪肝を素地とする肝がん進行の抑制につながる可能性がある、と研究グループは述べている。
▼関連リンク
・大阪公立大学 プレスリリース




