病理形態像と遺伝子異常・エピゲノム変化を紐づけた試料が蓄積されてきた
横浜市立大学は5月30日、H&E(ヘマトキシリン・エオジン)染色の大腸がんの病理組織画像から、がんの遺伝子異常を検出する高性能な検出器の作製に成功したと発表した。この研究は、同大大学院医学研究科分子病理学の藤井誠志主任教授、国立がん研究センター東病院の吉野孝之消化管内科長らの研究グループによるもの。研究成果は、「Clinical Cancer Research」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
日常の病理診断では、生検または外科手術によって採取された病理標本はホルマリン固定された後にパラフィンに包埋されたブロック標本が作製される。そしてそのブロック標本から薄切された未染色切片がH&E染色され、それを顕微鏡下で観察し、病理医が病理診断を行う。がんの個別化医療(precision medicine)では、がん細胞、がん組織を含むブロック標本から薄切された未染色切片から核酸を抽出し、がん遺伝子パネル検査を用いて遺伝子異常が検出される。そして、その結果に基づいて分子標的治療の可否が決定される。がんの病理形態像は遺伝子異常、エピゲノム変化等の合算から作られるが、がんの個別化医療の実践により、病理形態像と遺伝子異常・エピゲノム変化についての情報を紐づけた試料が蓄積され、これらの関係を検討する機会が得られるようになった。
大腸がん患者1,657人分の画像を病理医がまず3つの特徴別に仕分け
研究グループは今回、病理医ががんにおける病理形態学的特徴を目視で抽出し、DL(ディープラーニング)を使用して個別に学習させることにより、さまざまながんの病理形態学的特徴を検出する検出器を作製した。
まず、産学連携全国がんゲノムスクリーニング「SCRUM-Japan」の GI-SCREEN-Japan(現MONSTAR-SCREEN)のコホートから、BRAFV600E変異やマイクロサテライト不安定性(MSI)に関する次世代シーケンス配列(NGS)データを持つ大腸がん患者の1,657の病理組織画像(患者1人に対して1画像)を入手し、986画像の探索的コホート、248・423画像の検証コホートに分けた。
病理医がまずH&E染色画像を目視で見比べて、どのような形態像が遺伝子異常に関連しているのかを注意深く観察して見出し、従来の病理組織学的診断に用いる病理組織学的特徴、これまで遺伝子異常との関連が示唆されている病理組織学的特徴、そして全く新規で従来の病理組織学的診断には用いない病理組織学的特徴を選抜した。
33の病理組織学的特徴からがんの特徴を予測し、さらにDLで遺伝子異常を予測
次に、1人の病理医が病理組織画像に対して、33個の病理組織学的特徴について高精度で、約105万に及ぶアノテーション(ラベル付け)を行い、第一段階のがんの病理形態学的特徴を予測するモデルを構築した。そして、この検出器を用いて画像を分類して得られた病理組織画像の組み合わせに対して、その特徴(遺伝子異常)との関係に関してDLを使用して遺伝子異常予測モデルを構築し、検出器を作製した。その結果、病理画像から病理組織学的特徴を抽出し、遺伝子異常を高精度に検出するアルゴリズムが確立され、新しいスクリーニングシステムの開発に成功した。
この2段階での検出器作製のアプローチは、同研究で初めて用いられたこれまでにない新規の方法。この方法では、病理形態学的特徴が予測された画像の組み合わせの中から、DLによって遺伝子異常との関係の存在が示唆される画像の組み合わせを探索することで、元来ブラックボックスに陥りかねないDLを用いながらも、作製した検出器が利用する病理形態学的特徴領域の組み合わせによって説明できるようになる。
BRAFV600EとMSI-Hに対して高い精度で遺伝子異常を検出
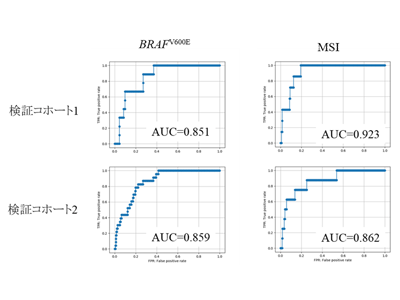
同研究で対象としたBRAFV600EおよびMSI-Hは、BRAF阻害剤または免疫チェックポイント阻害剤によるがん治療のために確認される、よく知られたバイオマーカーだが、同研究では、2つの病理組織学的特徴を使用する遺伝子異常検出アルゴリズムを用いた、BRAFV600EおよびMSI-Hに対する検出器により、2つの独立した検証コホートで高いAUC値を再現した(BRAFV600E、MSIの順に、検証コホート1はAUC=0.851、0.923)、検証コホート2はAUC=0.859、0.862)。特異的な遺伝子異常をもつ結腸・直腸がんの患者に、最も適した治療の選択をする有用なスクリーニングツールとして役立つ可能性がある。
病理画像から遺伝子異常を検出するこのスクリーニングシステムを同研究グループでは「Virtual sequencing(バーチャルシーケンシング)」と提唱し、病理組織学的特徴数を増やすことによって検出器の性能向上をさせる等、実際の医療に用いることを意識したアプローチを行っているという。
遺伝子パネル検査などの従来の検査を行う前に、遺伝子異常を予測できるこの新しい方法は、近い将来の大腸がんなど、がんに対する治療戦略の迅速な決定に利活用できることが期待される。病理学の面からは、病理医とAIが恊働することによって可能になる「次世代病理学の創生」を目指し、このプロジェクトを引き続き遂行していく考えを研究グループは示している。
▼関連リンク
・横浜市立大学 プレスリリース




