骨髄の線維化、分子機構には不明な点が多かった
大阪大学は5月27日、造血幹細胞を維持する微小環境である「造血幹細胞ニッチ」を構成するCAR細胞で骨髄の線維化を抑制し、造血幹細胞ニッチを維持する転写因子を同定したと発表した。この研究は、同大大学院医学系研究科の尾松芳樹准教授、長澤丘司教授(幹細胞生物学)(生命機能研究科/免疫学フロンティア研究センター)らの研究グループによるもの。研究成果は、「Nature Communications」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
全身を循環する血液細胞は骨髄で産生されており、骨髄には全ての血液細胞を生み出す造血幹細胞が存在している。造血幹細胞はニッチと呼ばれる特別な微小環境によって維持されていると考えられてきたが、その実体は長年不明だった。
長澤教授の研究グループは、これまでに造血幹細胞ニッチを構成する中心的な細胞として、CAR細胞を特定し、造血幹細胞ニッチの形成と維持には、CAR細胞で特異的に高発現する転写因子Foxc1およびEbf3が必須の役割を果たすことを明らかにした。CAR細胞においてFoxc1は脂肪細胞への分化を抑制し、Ebf3は骨芽細胞への分化を抑制し、いずれも造血幹細胞の維持に必須であるサイトカインCXCL12とSCFの発現を促進することが示されていた。一方、さまざまな造血器腫瘍で造血を障害し予後不良とする骨髄線維症においては、CAR細胞が線維芽細胞に変化すると考えられているが、その分子機構は、PDGF受容体の関与の他、十分明らかにはなっていない。
Runx1/2両方をCAR細胞特異的に欠損させたマウスで骨髄の血液細胞が著減
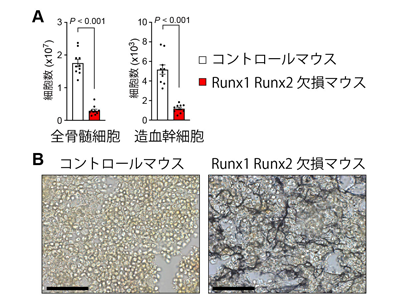
研究グループは、造血幹細胞の発生に必須の転写因子Runx1と骨芽細胞の発生に必須の転写因子Runx2が、CAR細胞で高発現していることを見出した。そこでRunx1とRunx2のCAR細胞における機能を明らかにするため、Runx1またはRunx2のどちらか片方をCAR細胞で欠損させたマウスを解析したところ、正常なCAR細胞が形成、維持された。ところが、Runx1とRunx2の両方をCAR細胞特異的に欠損させたマウスでは、骨髄の血液細胞が著減し、造血幹細胞、前駆細胞および分化細胞が著減していたことがわかった。
また、CAR細胞を分離して解析したところ、CAR細胞では、線維芽細胞で高発現するIII型コラーゲン、VI型コラーゲン遺伝子の発現が著しく増加していた。そこで組織学的解析を行ったところ、骨髄の至る所で、線維化の際、線維芽細胞が産生する好銀線維が著しく増加していたことがわかった。
Runx1/2がCAR細胞の線維化を抑制、造血幹細胞ニッチを維持
培養したCAR細胞では、Runx1またはRunx2を強制発現させるとIII型コラーゲン、VI型コラーゲン遺伝子の発現が低下。さらに、骨髄細胞でトロンボポエチン遺伝子を強制発現させた原発性骨髄線維症モデルマウスでは、CAR細胞のRunx1とRunx2の発現が低下していた。以上より、転写因子Runx1とRunx2が、CAR細胞の線維化を抑制することにより、造血幹細胞ニッチを維持していることが示唆された。
Runx1/2、新規の治療標的となる可能性
研究により、CAR細胞の線維化を抑制し、造血幹細胞ニッチを維持する転写因子が明らかになった。これらの知見は、骨髄の線維化を抑制するという造血幹細胞ニッチを維持する新しい分子機構を明らかにし、骨髄線維症の発症メカニズムの解明に貢献するものと考えられる。「骨髄線維症においてはCAR細胞でRunx1/2の発現が低下することがその進展に重要である可能性があり、Runx1/2が新たな治療標的となる可能性がある」と、研究グループは述べている。
▼関連リンク
・大阪大学 免疫学フロンティア研究センター プレスリリース



