免疫調節薬に対する薬剤耐性獲得問題の克服へ
慶應義塾大学は5月23日、薬剤に耐性となった多発性骨髄腫細胞から分泌される細胞外小胞(Extracellular Vesicles;EV)が薬剤感受性を持つ細胞に取り込まれることで新たに薬剤感受性株に薬剤耐性能を獲得させることが判明したと発表した。この研究は、同大薬学部病態生理学講座の服部豊教授、東京医科大学医学総合研究所分子細胞治療研究部門の落谷孝広教授、山元智史助教(特任)、分子病理学分野の黒田雅彦主任教授、国立がん研究センター病態情報学ユニットの山本雄介氏の研究グループによるもの。研究成果は、「Blood Advances」に掲載されている。
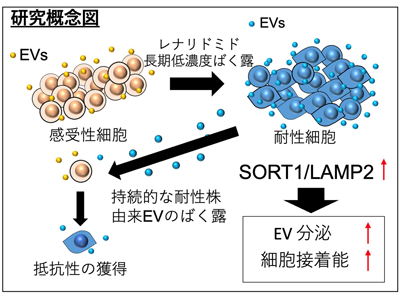
画像はリリースより
(詳細は▼関連リンクからご確認ください)
EVは約100nm前後の細胞外に分泌される小胞であり、脂質二重膜の安定的な構造の中にDNA、RNA、タンパク質など多くの物質を内包している。EVは組織修復や再生、疾患の発症や進展など、多くの機能や病態に関与することが知られており、薬剤耐性についても大きな役割を果たすことがわかっている。
多発性骨髄腫は、形質細胞が多段階の遺伝子変異を獲得することでがん化した造血器腫瘍。2000年代に、レナリドミドなどの免疫調節薬、プロテアソーム阻害薬、抗体医薬などの開発により多発性骨髄腫の予後は大きく改善されてきた。しかし、治療薬に長期間曝されることにより治療薬に対する耐性を獲得することが問題となっている。特に、免疫調節薬に対する薬剤耐性獲得は、多発性骨髄腫治療において深刻な問題であるが、その耐性化機構は完全に明らかとなっていない。
研究グループは、樹立されたレナリドミド耐性株においてEV分泌量が増加していることから、新たにEVを介した細胞間相互作用によるレナリドミド耐性化機構が存在すると考えた。
レナリドミド耐性株で細胞接着能やEV分泌量が亢進
同大薬学部病態生理学講座が所有するレナリドミド耐性株は、親株であるKMS21、KMS27、KMS34に対し、レナリドミドを長期低濃度でばく露させることで樹立した細胞株(KMSR21R、KMSR27R、KMSR34R)。特徴として、培養ディッシュへの接着を示す。また、超遠心法で回収したEVをnanoparticle tracking analysis(NTA法)でその粒子数を計測したところ、親株と比較して耐性株では分泌されるEVの量が多いことが明らかとなった。
次に、耐性株で増加したEVがレナリドミドに感受性を持つ親株に与える影響を共培養法によって検討した。トランズウェルという細胞を培養する容器の上部に耐性株を、下に親株を入れた。上下は0.4μmという小さな孔の開いた膜で隔てられているが、0.4μmという大きさは、EVは通過することが可能であるが、細胞などは通さないため、EVの作用・効果を確認するためによく用いられる。共培養の結果、親株であるKMS21細胞は、それぞれの耐性株と共培養することで細胞接着能が亢進し、薬剤感受性が低下することが明らかとなった。
耐性株でEV分泌を亢進させるSORT1、LAMP2を同定
耐性株由来EVが親株の薬剤耐性に影響することが明らかとなったことから、実際にその薬剤耐性を制御する遺伝子の探索を行った。6種類の細胞株、KMS21、KMS27、KMS34、KMS21R、KMS27R、KMS34RについてRNAシークエンスを行ない、耐性株で変動する遺伝子の発現量解析をした。基準として、耐性株と親株における遺伝子発現を比較し、耐性株で発現が1.5倍以上、かつ、p値が0.01以下の遺伝子を118個選び、さらに文献調査によりEVの分泌に重要なエンドソームなどに関連する遺伝子として13個の遺伝子を抽出した。
これら13遺伝子をsiRNAによって、遺伝子のノックダウン実験を行った。この際、ノックダウンによってレナリドミドの感受性が回復した8個の遺伝子に対して、Exo Screen法によるEV分泌量の低下を確認した。最終的に、レナリドミド耐性細胞株においてEV分泌を亢進させる責任遺伝子としてSORT1とLAMP2という2つの遺伝子を同定した。
SORT1とLAMP2高発現患者で全生存期間、無増悪生存期間が短い
最後に、SORT1とLAMP2遺伝子の臨床的意義を検討するため、公共のデータベースを利用した予後解析を実施。レナリドミド治療を行なった患者検体群の臨床試験データセットでは、SORT1とLAMP2の高発現患者では、全生存期間、および、無増悪生存期間が短かった。このことから、SORT1、LAMP2の高発現は予後を示すマーカーとなる可能性が示唆された。
多発性骨髄腫細胞に対するEV分泌阻害剤の開発などに期待
研究結果より、多発性骨髄腫における免疫調節薬の耐性化機構にEVが関与することが明らかとなった。耐性株由来のEVが感受性株に耐性能を与えることを示したが、まだどのように耐性株でSORT1、LAMP2遺伝子の発現が上昇するのか、その機序は解明できていない。現在、この耐性株におけるSORT1、LAMP2遺伝子の発現亢進機構の解明に取り組んでいる。
「今後、多発性骨髄腫細胞に対するEV分泌阻害剤などの開発が進むことで、既存の多発性骨髄腫治療に加えて、EV分泌阻害剤を併用することが、治療に抵抗性を持たないように治療を続けるといった新たな多発性骨髄腫治療戦略の開発につながることを期待する」と、研究グループは述べている。
▼関連リンク
・慶應義塾大学 プレスリリース



