日本で約1300万人が腰痛を患い、20~40%は椎間板変性が腰痛の原因
大阪大学は4月15日、ヒトiPS細胞から作った軟骨様髄核組織を、脊椎の髄核を摘出した動物モデルに移植することにより椎間板変性を防げることを明らかにしたと発表した。この研究は、同大大学院医学系研究科の大学院生の釜谷崇志氏(研究当時、整形外科学/京都大学iPS細胞研究所(CiRA)臨床応用研究部門)、萩澤宏樹氏(整形外科学/CiRA臨床応用研究部門)、海渡貴司准教授(整形外科学)、妻木範行教授(組織生化学/CiRA臨床応用研究部門)らの研究グループによるもの。研究成果は、「Biomaterials」に掲載されている。
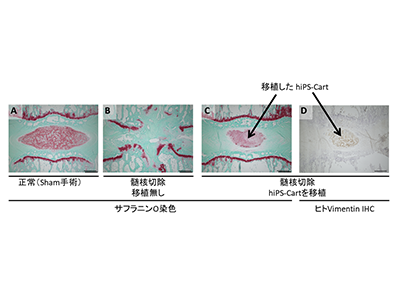
画像はリリースより
(詳細は▼関連リンクからご確認ください)
髄核は椎間板の中心部分を構成する組織で、脊椎にクッション性と可動性を与える。髄核の変性・消失は腰痛の原因になり、変性した髄核は治らない。日本では約1300万人が腰痛を患い、その20~40%は椎間板変性が腰痛の原因と考えられている。椎間板変性は、多くの場合において髄核の変性・消失から始まると考えられている。また、細胞移植による再生治療法の開発が期待されているが、髄核を置換するような組織を再生することはできない。
ラット動物モデルで移植のヒトhiPS-Cart、少なくとも6か月生着し椎間板の変性を防ぐ
今回、研究グループは、ヒトと同じ霊長類であるサルの髄核と軟骨の遺伝子発現をシングルセルRNAシーケンスの方法を使って単一細胞レベルで網羅的に調べた。その結果、髄核は軟骨様組織と脊索様組織で構成されることが転写発現レベルで明らかになった。
続いて、ヒトiPS細胞から軟骨様髄核に相当する組織(hiPS-Cart)を作り出し、椎間板変性をおこすラット動物モデルにおいて、髄核が失われた部分に移植。移植したヒトhiPS-Cartは少なくとも6か月の長期にわたって生着し、椎間板の変性を防いだ。力学試験により、移植組織は正常椎間板に近い力学特性を持つことが判明。さらに、移植後にもシングルセルRNAシーケンス解析を行うことにより、hiPS-Cartは椎間板に移植された後に、椎間板の低酸素環境に順応した細胞分化をすることがわかった。
これまでの移植物と異なり、hiPS-Cartは細胞外マトリックスを含むため、細胞の生存と分化が可能になったと考えられる。その結果、hiPS-Cartは生着して髄核の機能を果たし、髄核を置換する組織を再生したとしている。
腰痛を根治的に治癒する再生治療方法開発に期待
同研究成果により、変性・消失した髄核部分にhiPS-Cartを移植することで椎間板変性を防ぎ、腰痛を根治的に治癒する再生治療方法を開発することが期待される、と研究グループは述べている。
▼関連リンク
・大阪大学 ResOU






