慢性期脊髄損傷は亜急性期の治療より難しい
慶應義塾大学は4月5日、ヒトiPS細胞から作製した神経細胞(ニューロン)において神経突起伸長を促進する新しいシグナル経路を解明したと発表した。この研究は、同大医学部生理学教室の加瀬義高助教、佐藤月花氏(大学院医学研究科博士課程学生)、岡野雄士氏(医学部学生)、岡野栄之教授らの研究グループによるもの。研究成果は、「iScience」に掲載されている。
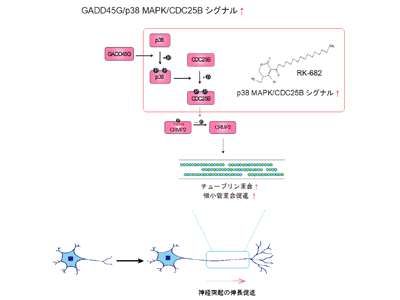
画像はリリースより
(詳細は▼関連リンクからご確認ください)
慶應義塾大学医学部生理学教室と整形外科学教室では、亜急性期脊髄損傷に対するヒトiPS細胞由来神経前駆細胞を用いた再生医療の臨床研究を開始している。しかし、脊髄損傷患者の大部分は慢性期にあり、かつ、慢性期脊髄損傷は亜急性期の治療より難しいことから、慢性期脊髄損傷の治療技術の開発が求められている。
ヒトiPS細胞由来の「ヒトの」ニューロンで解析
研究グループは、これまでにγ-セクレターゼ阻害剤のDAPTをヒトiPS細胞由来神経幹細胞/前駆細胞に添加することで、移植後に分化したニューロンの神経突起が伸長し慢性期脊髄損傷モデルマウスを治療することに成功してきた。しかし、ヒトの神経突起伸長がどのようなメカニズムで生じているのか、どのようにすれば伸長を促進できるか、わかっていない部分があった。
シグナル経路GADD45G/p38 MAPK/CDC25BがCRMP2に作用して神経突起を伸ばす
今回の研究では、γ-セクレターゼ阻害剤で前処理したヒトiPS細胞由来神経幹細胞/前駆細胞の集合体であるニューロスフェア1つ1つを、RNA-seqで解析して全転写産物を調べ、キーとなっている遺伝子を探すための網羅的解析を行った。するとGADD45Gという遺伝子の発現が際立って高くなっていることが明らかになった。さらに関連タンパク質の発現や、リン酸化の状態を調べていくと、このGADD45Gがp38のリン酸化を惹起し、さらにリン酸化p38がCDC25Bのリン酸化を惹起していることが明らかになった。最終的には、CRMP2の514番目のトレオニン(threonine)の脱リン酸化を促進することで神経突起の骨組みである微小管の重合を促し、神経突起伸長を促進していることがわかった。
γ-セクレターゼ阻害剤「Compound34」、DAPTより強力な神経突起伸長効果
また、細菌の一種であるストレプトマイセス属が産生する化合物RK-682は、この新たに発見されたメカニズムの中のp38のリン酸化を維持することで、p38 MAPK/CDC25Bのシグナル経路を増強し、神経突起を伸長することがわかった。さらに研究グループでは、これまでγ-セクレターゼ阻害剤にはDAPTを使用してきたが、Compound34というγ-セクレターゼ阻害剤がDAPTの10分の1の量で同等の効果を発揮することを発見した。これらの研究成果は、論文発表とともに、慢性期脊髄損傷治療に応用する目的で、「神経突起伸長促進用キット及びその使用」として特許出願された。
ヒト大脳の進化に重要な GADD45G のニューロンでの役割を初めて解明
興味深いことに、このシグナル経路の最初の起点であるGADD45Gは、遺伝子の発現を促進する遺伝配列上のエンハンサーがヒト特異的に欠失しているhCONDELという遺伝子群の1つだ。マウスやチンパンジーではGADD45Gのエンハンサーは欠失しておらず、神経幹細胞/前駆細胞の増殖がヒトよりも劣っているため大脳が小さいと考えられている。しかしながら、幹細胞の状態から分化したニューロンのレベルではどのような機能を発揮しているのか全くわかっておらず、今回の神経突起伸長に関わっているという発見は、ニューロンでのGADD45Gの役割を解明した初めての報告となる。
ヒトES細胞から作製したニューロンにおいても、ニューロンの成熟度が上がる過程でGADD45Gの発現が上昇してくることから、ヒトにおいては、幹細胞の状態から終末分化細胞であるニューロンになった後の精細なこの遺伝子の発現上昇が、ニューロンが機能を発揮するために必要な要素であることがわかった。
「まずは慢性期脊髄損傷治療への応用を見据えている」
今回の研究は、ヒト以外の動物種ではなく、ヒトのニューロンでの神経突起伸長メカニズムを解明し、そのメカニズムに立脚した神経突起伸長化合物RK-682と強力なγ-セクレターゼ阻害剤作用を有するCompound34を同定したもので、いまだ課題の残る慢性期脊髄損傷治療のブレイクスルーとなる可能性がある成果だ。
さらに、GADD45Gは、ヒトの大脳がなぜ他の動物種と異なり、大きく進化できたのかを説明できる遺伝子として注目されており、その遺伝子のニューロンにおける役割を初めて発見できた同研究結果は進化生物学的にも意義のある成果といえる。
研究グループは、「まずは慢性期脊髄損傷治療への応用を見据えているが、今回発見したシグナル経路の強度が老化とともに減少してしまうのかどうか、もしそうならば、このシグナル経路を増強すれば若返りにつながるのか、また他の神経軸索が変性してしまう神経変性疾患でも共通のメカニズムがあるのかどうかなど、現在検証を開始している」と、述べている。
▼関連リンク
・慶應義塾大学 プレスリリース




