高度な組織修復力を持つ腸管上皮、再生メカニズムの詳細は不明だった
九州大学は3月22日、腸管上皮の再生に必要な組織幹細胞を新たに発見し、腸管の再生やがん化の過程に「胎児返り」と「胃上皮様変化」という2つの現象が重要であることを明らかにしたと発表した。この研究は、同大生体防御医学研究所の中山敬一主幹教授、比嘉綱己研究員らの研究グループによるもの。研究成果は、「Nature Communications」に掲載されている。
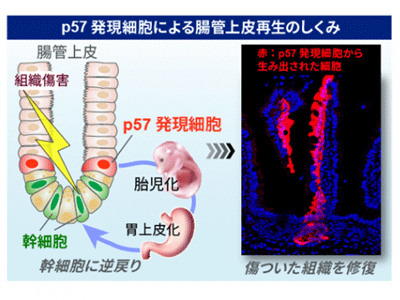
画像はリリースより
(詳細は▼関連リンクからご確認ください)
哺乳類の腸管上皮にはLgr5発現細胞という幹細胞が存在しており、定常状態における組織の維持を担っている。一方で、Lgr5発現細胞は化学物質や放射線などの組織傷害によって一時的にほぼ完全に失われるが、腸管上皮は問題なく維持される。この事実は、Lgr5発現細胞以外に、腸管の傷害後再生に重要な幹細胞集団が存在することを強く示唆しているが、そのような幹細胞の実体や再生のメカニズムは不明だった。
研究グループは以前、細胞周期の静止状態を維持するp57遺伝子が、造血幹細胞や神経幹細胞といった代表的な組織幹細胞に特異的に発現することを発見していた。そこでこのp57の発現を指標とすることで、腸管においても新たな幹細胞集団を同定できるのではないかと考えた。
通常は分化細胞として存在するp57発現細胞、傷害を受けると脱分化して幹細胞に
研究グループはまず、免疫染色を用いて小腸におけるp57の発現を調べた。小腸上皮は絨毛と陰窩という基本構造の繰り返しからなる組織だが、p57は幹細胞が存在すると言われている陰窩において、希少な細胞集団に発現していることが判明。これらp57発現細胞はLgr5発現細胞とは独立した細胞集団で、かつ細胞増殖のマーカーであるKi67が陰性であることから、少なくとも定常状態においては造血幹細胞などと同様に、細胞周期を停止した状態にあることがわかった。
次に研究グループは、遺伝子改変技術を用いてp57の系統追跡マウスを作製。このマウスにタモキシフェンという薬剤を投与すると、まずp57発現細胞がtdTomatoという赤色蛍光タンパク質で標識され、さらにこの蛍光標識がp57発現細胞の子孫細胞にも次々伝わっていく仕組みになっている。実際にp57系統追跡マウスにタモキシフェンを投与すると、腸管陰窩のp57発現細胞がtdTomatoで標識された。しかしながら、定常状態ではこの蛍光標識は他の細胞に伝わることはなく、またp57発現細胞は内分泌細胞のマーカーを発現していることがわかった。
一方、このマウスに抗がん剤や放射線で傷害を与えると、最初はp57発現細胞だけに限局していたtdTomato標識が、2週間後には陰窩~絨毛までのすべての細胞に伝わることが判明。これらの結果から、p57発現細胞は定常状態では内分泌細胞として存在しているものの、組織が傷害されると脱分化して幹細胞となり、ピンチヒッターとして組織修復に寄与することが明らかとなった。
ダイナミックなリプログラミング「胎児返り」「胃上皮様変化」で脱分化
さらに、蛍光標識したp57陽性細胞を含む腸管上皮細胞を正常および傷害後のマウスから単離し、1細胞RNA-seq解析によって個々の細胞の全遺伝子の発現プロファイルを調べた。その結果、再生途上のp57発現細胞では、本来成体腸管には発現していないはずの胎児腸管の遺伝子群や胃上皮の遺伝子群が高発現していることがわかり、幹細胞性獲得の過程において通常の成体腸管とはまったく異なった細胞状態を経ていることが明らかとなった。つまり腸管の傷害後再生においては、分化した細胞の遺伝子発現プロファイルをダイナミックに作り変える(リプログラミングする)ことで脱分化を引き起こし、新たな幹細胞集団を作り出していると考えられた。
p57発現細胞はまた、Apc変異マウスの腸管腫瘍においてもがん幹細胞として機能しており、かつ腫瘍内でも上記と同様のリプログラミング現象が起こっていることがわかった。これらの結果は、正常腸管上皮に備わっている再生システムが、腫瘍においても利用されていることを示唆している。
がんの新規治療法の開発や再生医療などへの応用に期待
今回の研究により、腸管の再生や発がんの過程では胎児返りや胃上皮化生様の変化を伴う大規模なリプログラミングを経て幹細胞を生み出していることがわかった。研究グループは、今後この現象の分子メカニズムを解明することで、生体の組織維持機構の基本原理を明らかにするとともに、再生医療に用いる組織幹細胞の誘導・制御や、より根治的ながん治療のための戦略開発などに役立てていきたいとしている。
▼関連リンク
・九州大学 研究成果



