ワクチンでCD4+T細胞が誘導されるとHIV暴露後に感染増殖が増強してしまう
東京大学医科学研究所は3月1日、HIVの主標的となるHIV特異的CD4陽性T細胞を誘導せずにHIV特異的CD8陽性T細胞を誘導する新規抗原を設計し、動物実験でHIV経直腸粘膜感染防御効果を明らかにしたと発表した。この研究は、同研究所所附属病院エイズワクチン開発担当分野の俣野哲朗教授(委嘱)らの研究グループによるもの。研究成果は、「Molecular Therapy」に掲載されている。
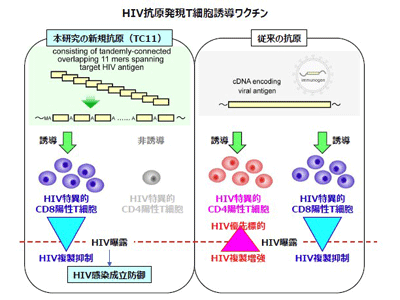
画像はリリースより
(詳細は▼関連リンクからご確認ください)
HIV感染症の制圧は国際的重要課題であり、予防ワクチン開発が切望されている。感染拡大の抑制には、早期診断・治療促進が重要だが、それだけでは不十分であり、有効性50~70%のワクチンでも導入効果が期待しうることが試算されている。HIVワクチン開発においては、抗原導入のためのウイルスベクター等のデリバリープラットフォームの開発は進展してきたが、抗原至適化が課題だ。特に、多様性に富むHIVに対するワクチン抗原開発は、容易ではなく難航している。中和抗体誘導はHIVワクチン開発の重要戦略だが、中和抗体標的となる表面タンパク質抗原の多様性が極めて高いため、広域交差性中和抗体誘導を目指した研究が進められているものの、誘導法の確立には至っていない。
一方、T細胞誘導ワクチン開発においても、抗原至適化が課題となっている。HIV特異的CD4陽性T細胞は、HIV感染の優先標的であることが知られていたが、近年の研究で、ワクチンによるHIV特異的CD4陽性T細胞誘導は、HIV曝露後の感染増殖を増強してしまうことがわかってきた。
CD8+T細胞を誘導する11アミノ酸ペプチド抗原発現ウイルスベクターワクチン
そこで研究グループは、HIV特異的CD4陽性T細胞を誘導せずにHIV特異的CD8陽性T細胞を誘導する新規抗原を設計した。同抗原は、CD4陽性T細胞の標的至適エピトープが12アミノ酸以上のペプチドであるのに対し、CD8陽性T細胞の標的至適エピトープが8~11アミノ酸ペプチドであることに基づき設計された11アミノ酸ペプチド断片連結抗原だ。
動物実験でワクチン接種後、繰り返しの経直腸HIV感染に対し防御効果を確認
動物実験で、この新規抗原発現ウイルスベクターワクチンの接種実験を行ったところ、HIV特異的CD4陽性T細胞を誘導せずにHIV特異的CD8陽性T細胞を誘導することが確認された。
ベクターウイルス抗原特異的CD4陽性T細胞は誘導されており、これがヘルパーとして機能的HIV特異的CD8陽性T細胞誘導に貢献していることを示唆する結果も得られているという。さらに、繰り返しの経直腸ウイルスチャレンジ実験を行ったところ、8回のチャレンジに対して、ワクチン接種群の3分の2で感染が防御され、統計学的にも有意な感染防御効果が示された。特にワクチン誘導Gag抗原特異的CD8陽性T細胞が感染防御に寄与していることを示唆する結果も得られた。
多様性の高いHIVに対する有効なワクチンとして今後の進展に期待
HIVは粘膜上皮細胞には感染しないが、トランスサイトーシスや粘膜損傷部位を介して粘膜バリアを通過し、粘膜下でCD4陽性Tリンパ球等の標的細胞に感染して増殖すると考えられている。今回の研究で、ワクチン誘導CD8陽性T細胞によって、粘膜下でウイルス増殖が抑えられ、感染成立阻止にいたることを示唆する結果が示された。
今回の研究成果は、多様性の高い表面タンパク質抗原を用いないHIVワクチンで、初めて抗体非依存性の粘膜感染防御効果を示したもの。この抗原設計は、各種ウイルスベクターなどを含むワクチンシーズにも応用が可能だ。同研究の新規抗原を導入したHIVワクチンについて研究グループは、「多様性への交差性の高い有効なワクチンとして、臨床試験有効性評価段階への進展も含めて今後の発展が期待される」と、述べている。
▼関連リンク
・東京大学医科学研究所 プレスリリース




